Clear Sky Science · es
Variantes bialélicas en RNU2-2 causan el trastorno neurodesarrollativo recesivo conocido más prevalente
Pistas ocultas en el ADN familiar
Algunas de las afecciones cerebrales infantiles más graves han quedado durante mucho tiempo sin explicación, dejando a las familias sin respuestas claras ni orientación. Este estudio descubre una de las causas hereditarias más comunes de esas afecciones, atribuyéndola no a un gen que codifica proteínas sino a un diminuto fragmento de ARN que ayuda a las células a procesar los mensajes genéticos. Comprender este nuevo trastorno no solo ofrece diagnósticos largamente esperados para muchas familias, sino que también abre opciones prácticas para pruebas de portadores, planificación familiar y una atención más temprana para los niños afectados. 
Un ARN diminuto con una gran tarea
Nuestras células necesitan editar los mensajes genéticos crudos antes de que puedan usarse para fabricar proteínas. Esta edición, llamada empalme (splicing), la realiza una gran maquinaria conocida como espliceosoma. Uno de sus componentes clave es el ARN pequeño U2, una molécula de ARN corta que ayuda a reconocer dónde deben cortarse y unirse los fragmentos del código genético. El gen RNU2-2 codifica una versión de este ARN U2. Hasta hace poco, se sabía que las alteraciones en este y en genes de ARN relacionados causaban trastornos cerebrales de forma dominante —donde una sola copia defectuosa basta para provocar la enfermedad. El nuevo trabajo revela que cuando ambas copias de RNU2-2 están dañadas, surge una forma diferente, recesiva, de trastorno neurodesarrollativo, y es sorprendentemente común.
Descubriendo un trastorno cerebral hereditario común
Los investigadores examinaron datos genéticos de decenas de miles de personas con condiciones raras inscritas en el proyecto 100.000 Genomas del Reino Unido y en programas genómicos del Servicio Nacional de Salud. Usando una herramienta estadística diseñada para encontrar variantes raras causantes de enfermedad, compararon genes no codificantes de proteínas en más de 14.000 individuos con problemas neurodesarrollativos frente a más de 50.000 sin tales diagnósticos. Solo dos genes destacaron, RNU4-2 y RNU2-2, pero cuando buscaron específicamente cambios que actúen de forma recesiva —donde una persona debe heredar una copia alterada de cada progenitor— RNU2-2 mostró evidencia abrumadora. Identificaron 18 familias de alta confianza en las que los niños afectados portaban dos variantes dañinas de RNU2-2 en copias opuestas del gen, además de familias candidatas adicionales y nueve casos más procedentes de cohortes independientes en Estados Unidos, Italia y Países Bajos. 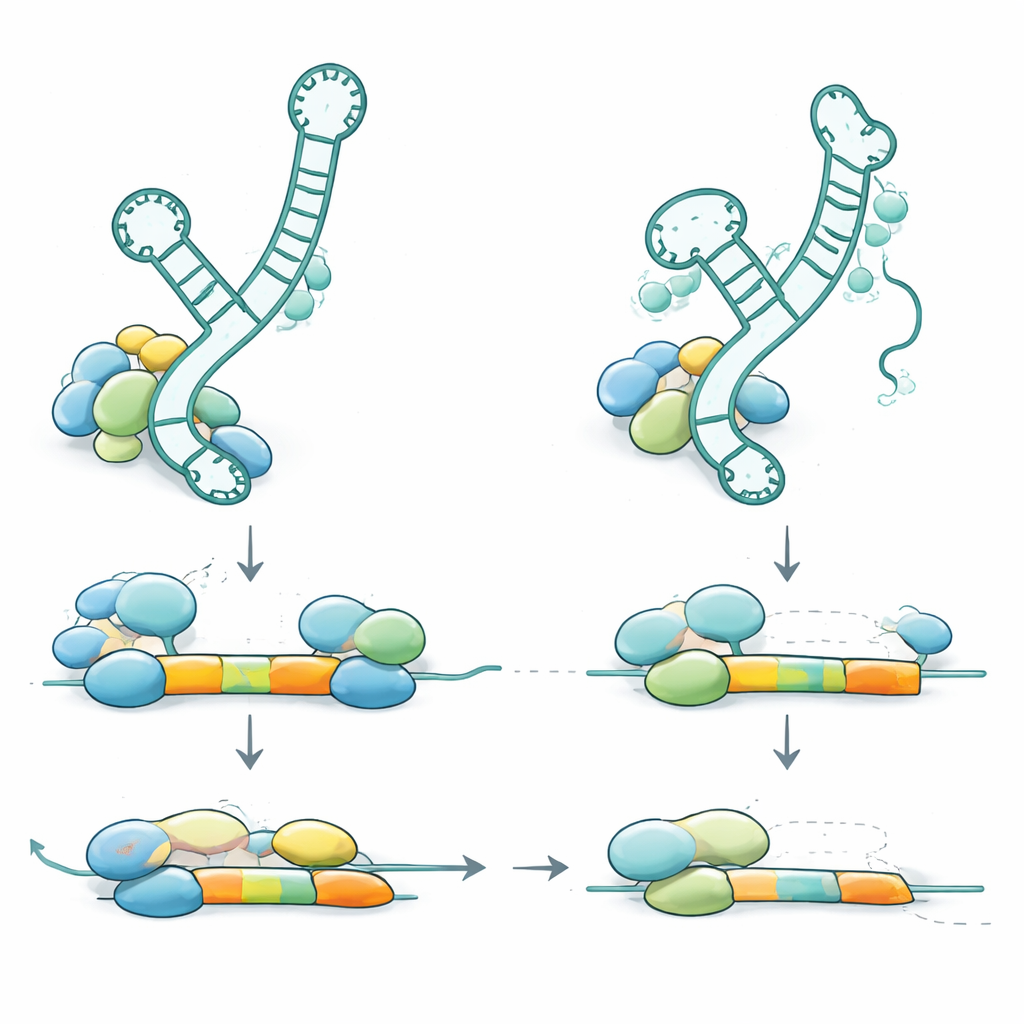
Cómo se manifiesta la condición en la vida real
Los niños con este síndrome recesivo de RNU2-2 suelen acudir a atención médica en la infancia o la primera niñez. La mayoría presentan retrasos en alcanzar hitos del desarrollo, como sentarse, caminar o hablar, y muchos tienen discapacidad intelectual de moderada a grave. Las convulsiones son muy frecuentes y pueden empezar temprano; en algunos niños evolucionan hacia síndromes epilépticos difíciles de tratar. El tono muscular y el movimiento suelen verse afectados, con un espectro que va desde hipotonía en la infancia hasta rigidez, posturas anormales o movimientos involuntarios en etapas posteriores. Las exploraciones cerebrales pueden parecer inicialmente normales pero más tarde mostrar pérdida de tejido cerebral o cambios en la materia blanca que conecta distintas regiones. Algunas personas presentan afectación leve y permanecen relativamente estables, mientras que otras desarrollan complicaciones graves, incluidos problemas respiratorios, de alimentación y, en casos raros, muerte temprana.
Cómo las alteraciones en RNU2-2 perturban la edición celular
Para entender cómo estas variaciones genéticas causan la enfermedad, el equipo examinó dónde caen las variantes dentro del ARN U2-2 y cómo afectan su estructura y comportamiento. Muchas de las variantes recesivas se predice que debilitan estructuras de tallo‑bucle —pequeñas horquillas en el ARN que le ayudan a unirse a proteínas asociadas y a otros ARN. Otras se sitúan directamente en la región que reconoce los sitios de empalme o en el sitio de acoplamiento para un anillo de proteínas ayudantes. Cuando los investigadores analizaron muestras de sangre, encontraron que las copias defectuosas de RNU2-2 se expresaban a menos del 10% de los niveles normales en los individuos afectados, lo que indica que el ARN alterado es inestable y se destruye en gran medida. El organismo compensa en parte aumentando la expresión de un gen U2 relacionado (RNU2-1), de modo que los niveles totales de U2 se mantienen aproximadamente normales, pero esta compensación no es suficiente para evitar la enfermedad. En portadores sanos que tienen solo una copia defectuosa, el ARN dañado también está muy reducido, sin embargo la copia normal restante incrementa su producción, manteniendo la función global por encima del umbral de aparición de síntomas.
Por qué este descubrimiento importa para las familias
Debido a que este síndrome sigue una herencia recesiva, tiende a repetirse entre hermanos cuando ambos progenitores son portadores sanos. En el proyecto genómico del Reino Unido, el síndrome recesivo de RNU2-2 representa aproximadamente una de cada diez familias con un diagnóstico recesivo neurodesarrollativo conocido, lo que lo convierte en la causa única más frecuente en esa categoría y casi tan común como un trastorno dominante descrito anteriormente causado por un gen de ARN espliceosomal distinto. De forma crucial, los autores muestran que una simple prueba de ARN en sangre puede ayudar a distinguir variantes verdaderamente dañinas de las inocuas midiendo cuánto se pierde de RNU2-2 y cuánto se incrementa el respaldo RNU2-1. Para las familias, esto significa diagnósticos más claros, mejores estimaciones del riesgo de recurrencia y la posibilidad de asesoramiento genético preconcepcional o prenatal —convirtiendo un fragmento oscuro de la biología del ARN en información práctica para decisiones médicas del mundo real.
Cita: Greene, D., Mendez, R., Lees, J. et al. Biallelic variants in RNU2-2 cause the most prevalent known recessive neurodevelopmental disorder. Nat Genet 58, 774–781 (2026). https://doi.org/10.1038/s41588-026-02539-5
Palabras clave: trastorno neurodesarrollativo, herencia recesiva, espliceosoma, ARN nuclear pequeño, secuenciación del genoma