Clear Sky Science · it
Una famiglia di tre generazioni con associazione VACTERL risulta portatrice di una rara forma di anemia di Diamond-Blackfan
Indizi familiari per un disturbo del sangue nascosto
Alcune famiglie sembrano portare attraverso le generazioni un filo di problemi di salute misteriosi, da conformazioni ossee inusuali a disturbi del sangue che insospettiscono i medici. Questo articolo segue una di queste famiglie e mostra come la moderna lettura del DNA dell’intero genoma possa smascherare una rara malattia ereditaria del sangue che si nasconde dietro un complesso insieme di difetti congeniti.
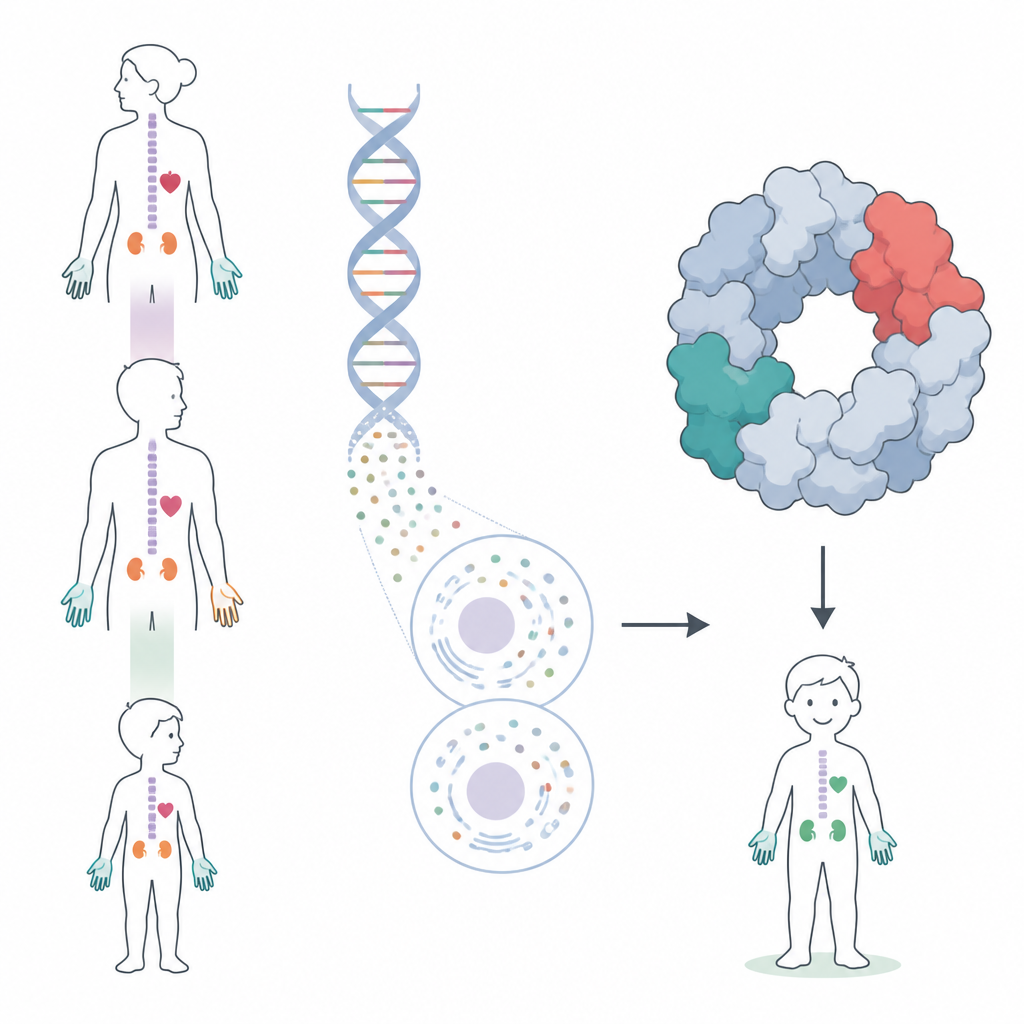
Molte differenze congenite, una storia familiare
La storia inizia con un bambino nato con diverse anomalie strutturali: ossa del pollice mancanti e supplementari, alterazioni della colonna vertebrale e delle costole, difetti cardiaci, un rene assente, crescita scarsa e ipotiroidismo. Gli esami del sangue durante l’infanzia hanno mostrato periodi di riduzione dei globuli rossi e bianchi. Anche la madre, la nonna e altri parenti presentavano miscele di problemi agli arti, alla colonna e alla tiroide, oltre a conte ematiche bianche basse, suggerendo una causa ereditaria condivisa piuttosto che una serie di eventi scollegati.
Districare condizioni simili nell’aspetto
I medici inizialmente sospettarono l’associazione VACTERL, un’etichetta usata quando un bambino presenta un particolare raggruppamento di difetti congeniti che interessano la colonna, l’intestino, il cuore, la trachea, i reni e gli arti. Tuttavia, VACTERL può sovrapporsi a diversi altri disturbi rari, inclusa l’anemia di Fanconi e una condizione legata ai ribosomi chiamata anemia di Diamond-Blackfan, che colpisce principalmente la formazione del sangue. Poiché questi disturbi possono apparire simili esternamente ma derivare da cause genetiche diverse e comportare rischi differenti, il team ha scelto di non limitare i test a un piccolo insieme di geni noti. Invece, ha letto il DNA di quasi tutti i membri della famiglia mediante sequenziamento dell’intero genoma.
Individuare alterazioni nelle “fabbriche” proteiche cellulari
Il sequenziamento dell’intero genoma ha rivelato cambiamenti rari in due geni, RPL18 e RPS6, che entrambi codificano parti delle “fabbriche” proteiche cellulari note come ribosomi. Queste fabbriche costruiscono tutte le proteine del corpo, e danni ai loro componenti possono compromettere la crescita e la formazione del sangue. La stessa variazione in RPL18 è comparsa in tutti i parenti affetti ma non nei membri sani della famiglia, indicando fortemente che si tratta del principale colpevole. La variazione in RPS6 era presente solo nel bambino e nella madre, che avevano problemi più gravi, suggerendo che potesse aggravare lievemente il difetto principale piuttosto che causare la malattia da sola.
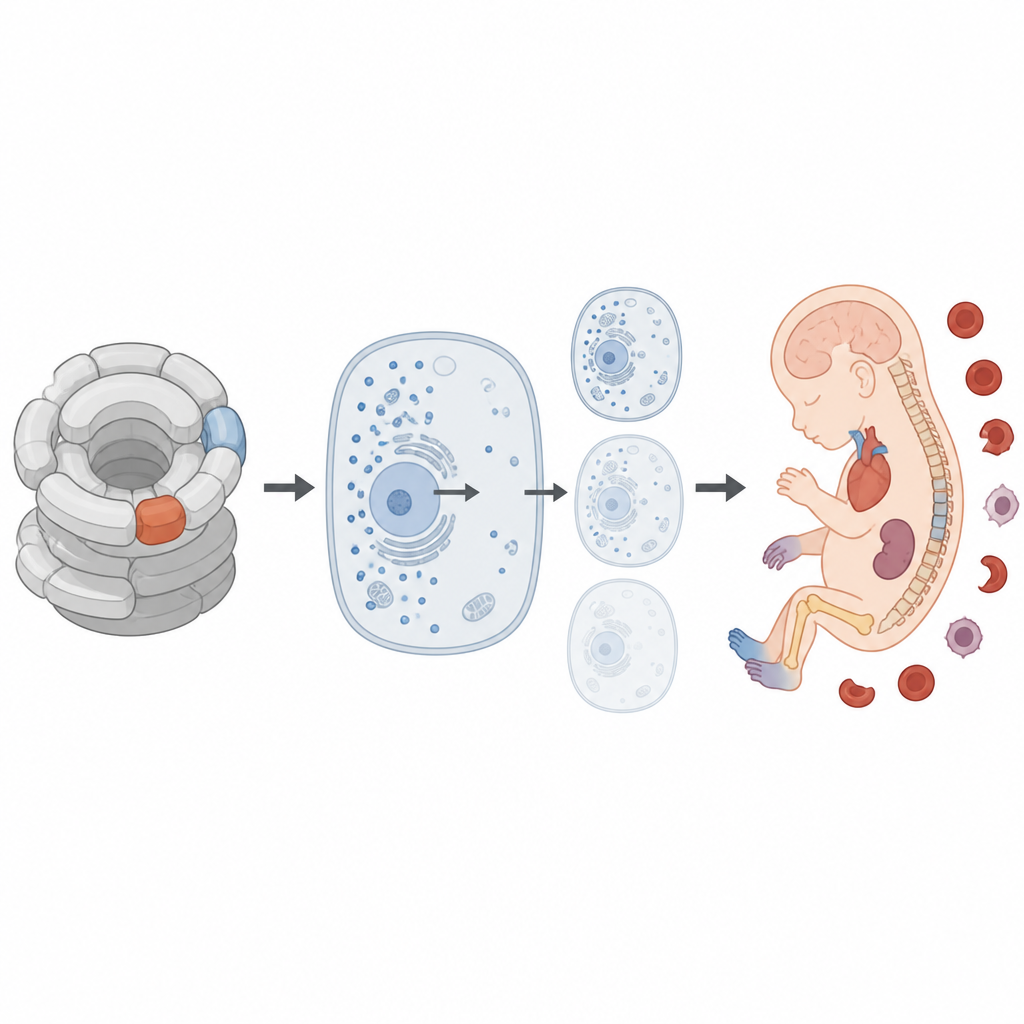
Testare i geni sospetti in laboratorio
Per capire come si comportano questi geni alterati all’interno delle cellule, i ricercatori hanno prodotto versioni fluorescenti delle proteine normali e mutanti e le hanno osservate in linee cellulari umane. La proteina RPL18 alterata era meno stabile, si degradava più rapidamente e mostrava una distribuzione anomala all’interno della cellula, in particolare nelle aree dove i ribosomi vengono assemblati. Soprattutto, le cellule che portavano la RPL18 alterata producevano complessivamente meno proteine nuove. In confronto, la proteina RPS6 alterata risultava anch’essa in quantità ridotta e con una distribuzione cellulare modificata, ma non rallentava in modo misurabile la sintesi proteica. Modelli computazionali della struttura proteica hanno supportato queste osservazioni, prevedendo che entrambe le varianti destabilizzassero le rispettive proteine, con l’alterazione di RPL18 che esercita l’effetto maggiore.
Cosa significa per diagnosi e cura
Nel complesso, la storia clinica, il quadro familiare, la modellizzazione al computer e gli esperimenti cellulari mostrano che la condizione di questa famiglia corrisponde a una rara forma di anemia di Diamond-Blackfan legata a RPL18, con un possibile contributo aggiuntivo della variante in RPS6 in alcuni membri. Il lavoro evidenzia come un ampio e imparziale sequenziamento del genoma possa rivelare un disturbo ematologico sottostante in pazienti inizialmente classificati solo come affetti da associazione VACTERL. Per le famiglie, questo tipo di diagnosi precisa può indirizzare il monitoraggio per futuri problemi ematici e guidare i test sui parenti, trasformando un insieme confuso di sintomi in una spiegazione condivisa e più chiara.
Citazione: Leshchynska, I., Das, D., O’Reilly, V. et al. A three generation family with VACTERL association is found to have a rare form of diamond-blackfan anaemia. Eur J Hum Genet 34, 619–629 (2026). https://doi.org/10.1038/s41431-026-02076-z
Parole chiave: Anemia di Diamond-Blackfan, proteine ribosomiali, associazione VACTERL, sequenziamento dell’intero genoma, malformazioni congenite