Clear Sky Science · es
Una familia de tres generaciones con asociación VACTERL resulta tener una forma rara de anemia de Diamond-Blackfan
Pistas familiares sobre un trastorno sanguíneo oculto
Algunas familias parecen portar un hilo misterioso de problemas de salud a lo largo de generaciones, desde formas óseas inusuales hasta alteraciones sanguíneas que desconciertan a los médicos. Este artículo sigue a una de esas familias y muestra cómo la lectura moderna del genoma completo puede desenmascarar un raro trastorno sanguíneo heredado que se oculta tras una mezcla compleja de defectos congénitos.
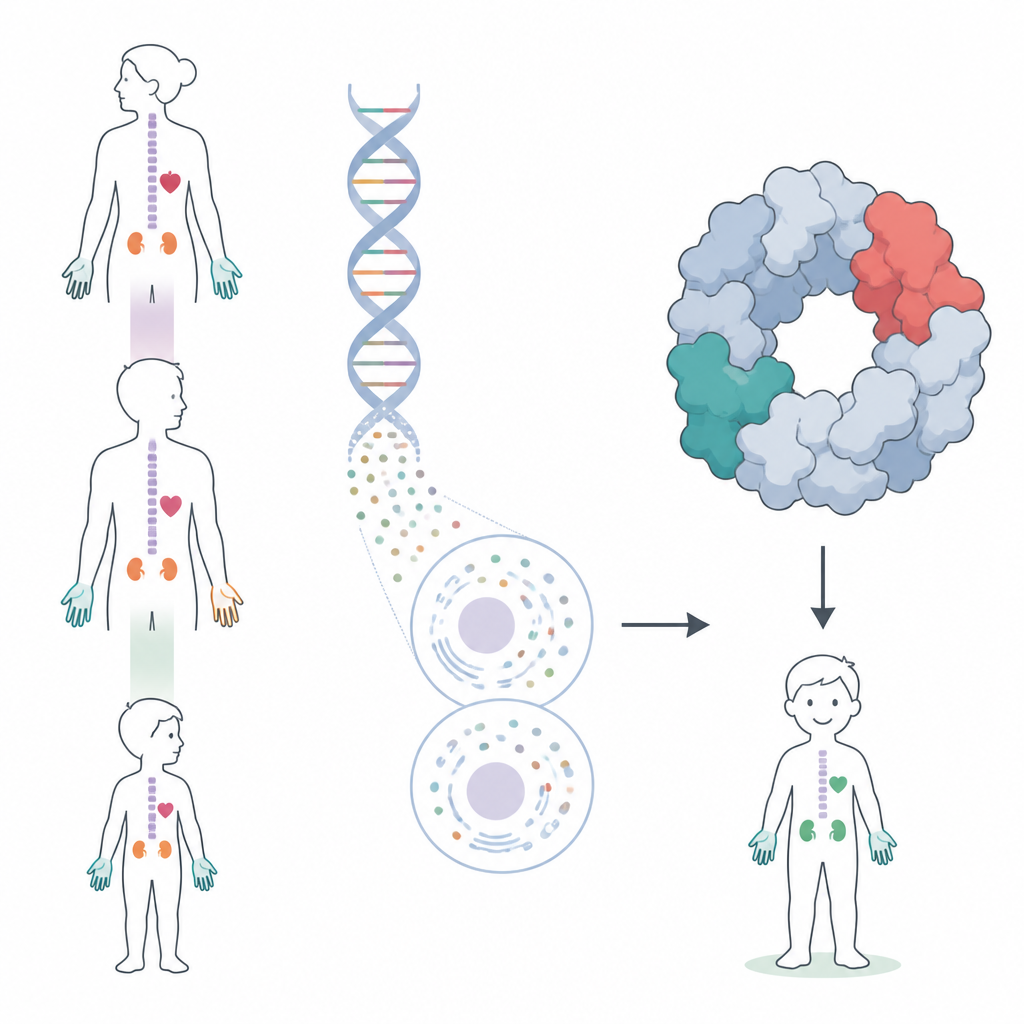
Muchas diferencias al nacer, una sola historia familiar
La historia comienza con un niño nacido con varias diferencias estructurales: falanges del pulgar ausentes y supernumerarias, alteraciones de la columna y las costillas, cardiopatías, un riñón ausente, crecimiento deficiente y una tiroides poco activa. Análisis de sangre durante la infancia revelaron periodos de disminución de glóbulos rojos y blancos. Su madre, su abuela y otros familiares también presentaban combinaciones de problemas en las extremidades, la columna y la tiroides, además de recuentos bajos de glóbulos blancos, lo que sugería una causa hereditaria compartida más que una serie de eventos no relacionados.
Desentrañando condiciones que se parecen entre sí
Los médicos sospecharon inicialmente asociación VACTERL, una etiqueta usada cuando un niño presenta un cúmulo particular de defectos congénitos que afectan la columna, el intestino, el corazón, la tráquea, los riñones y las extremidades. Sin embargo, VACTERL puede solaparse con varios otros trastornos raros, incluida la anemia de Fanconi y una condición relacionada con el ribosoma llamada anemia de Diamond-Blackfan, que afecta principalmente a la formación de la sangre. Dado que estas enfermedades pueden parecer similares externamente pero derivar de causas genéticas distintas y con riesgos diferentes, el equipo decidió no limitar las pruebas a un pequeño conjunto de genes conocidos. En su lugar, analizaron casi todo el ADN de los miembros de la familia mediante secuenciación del genoma completo.
Encontrando cambios en las fábricas de proteína celulares
La secuenciación del genoma completo descubrió cambios raros en dos genes, RPL18 y RPS6, que ambos codifican partes de las fábricas de proteínas celulares conocidas como ribosomas. Estas fábricas construyen todas las proteínas del organismo, y el daño a sus componentes puede interrumpir el crecimiento y la formación de la sangre. El mismo cambio en RPL18 apareció en todos los familiares afectados pero no en los miembros sanos de la familia, lo que apunta con fuerza a que es el principal culpable. El cambio en RPS6 estaba presente solo en el niño y en su madre, que tenían problemas más graves, lo que sugiere que podría agravar ligeramente el defecto principal en lugar de causar la enfermedad por sí solo.
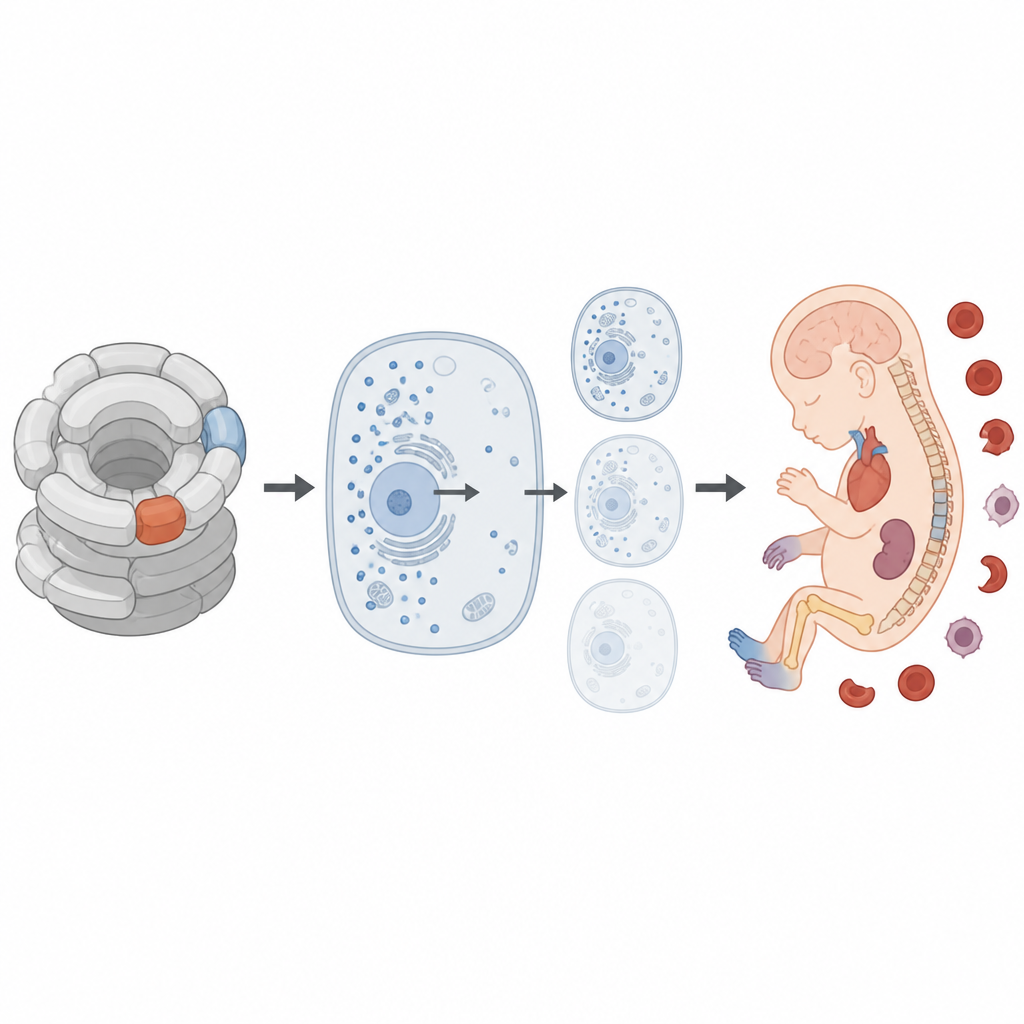
Probando los genes sospechosos en el laboratorio
Para ver cómo se comportan estos genes alterados dentro de las células, los investigadores crearon versiones fluorescentes de las proteínas normales y alteradas y las observaron en líneas celulares humanas. La proteína RPL18 alterada era menos estable, se degradaba más rápido y mostraba un patrón anormal dentro de la célula, especialmente en las zonas donde se ensamblan los ribosomas. Lo más importante, las células que portaban la RPL18 alterada producían menos proteínas nuevas en general. En contraste, la proteína RPS6 alterada también estaba reducida en cantidad y presentaba un patrón celular cambiado, pero no ralentizó de forma medible la producción proteica. Modelos computacionales de la forma proteica respaldaron estas observaciones, prediciendo que ambos cambios desestabilizarían sus proteínas, con el cambio en RPL18 teniendo el efecto más fuerte.
Qué significa esto para el diagnóstico y el cuidado
En conjunto, la historia clínica, el patrón familiar, la modelización por ordenador y los experimentos celulares muestran que la condición de esta familia encaja con una forma rara de anemia de Diamond-Blackfan ligada a una RPL18 defectuosa, con un posible efecto aditivo del cambio en RPS6 en algunos miembros. El trabajo subraya cómo la secuenciación genómica amplia e imparcial puede revelar un trastorno sanguíneo subyacente en pacientes considerados inicialmente con asociación VACTERL solamente. Para las familias, este tipo de diagnóstico preciso puede orientar la vigilancia de futuros problemas hematológicos e informar sobre las pruebas a parientes, convirtiendo una colección confusa de síntomas en una explicación compartida y más clara.
Cita: Leshchynska, I., Das, D., O’Reilly, V. et al. A three generation family with VACTERL association is found to have a rare form of diamond-blackfan anaemia. Eur J Hum Genet 34, 619–629 (2026). https://doi.org/10.1038/s41431-026-02076-z
Palabras clave: Anemia de Diamond-Blackfan, proteínas ribosomales, asociación VACTERL, secuenciación del genoma completo, malformaciones congénitas