Clear Sky Science · he
השתלת מיקרוביוטה צואתית בתוספת אימונו-תרפיה בסרטן ריאות שאינו תאי-סל ובלוטת המלנומה: הניסוי פאזה 2 FMT-LUMINate
מדוע המעי שלכם עשוי להיות חשוב בטיפול בסרטן
תרופות לסרטן שמְעוררות את מערכת החיסון שינו את הפרספקטיבה עבור רבים מהחולים עם מחלת ריאות מתקדמת ומלנומה. יחד עם זאת, בערך לחצי מהמטופלים התרופות הללו אינן יעילות דיה. המחקר הזה שואל שאלה מפתיעה עם השלכות מעשיות: האם שינוי קהילת המיקרובים שחיים במעי — באמצעות חומר צואת תורמים בריאים — יכול להפוך תרופות מבוססות-חיסון ליעילות יותר ולחשוף מדוע לעיתים הן גורמות לתופעות לוואי חמורות?
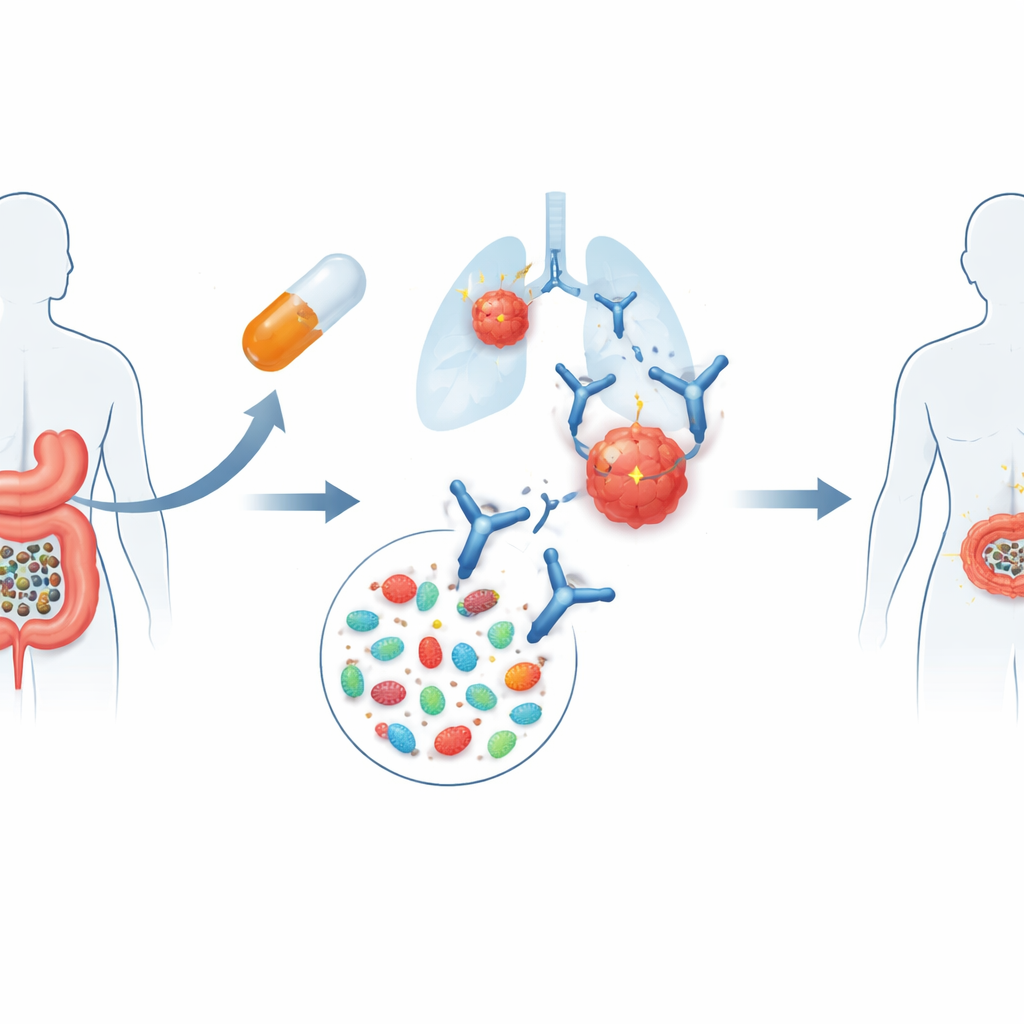
שימוש בצואת תורם כטיפול מסייע
ניסוי FMT-LUMINate בדק רעיון פשוט אך נועז. חולים עם סרטן ריאות שאינו תאי-סל או מלנומה מתקדמת, שהתכוננו להתחיל טיפול סטנדרטי בחסימות נקודות בדיקה חיסוניות, בלעו תחילה קפסולות המכילות צואה שעובדה מתורמים בריאים שעברו סינון קפדני. הליך זה, הידוע כהשתלת מיקרוביוטה צואתית (FMT), נועד לאפס את אקוסיסטמת המעי. בתוך שבוע החלו החולים את האימונו-תרפיה הרגילה שלהם: חולי ריאות קיבלו תרופה בודדת שמטרה שלה PD-1, בעוד חולי מלנומה קיבלו שילוב שמכוון גם ל-PD-1 וגם ל-CTLA-4, משטר אינטנסיבי יותר הידוע כעוצמתי אך גם רעיל יותר.
תגובות חזקות יותר ממה שציפו
בקבוצת סרטן הריאות, ל-16 מתוך 20 חולים הגידולים התקצרו — שיעור תגובה אובייקטיבי של 80% — גבוה באופן בולט לעומת שיעורי ההצלחה סביב 40–45% הנמדדים בדרך כלל עבור אותה תרופה כשלעצמה. רוב השאר שמרו על היכולת של המחלה להיות יציבה במשך שישה חודשים או יותר, וכולם היו עדיין בחיים שנה לאחר תחילת הטיפול. בקבוצת המלנומה שטופלה בשילוב התרופתי, 15 מתוך 20 חולים הגיבו, כולל ארבע תגובות של ריפוי מוחלט, שוב מעל לציפיות ההיסטוריות. תוצאות אלה מרמזות שקורס יחיד של FMT מתורם בריא, שניתן לפני האימונו-תרפיה, יכול להגביר באופן משמעותי את הסיכויים שהתרופות החזקות הללו יעבדו.
בטיחות: כשהמיקרובים במעי נפגשים עם תרופות עוצמתיות
תמונת הבטיחות נראתה שונה בהתאם לסוג הסרטן ולבסיס הטיפולי. בחולי סרטן ריאות שקיבלו רק טיפול חוסם PD-1, לא זוהו תופעות לוואי חמורות (דרגה 3 או יותר) שיוכחו כמשויכות לשילוב של FMT ותמיכה אימונית. בחולי מלנומה במשטר הדו-תרופתי, לעומת זאת, בעיות חיסוניות חמורות כגון שלשול חמור, קוליטיס ודלקת בלב (מיוקרדיטיס) היו שכיחות יותר והופיעו מוקדם יותר מהמקובל. ניתוח גנטי מוקפד של דגימות צואה של תורמים וחולים הצביע על תורם אחד שהמעי שלו היה עשיר בקבוצה של חיידקים הקרואים Prevotella. כל מקבלי הצואה של אותו תורם בקבוצת הטיפול המשולב פיתחו תופעות לוואי חמורות, בעוד שתורמים דומים לא גרמו לאותה בעיה כאשר שוּלבו עם טיפול בודד. הממצא הזה מדגיש כי בטיחות ה-FMT עשויה להיות תלויה מאוד גם במיקרוביולוגיה של התורם וגם בשילוב התרופתי הספציפי נגד הסרטן.
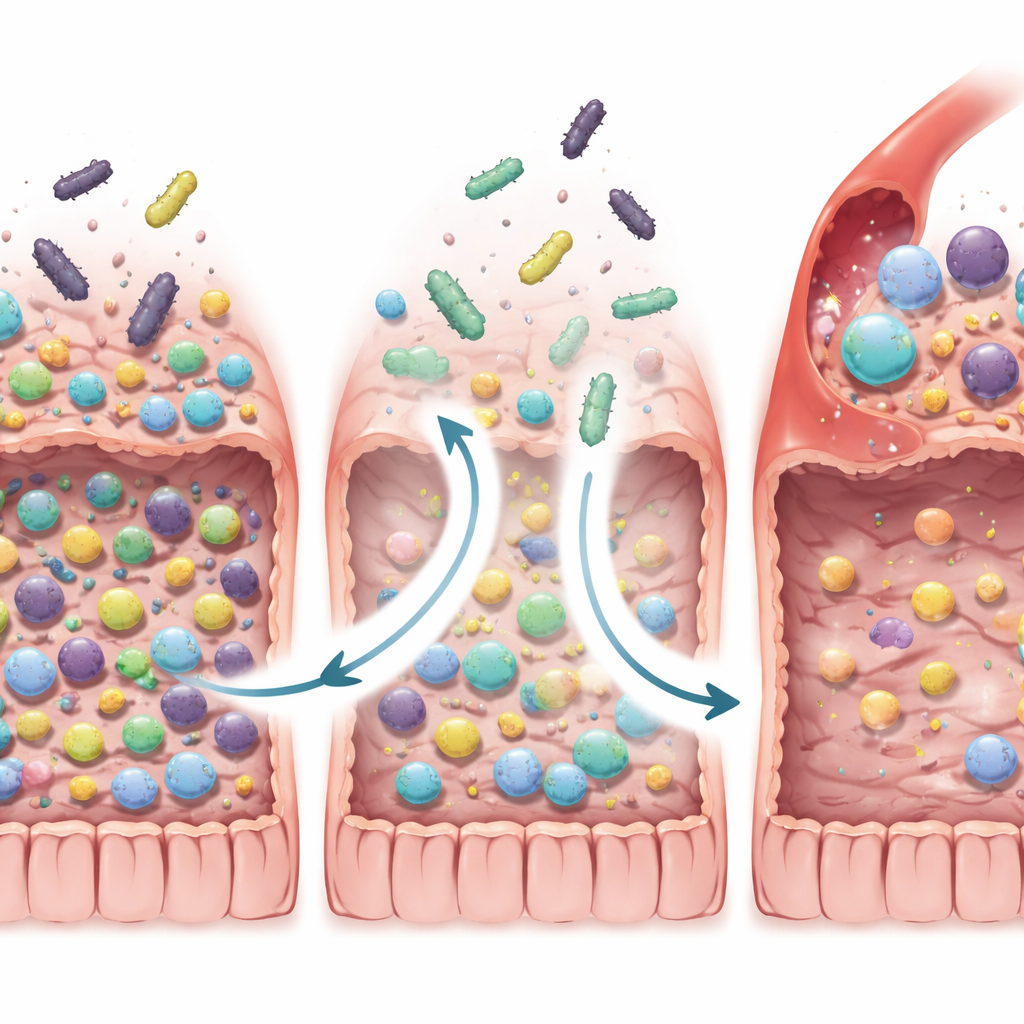
תוצאות טובות קשורות לאובדן המיקרובים הלא-נכונים
המדענים חקרו עמוק יותר כיצד ה-FMT עיצב מחדש את אקוסיסטמת המעי. ציפו שחולים שמצבם השתפר אולי פשוט יקבלו יותר מה"חיידקים הטובים" של התורם. במקום זאת נמצאה תופעה עדינה יותר: מגיבים נטו לאבד חלק גדול יותר מהמינים החיידקיים שהיו להם בתחילת המחלה, במיוחד מיקרובים מסוימים שקישרו בעבר לעמידות לאימונו-תרפיה ולדלקת כרונית, כולל מינים ספציפיים של Enterocloster, Clostridium, Streptococcus ו-Dialister. הדפוס הזה נצפה לא רק ב-FMT-LUMINate אלא גם כשצוות החוקרים ניתח מחדש נתונים משלושה ניסויי FMT מול סרטן קודמים. בעכברים במעבדה, החזרת אותם חיידקים "שאבדו" לחיות שקיבלו צואה ממגיבים החלישה את השפעות ההגנה על הגידול של האימונו-תרפיה, ותומכת ברעיון שהיפטרות מתושבים מזיקים היא קריטית.
הדים בחילוף החומרים ובמערכת החיסון
הסרת מיקרובים מטרידים לא שינתה רק את מפה המעי על הנייר — היא שינתה כימיה וחיסון בכל הגוף. חולים שאיבדו יותר מהמיקרובים הבסיסיים שלהם הראו פרופילי מטבוליטים בדם שונים, במיוחד בחומרים המיוצרים מחומצת האמינו טריפטופאן. לא-מגיבים ואילו ששמרו יותר מהמיקרובים המקוריים שלהם הגביהו רמות של מטבוליטים כגון חומצה קינולינית וקינורנין, שקושרו לדיכוי חיסוני ולתגובות גרועות לאימונו-תרפיה בסרטן. במקביל, חולים עם אובדן חיידקי גדול יותר הציגו יותר תאי CD8 שפועלים נגד סרטן ופחות תאי T רגולטוריים, שפועלים בדרך כלל כבלמים על התגובות החיסוניות. יחד, השינויים הללו מרמזים על סביבה עוינת יותר לגידולים ונדיבה יותר לתאי החיסון המלחמים בסרטן.
מה אומר הדבר לטיפול העתידי בסרטן
לא-מומחים, המסר המרכזי הוא שהמיקרובים שכבר חיים במעי של המטופל יכולים או לעזור או להכשיל תרופות חדשניות נגד סרטן. מחקר פאזה 2 זה מראה שקורס יחיד של FMT מתורמים בריאים שבוצע בקפדנות יכול להגדיל בבטחה את שיעורי ההצלחה של אימונו-תרפיה בסרטן ריאות ומלנומה, תוך הדגשת הצורך בבחירת תורמים קפדנית כדי למנוע החמרה של תופעות לוואי מסוכנות. באופן מהותי, נראה שההטבה נובעת פחות מ"הוספת חרקים טובים" ויותר מ"פינוי הרעים". תובנה זו מציעה מפת דרכים לעיצוב טיפולים מבוססי-מיקרוביום דור הבא — בין אם FMT פשוט או קוקטיילים מיקרוביאליים מדויקים יותר — שמטרתם להוציא מינים מזיקים באופן סלקטיבי, לאזן מחדש מטבוליזם ולתת למערכת החיסון סיכוי ברור יותר להשמיד את הסרטן.
ציטוט: Duttagupta, S., Messaoudene, M., Hunter, S. et al. Fecal microbiota transplantation plus immunotherapy in non-small cell lung cancer and melanoma: the phase 2 FMT-LUMINate trial. Nat Med 32, 1337–1350 (2026). https://doi.org/10.1038/s41591-025-04186-5
מילות מפתח: השתלת מיקרוביוטה צואתית, אימונו-תרפיה בסרטן, מיקרוביום המעי, סרטן ריאות שאינו תאי-סל, מַלְנוֹמָה