Clear Sky Science · fr
Transplantation de microbiote fécal plus immunothérapie dans le cancer du poumon non à petites cellules et le mélanome : l’essai de phase 2 FMT-LUMINate
Pourquoi votre intestin pourrait compter dans le traitement du cancer
Les médicaments contre le cancer qui « réveillent » le système immunitaire ont transformé le pronostic de nombreuses personnes atteintes d’un cancer du poumon avancé et de mélanome. Pourtant, pour environ la moitié des patient·e·s, ces traitements ne sont pas suffisamment efficaces. Cette étude pose une question surprenante aux conséquences concrètes : modifier la communauté de microbes vivant dans l’intestin — en utilisant du matériel fécal de donneur·se·s sains — peut-il rendre les traitements immunitaires anticancéreux plus efficaces et révéler pourquoi ils provoquent parfois des effets indésirables graves ?
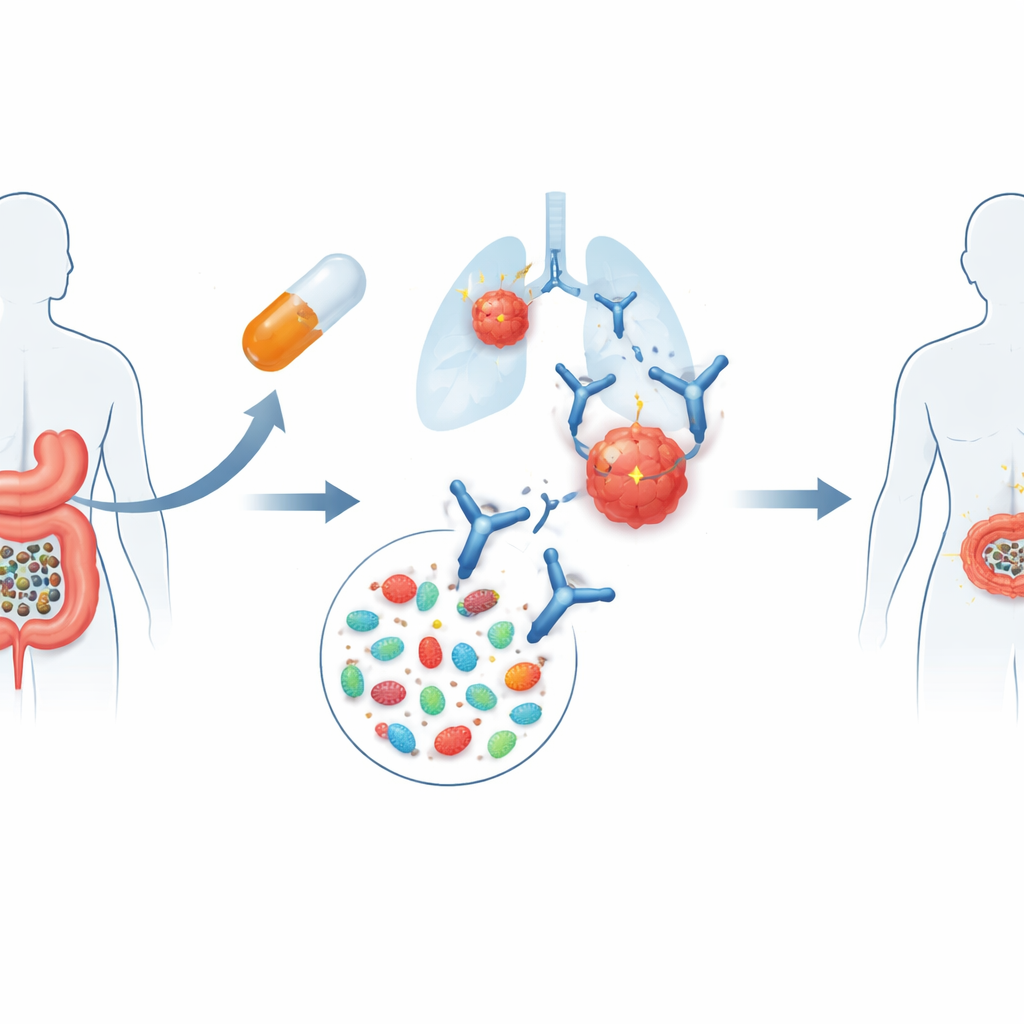
Utiliser les selles de donneur comme thérapie d’appoint
L’essai FMT-LUMINate a testé une idée simple mais audacieuse. Des patient·e·s atteints d’un cancer du poumon non à petites cellules avancé ou d’un mélanome, sur le point de débuter une immunothérapie par inhibiteur de point de contrôle standard, ont d’abord avalé des capsules contenant des selles traitées provenant de volontaires sains rigoureusement dépisté·e·s. Cette procédure, appelée transplantation de microbiote fécal (TMF), vise à réinitialiser l’écosystème intestinal. Dans la semaine qui a suivi, les patient·e·s ont commencé leur immunothérapie habituelle : les patient·e·s poumon ont reçu un médicament ciblant PD‑1 en monothérapie, tandis que les patient·e·s mélanome ont reçu une combinaison ciblant à la fois PD‑1 et CTLA‑4, un schéma plus intensif connu pour être puissant mais aussi plus toxique.
Réponses plus fortes que prévu
Dans le groupe cancer du poumon, 16 des 20 patient·e·s ont vu leurs tumeurs diminuer, soit un taux de réponse objective de 80 % — nettement supérieur aux taux d’environ 40–45 % rapportés habituellement pour ce même médicament en monothérapie. La plupart des patient·e·s restant ont au moins maintenu leur maladie stable pendant six mois ou plus, et tou·te·s étaient encore en vie un an après le début du traitement. Dans le groupe mélanome traité par immunothérapie combinée, 15 des 20 patient·e·s ont répondu, dont quatre réponses complètes, là encore au‑dessus des attentes historiques. Ces résultats suggèrent qu’une seule cure de TMF provenant de donneur·se·s sains, administrée avant l’immunothérapie, peut augmenter sensiblement les chances d’efficacité de ces médicaments puissants.
Sécurité : quand les microbes intestinaux rencontrent des médicaments puissants
La sécurité variait selon le type de cancer et le traitement associé. Chez les patient·e·s atteints de cancer du poumon recevant uniquement une thérapie bloquant PD‑1, aucun effet indésirable sévère (grade 3 ou plus) n’a été attribué à la combinaison TMF plus immunothérapie. En revanche, chez les patient·e·s mélanome sous schéma à deux médicaments, des problèmes immunitaires sévères tels que diarrhée grave, colite et inflammation cardiaque (myocardite) étaient plus fréquents et sont apparus plus tôt qu’habituellement. Une analyse génétique soignée des échantillons de selles des donneur·se·s et des patient·e·s a pointé un donneur dont le microbiote était riche en un groupe de bactéries appelé Prevotella. Tous·tes les receveur·se·s des selles de ce donneur dans le groupe à double thérapie ont développé des effets indésirables sévères, tandis que des donneur·se·s similaires n’ont pas causé de tels problèmes lorsqu’ils étaient associés à la monothérapie. Cela souligne que la sécurité de la TMF peut dépendre fortement à la fois de la composition microbienne du donneur et de la combinaison précise de médicaments anticancéreux.
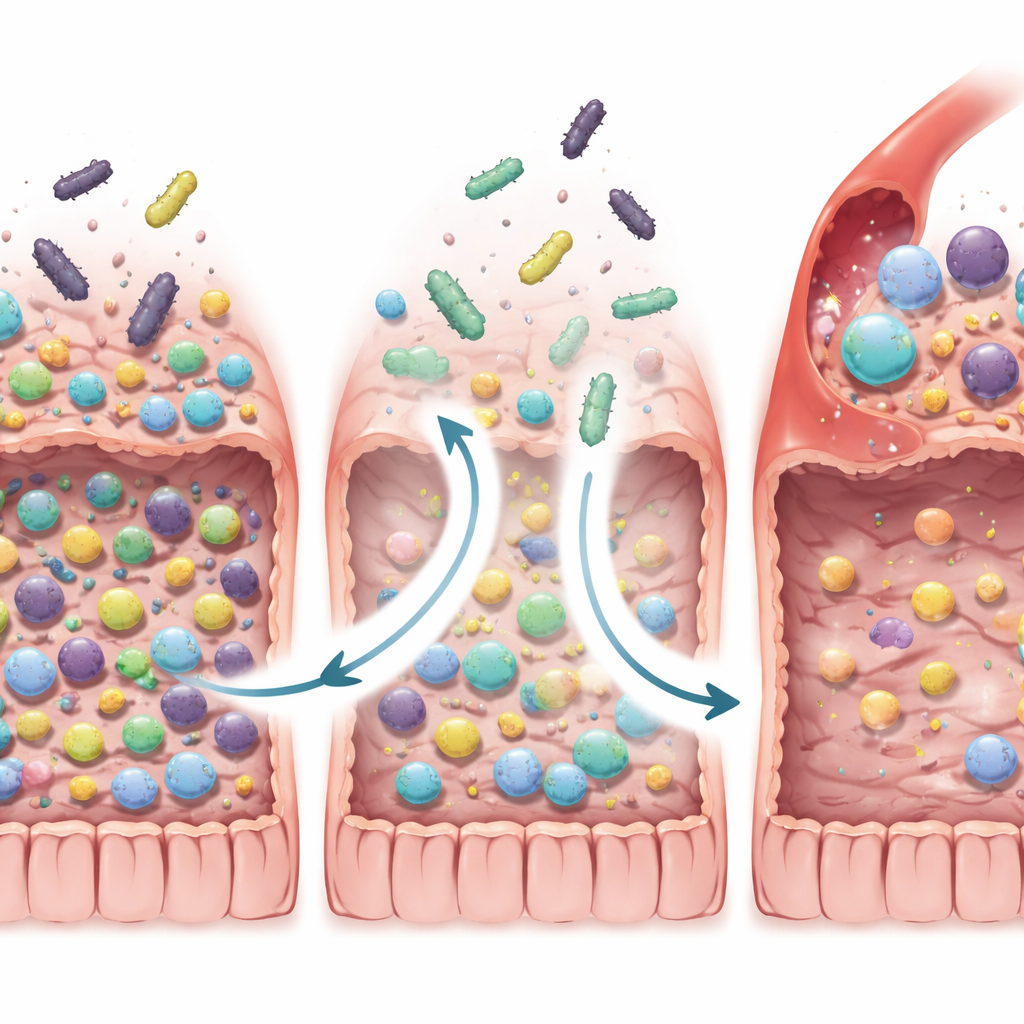
De bons résultats liés à la perte des mauvais microbes
Les chercheurs ont ensuite exploré plus en profondeur comment la TMF remodelait l’écosystème intestinal. Ils s’attendaient à ce que les patient·e·s qui allaient bien acquièrent simplement davantage des « bonnes » bactéries du·de la donneur·se. Ils ont trouvé quelque chose de plus subtil : les répondeur·se·s avaient tendance à perdre une plus grande fraction des espèces bactériennes qu’iels avaient au départ, en particulier certaines espèces antérieurement associées à la résistance à l’immunothérapie et à l’inflammation chronique, incluant des espèces spécifiques d’Enterocloster, Clostridium, Streptococcus et Dialister. Ce schéma a été observé non seulement dans FMT-LUMINate mais aussi lorsque l’équipe a réanalysé les données de trois essais FMT anticancéreux antérieurs. Chez la souris en laboratoire, la réintroduction de ces bactéries « perdues » chez des animaux ayant reçu des selles de répondeur·se·s a affaibli les effets antitumoraux de l’immunothérapie, soutenant l’idée que l’élimination de résidents nuisibles est cruciale.
Ondulations dans le métabolisme et le système immunitaire
La suppression des microbes problématiques n’a pas seulement modifié la carte microbienne : elle a altéré la chimie et l’immunité dans tout l’organisme. Les patient·e·s qui avaient perdu plus de leurs bactéries de départ présentaient des profils métabolites sanguins différents, notamment pour des composés dérivés de l’acide aminé tryptophane. Les non‑répondeur·se·s et celles et ceux qui avaient conservé davantage de leurs microbes originels montraient des taux plus élevés de métabolites tels que l’acide quinolinique et la kynurénine, liés à l’immunosuppression et à de mauvaises réponses à l’immunothérapie. Parallèlement, les patient·e·s ayant subi une plus grande perte bactérienne présentaient davantage de cellules T CD8 activées combattant le cancer et moins de cellules T régulatrices, qui agissent normalement comme freins sur les réponses immunitaires. Ensemble, ces modifications dessinent un environnement moins favorable aux tumeurs et plus propice aux cellules immunitaires anticancéreuses.
Ce que cela signifie pour les soins du cancer à venir
Pour un public non spécialiste, le message central est que les microbes déjà présents dans l’intestin d’un·e patient·e peuvent aider ou freiner les traitements anticancéreux de pointe. Cette étude de phase 2 montre qu’une seule TMF provenant de donneur·se·s sains soigneusement sélectionné·e·s peut augmenter en toute sécurité les taux de succès de l’immunothérapie pour le cancer du poumon et le mélanome, tout en soulignant la nécessité d’une sélection rigoureuse des donneur·se·s pour éviter d’amplifier des effets secondaires dangereux. Fait crucial, les bénéfices semblent moins venir de « rajouter des microbes bénéfiques » que d’« évincer les mauvais ». Cette insight offre une feuille de route pour concevoir des traitements microbiens de nouvelle génération — qu’il s’agisse de TMF ou de cocktails microbien plus raffinés — visant à éliminer sélectivement les espèces nuisibles, rééquilibrer le métabolisme et donner au système immunitaire une meilleure chance d’éradiquer le cancer.
Citation: Duttagupta, S., Messaoudene, M., Hunter, S. et al. Fecal microbiota transplantation plus immunotherapy in non-small cell lung cancer and melanoma: the phase 2 FMT-LUMINate trial. Nat Med 32, 1337–1350 (2026). https://doi.org/10.1038/s41591-025-04186-5
Mots-clés: transplantation de microbiote fécal, immunothérapie du cancer, microbiome intestinal, cancer du poumon non à petites cellules, mélanome