Clear Sky Science · ar
زرع ميكروبيوتا البرازية بالإضافة إلى العلاج المناعي في سرطان الرئة غير صغير الخلايا والميلانوما: التجربة المرحلية الثانية FMT-LUMINate
لماذا قد يكون لأمعائك دور في علاج السرطان
حوّلت الأدوية السرطانية التي «تنشط» الجهاز المناعي آفاق العلاج للعديد من الأشخاص المصابين بسرطان رئوي متقدم والميلانوما. ومع ذلك، فإن هذه الأدوية لا تعمل بشكل كافٍ بالنسبة لحوالي نصف المرضى. تطرح هذه الدراسة سؤالاً مفاجئاً ذو نتائج عملية: هل يمكن لتغيير مجتمع الميكروبات الساكنة في الأمعاء — باستخدام مادة برازية من متبرعين أصحاء — أن يجعل أدوية المناعة ضد السرطان أكثر فعالية ويكشف سبب تعرضها أحياناً لآثار جانبية خطيرة؟
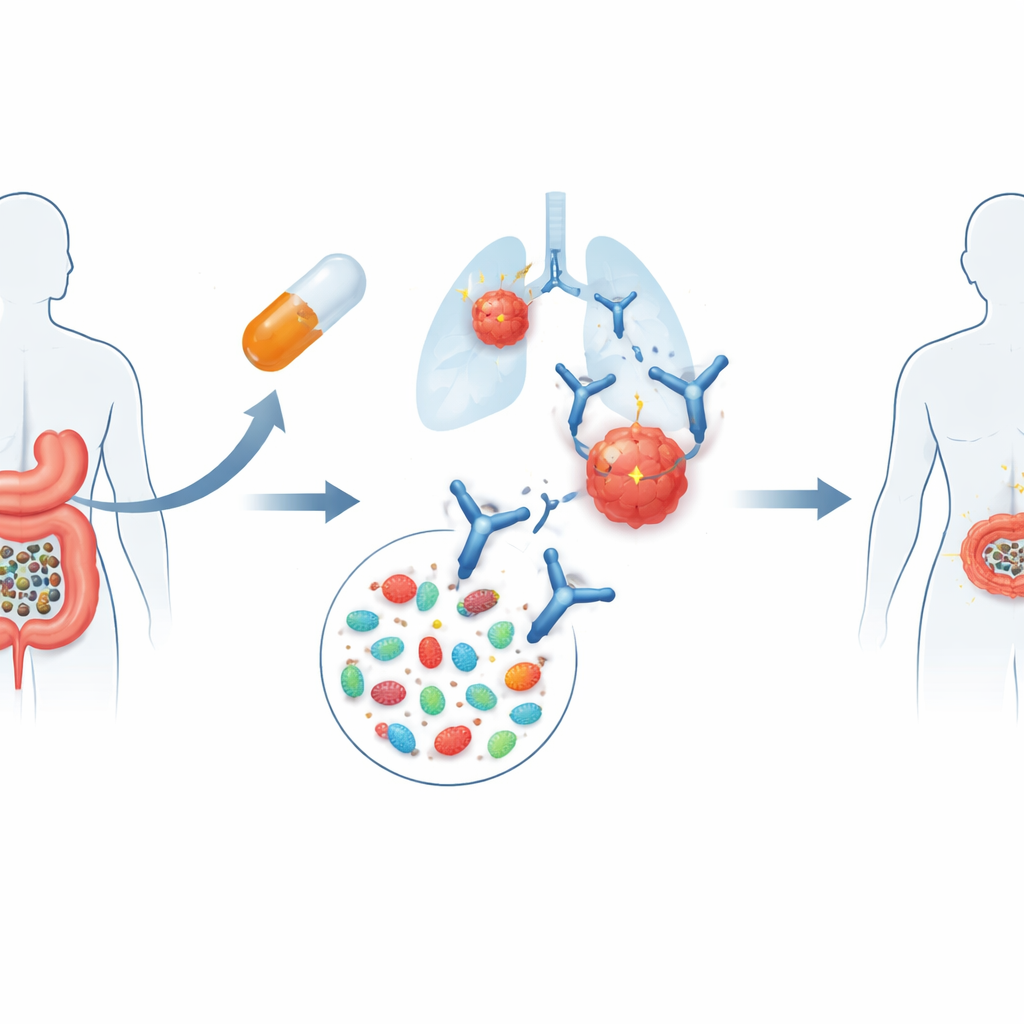
استخدام براز المتبرع كعلاج مساعد
اختبرت تجربة FMT-LUMINate فكرة بسيطة لكنها جريئة. تلقى المرضى المصابون بسرطان الرئة غير صغير الخلايا أو الميلانوما المتقدم، والذين كانوا على وشك بدء العلاج المعياري بعوامل منع نقاط التفتيش المناعية، كبسولات تحتوي على براز معالج من متطوعين أصحاء تم فحصهم بدقة. يهدف هذا الإجراء، المعروف باسم زرع ميكروبيوتا البراز، إلى إعادة ضبط نظام الأمعاء البيئي. وخلال أسبوع، بدأ المرضى علاجهم المناعي المعتاد للسرطان: تلقى مرضى الرئة دواءً واحداً يستهدف PD-1، بينما تلقى مرضى الميلانوما مزيجاً يستهدف كل من PD-1 وCTLA-4، وهو نظام أكثر كثافة معروف بقوته ولكنه أكثر سمية أيضاً.
استجابات أقوى مما كان متوقعاً
في مجموعة سرطان الرئة، شهد 16 من أصل 20 مريضاً تقلص أورامهم، بمعدل استجابة موضوعية قدره 80% — وهو أعلى بكثير من معدلات النجاح البالغ تقريباً 40–45% التي تُبلغ عادة عن نفس الدواء بمفرده. احتفظ معظم المرضى الباقين على الأقل باستقرار المرض لمدة ستة أشهر أو أكثر، وكان الجميع على قيد الحياة بعد سنة من بدء العلاج. في مجموعة الميلانوما المعالجة بالعلاج المركب، استجاب 15 من أصل 20 مريضاً، بما في ذلك أربع استجابات كاملة، مرة أخرى أعلى من التوقعات التاريخية. تشير هذه النتائج إلى أن دورة واحدة من زرع ميكروبيوتا متبرع صحي، تُعطى قبل العلاج المناعي، يمكن أن تزيد بشكل كبير من فرص فاعلية هذه الأدوية القوية.
السلامة: عندما تتفاعل ميكروبات الأمعاء مع أدوية قوية
بدت مسائل السلامة مختلفة باختلاف السرطان والأساس العلاجي. في مرضى سرطان الرئة الذين تلقوا علاجاً يثبط PD-1 فقط، لم تُنسب أي آثار جانبية شديدة (الدرجة 3 أو أعلى) إلى الجمع بين زرع الميكروبيوتا والبروتوكول المناعي. أما في مرضى الميلانوما الذين تناولوا نظام الدواء المزدوج، فكانت المشاكل المناعية الخطيرة مثل الإسهال الشديد، والتهاب القولون، والتهاب القلب (التهاب عضلة القلب) أكثر شيوعاً وظهرت في وقت أبكر مما يُرى عادة. أشارت تحليلات جينية دقيقة لعينات البراز من المتبرعين والمرضى إلى وجود متبرع واحد كان أمعاؤه غنية بمجموعة من البكتيريا تُدعى Prevotella. أصيب جميع متلقي براز هذا المتبرع في مجموعة العلاج المزدوج بآثار جانبية شديدة، بينما لم تتسبب مثل هذه المتبرعات في مشكلات عند اقترانها مع العلاج الدوائي الواحد. يبرز هذا أن سلامة زرع الميكروبيوتا قد تعتمد بشكل كبير على علم الأحياء الميكروبي للمتبرع وعلى تركيبة أدوية السرطان المستخدمة.
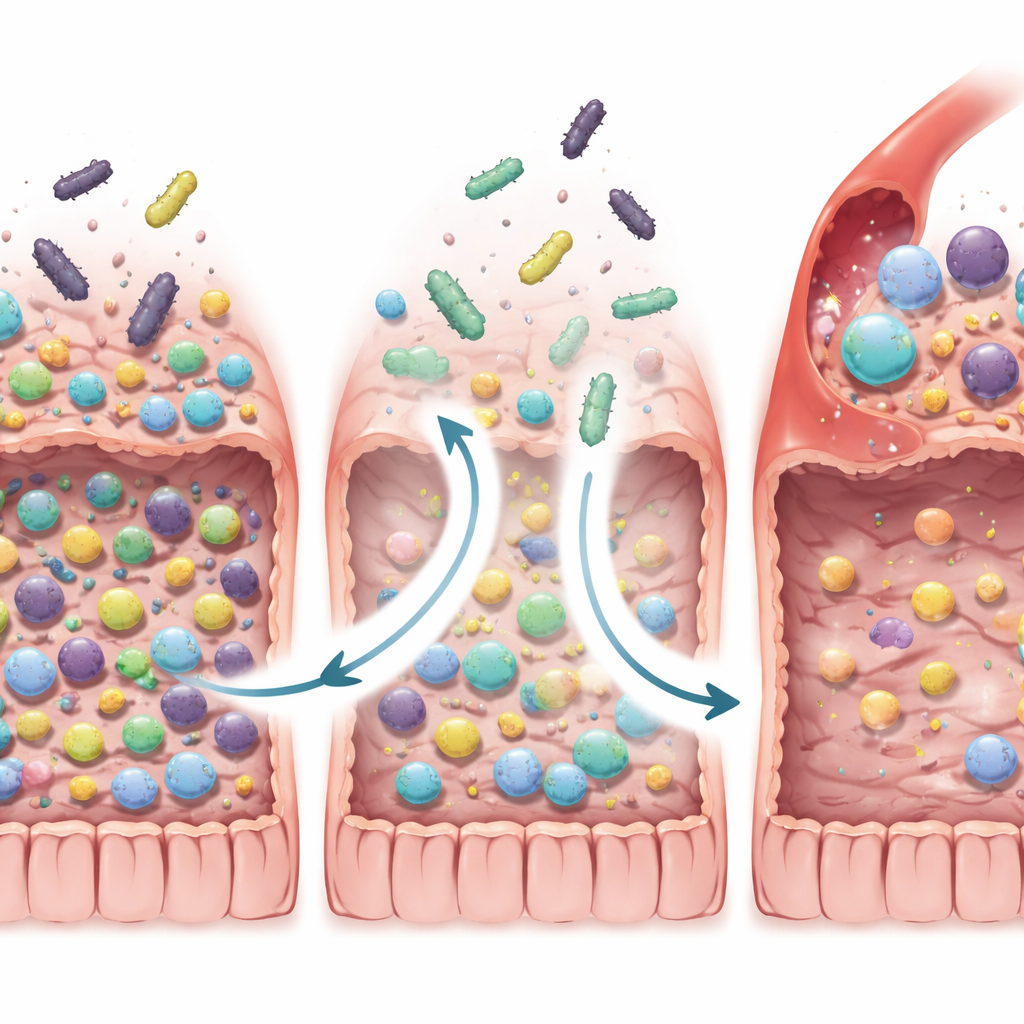
نتائج جيدة مرتبطة بفقدان الميكروبات الضارة
ثم تعمق العلماء في كيفية إعادة تشكيل زرع الميكروبيوتا لنظام الأمعاء البيئي. توقعوا أن المرضى الذين تحسنت حالتهم قد يكتسبون ببساطة المزيد من بكتيريا «المتبرع الجيدة». بدلاً من ذلك، وجدوا أمراً أكثر دقة: ميالون إلى الاستجابة فقدوا نسبة أكبر من أنواع البكتيريا التي كانت لديهم في البداية، لا سيما ميكروبات مرتبطة سابقاً بالمقاومة للعلاج المناعي والالتهاب المزمن، بما في ذلك أنواع محددة من Enterocloster وClostridium وStreptococcus وDialister. لوحظ هذا النمط ليس فقط في FMT-LUMINate ولكن أيضاً عندما أعاد الفريق تحليل بيانات من ثلاث تجارب زرع ميكروبيوتا سابقة على السرطان. وفي تجارب على الفئران، أدى إعادة إدخال هذه البكتيريا «المفقودة» إلى حيوانات تلقت براز المستجيبين إلى إضعاف تأثيرات العلاج المناعي المضاد للأورام، مما يدعم فكرة أن التخلص من السكان الضارين أمر حاسم.
تأثيرات عبر الأيض والجهاز المناعي
لم يقتصر تغيير الميكروبات المزعجة على تعديل خريطة الأمعاء فحسب — بل غيّر الكيمياء والمناعة في الجسم بأكمله. أظهر المرضى الذين فقدوا المزيد من بكتيريا الأساس أنماطاً مختلفة من المستقلبات الدموية، خصوصاً مركبات مشتقة من الحمض الأميني التربتوفان. كان لدى غير المستجيبين وأولئك الذين احتفظوا بالمزيد من ميكروباتهم الأصلية مستويات أعلى من مستقلبات مثل حمض الكينولينيك والكينورينين، والتي رُبطت بقمع المناعة وردود فعل ضعيفة على العلاج المناعي للسرطان. في الوقت نفسه، عرض المرضى الذين عانوا فقداناً ميكروبياً أكبر خلايا CD8 قاتلة للسرطان أكثر نشاطاً وخلايا T تنظيمية أقل، التي تعمل عادة كفرامل للاستجابات المناعية. معاً، تشير هذه التغيرات إلى بيئة أكثر عدائية للأورام وأكثر ملاءمة لخلايا المناعة المقاومة للسرطان.
ما الذي يعنيه هذا لرعاية السرطان المستقبلية
لغير المتخصصين، الرسالة المركزية هي أن الميكروبات التي تقطن أمعاء المريض يمكن أن تساعد أو تعيق الأدوية المناعية المتطورة. تُظهر هذه الدراسة المرحلية الثانية أن جرعة واحدة من زرع ميكروبيوتا من متبرعين صحيين مفحوصين بعناية يمكن أن تزيد بأمان من معدلات نجاح العلاج المناعي لسرطان الرئة والميلانوما، مع التأكيد على حاجة اختيار المتبرعين بدقة لتجنب تعزيز آثار جانبية خطيرة. والأهم أن الفوائد تبدو ناتجة أقل عن «إضافة كائنات جيدة» وأكثر عن «طرد الكائنات الضارة». يوفر هذا الفهم خارطة طريق لتصميم علاجات قائمة على الميكروبيوم من الجيل القادم — سواء كانت زرعاً كاملاً أو مجموعات ميكروبية مصقولة — تهدف إلى إزالة الأنواع الضارة بشكل انتقائي، وإعادة توازن الأيض، ومنح الجهاز المناعي فرصة أوضح للقضاء على السرطان.
الاستشهاد: Duttagupta, S., Messaoudene, M., Hunter, S. et al. Fecal microbiota transplantation plus immunotherapy in non-small cell lung cancer and melanoma: the phase 2 FMT-LUMINate trial. Nat Med 32, 1337–1350 (2026). https://doi.org/10.1038/s41591-025-04186-5
الكلمات المفتاحية: زرع ميكروبيوتا البراز, العلاج المناعي للسرطان, ميكروبيوم الأمعاء, سرطان الرئة غير صغير الخلايا, الميلانوما