Clear Sky Science · fr
Transplantation de microbiote fécal associée au pembrolizumab et à l’axitinib dans le carcinome rénal métastatique : l’essai randomisé de phase 2 TACITO
Pourquoi votre intestin peut compter dans le cancer du rein
Les médecins savent depuis longtemps que l’on peut stimuler notre système immunitaire pour qu’il combatte le cancer, mais ces médicaments puissants ne fonctionnent pas pour tout le monde. Cette étude pose une question surprenante aux implications importantes : modifier les bactéries du microbiote intestinal d’un patient peut‑il améliorer l’efficacité des traitements immunitaires contre le cancer avancé du rein ? En transférant des microbes intestinaux choisis de patients ayant eu des réponses exceptionnelles à l’immunothérapie vers des patients nouvellement diagnostiqués, les chercheurs ont testé si les « bons » microbes pouvaient augmenter les chances d’un contrôle prolongé de la maladie.
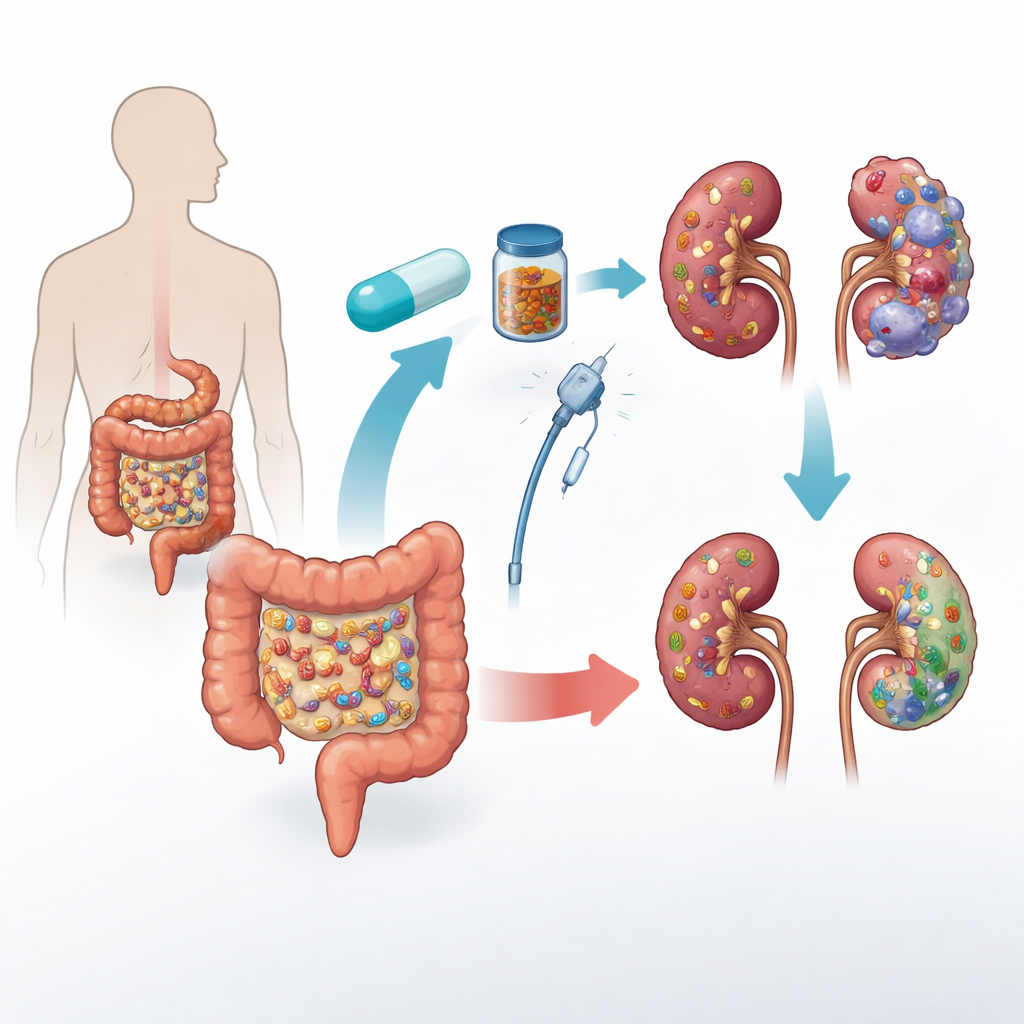
Un nouvel allié pour l’immunothérapie anticancéreuse
L’essai s’est concentré sur le carcinome rénal métastatique, la forme la plus fréquente de cancer rénal avancé. Le traitement standard de première ligne associe souvent deux médicaments : le pembrolizumab, qui aide les cellules immunitaires à reconnaître le cancer, et l’axitinib, qui coupe l’apport sanguin des tumeurs. Même avec ce duo puissant, de nombreux patients voient leur cancer progresser de nouveau en l’espace d’un an et demi. Des indices antérieurs issus d’autres cancers laissaient penser que les personnes dont le microbiote intestinal est plus riche et mieux équilibré répondaient mieux aux immunothérapies. Sur cette base, l’essai TACITO a testé si la transplantation de selles provenant de deux patients atteints de cancer du rein ayant eu des réponses complètes et durables à l’immunothérapie pouvait améliorer les résultats chez des patients récemment traités.
Comment l’essai a été mené
Dans cette étude randomisée et en double aveugle, 45 patients atteints de cancer du rein métastatique non traités ont reçu le traitement standard pembrolizumab plus axitinib. La moitié a été assignée à une transplantation de microbiote fécal de donneur (d‑FMT) et l’autre moitié à des capsules et une solution placebo (p‑FMT). Tous ont subi trois procédures sur six mois : d’abord une perfusion par coloscopie, puis deux prises de capsules congelées. Ni les patients ni les médecins traitants ne savaient qui avait reçu du matériel de donneur réel ou un placebo. L’objectif principal était de mesurer combien de patients restaient sans progression de la maladie un an après la randomisation ; l’équipe a aussi suivi la durée médiane sans progression, la survie globale, le taux de réponses tumorales (réduction des tumeurs) et l’évolution du microbiote intestinal au fil du temps.
Que s’est‑il passé pour les tumeurs et la survie
Bien que l’essai ait manqué de peu son objectif statistique principal à 12 mois, les signaux cliniques étaient frappants. Un an après la randomisation, 70 % des patients du groupe donneur et 41 % du groupe placebo n’avaient pas présenté de progression de la maladie, une différence qui se situe à la marge des seuils statistiques habituels. Sur l’ensemble du suivi, les personnes ayant reçu des microbes donneurs avaient une survie sans progression médiane de 24 mois, contre seulement 9 mois dans le groupe placebo. La part de patients dont les tumeurs ont diminué (réponse partielle ou complète) était également plus élevée avec la FMT donneur : 52 % contre 32 %. La survie globale favorisait aussi le groupe donneur (41 contre 28,3 mois au moment de l’analyse), bien que cette différence ne soit pas encore statistiquement solide, probablement parce que le nombre de décès restait modéré.
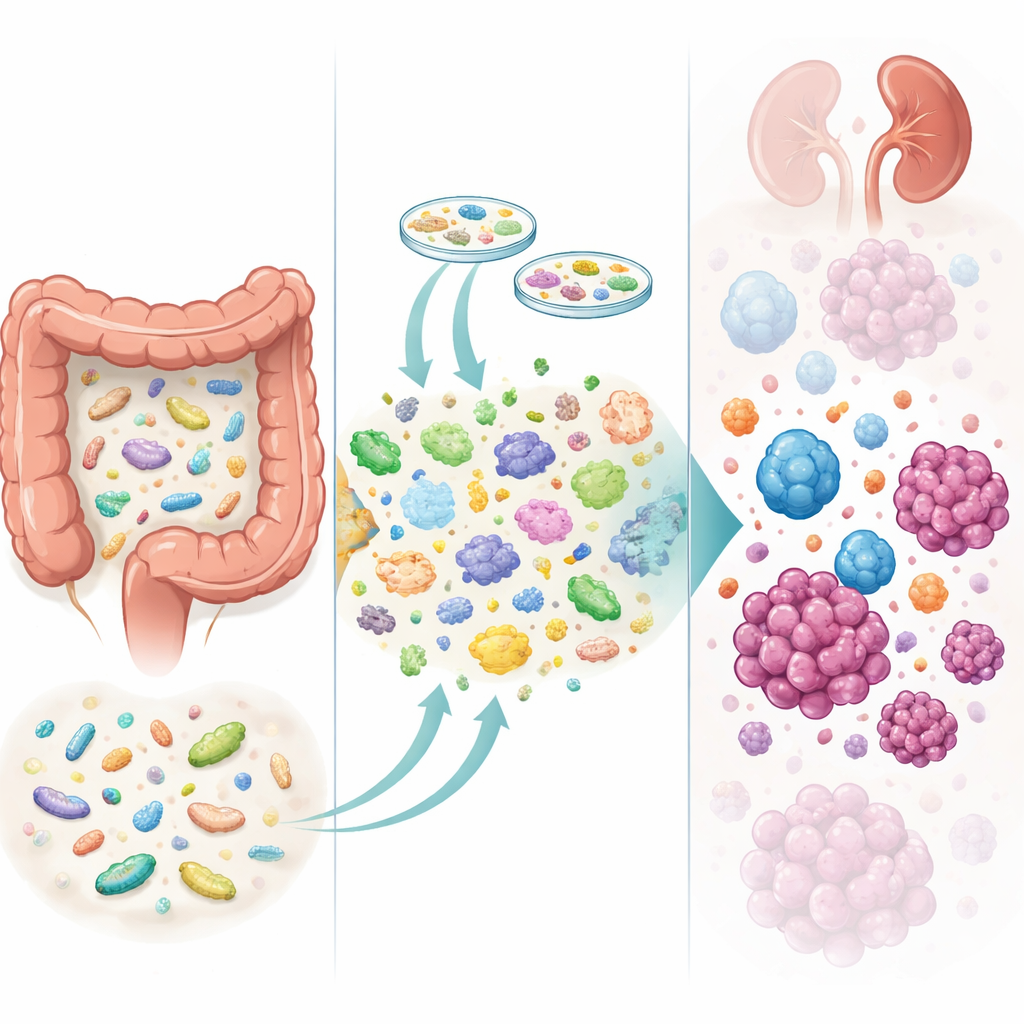
Comment les microbes ont changé
Pour comprendre ce qui se passait dans l’intestin, l’équipe a collecté plus de 240 échantillons de selles avant et après le traitement. Un séquençage à haute profondeur de l’ADN a montré que les patients ayant reçu le matériel donneur ont acquis davantage d’espèces microbiennes et ont eu des modifications plus marquées de la composition de leur microbiote que ceux sous placebo. Autrement dit, la greffe a clairement « pris ». Cependant, disposer simplement de plus de souches donneuses n’a pas garanti de meilleurs résultats. Les détails importaient : l’acquisition de certaines bactéries bénéfiques, comme une souche de Blautia wexlerae qui produit des acides gras à chaîne courte utiles, était liée à un contrôle plus long de la maladie. L’acquisition d’autres souches, y compris un proche récemment décrit du microbe bien connu Akkermansia muciniphila, s’associait à un contrôle plus court. De même, la perte de certains résidents intestinaux initiaux, comme des Escherichia coli inflammatoires, semblait favorable, tandis que la perte d’une espèce dégradant l’amidon nommée Ruminococcus bromii tendait à être un mauvais signe.
Sécurité et qui pourrait le plus en bénéficier
Les procédures ont été généralement bien tolérées. Les effets indésirables directement liés à la transplantation — que ce soit via coloscopie ou capsules — ont été rares et pour la plupart légers, sans décès ni infections détectées liées au matériel de donneur. Les effets secondaires habituels du pembrolizumab et de l’axitinib, comme la diarrhée et des modifications des enzymes hépatiques, sont survenus à des fréquences similaires à celles observées en pratique courante. Lorsque les chercheurs ont regardé spécifiquement les patients présentant un pronostic initial plus défavorable, les avantages de la d‑FMT semblaient encore plus marqués : ces patients ont eu un contrôle de la maladie nettement plus long et des taux de réponse plus élevés s’ils avaient reçu des microbes donneurs plutôt que le placebo. Cela suggère que les stratégies basées sur le microbiome pourraient être particulièrement utiles pour les personnes partant d’une situation plus fragile.
Ce que cela signifie pour les patients
Pour quelqu’un confronté à un cancer du rein avancé, ces résultats suggèrent un avenir où le traitement ne se limite pas aux médicaments, mais implique aussi d’ajuster la communauté microbienne intestinale. Dans cet essai relativement petit, des transplantations de selles soigneusement sélectionnées à partir de « répondeurs exceptionnels » ont paru sûres et ont prolongé le temps avant la progression du cancer, et pourraient à terme améliorer la survie, lorsqu’elles sont ajoutées à l’immunothérapie standard. Les résultats montrent aussi que tous les microbes ne se valent pas : ce sont des gains et pertes bactériens précis, plutôt qu’une augmentation globale des souches donneuses, qui semblent faire la différence. Des essais de plus grande envergure et des formulations microbiennes plus raffinées, sous forme de gélules, seront nécessaires avant que ces approches ne deviennent courantes, mais le message est clair : les microbes de nos intestins pourraient devenir des alliés puissants dans la lutte contre le cancer.
Citation: Porcari, S., Ciccarese, C., Heidrich, V. et al. Fecal microbiota transplantation plus pembrolizumab and axitinib in metastatic renal cell carcinoma: the randomized phase 2 TACITO trial. Nat Med 32, 1316–1324 (2026). https://doi.org/10.1038/s41591-025-04189-2
Mots-clés: microbiome intestinal, transplantation de microbiote fécal, thérapie par inhibiteur de point de contrôle immunitaire, carcinome rénal métastatique, immunothérapie anticancéreuse