Clear Sky Science · ar
زرع الميكروبيوم البرازي مع بيمبروليزوماب وأكسيتينيب في سرطان الكلى النقيلي: تجربة تاسيتو العشوائية من المرحلة الثانية
لماذا قد تهم أمعاؤك في سرطان الكلى
لطالما عرف الأطباء أن بإمكان جهازنا المناعي أن يُستثار لمهاجمة السرطان، لكن هذه الأدوية الفعّالة لا تناسب جميع المرضى. تطرح هذه الدراسة سؤالاً مفاجئاً له تبعات كبيرة: هل يمكن لتغيير البكتيريا التي تعيش في أمعاء المريض أن يجعل أدوية الرعاية المناعية المضادة للسرطان تعمل بصورة أفضل في سرطان الكلى المتقدم؟ عن طريق نقل ميكروبات معوية مختارة من مرضى استجابوا بشكل استثنائي للعلاج المناعي إلى مرضى تم تشخيصهم حديثاً، اختبر الباحثون ما إذا كانت الميكروبات "الصحيحة" قد تُحسّن فرص السيطرة الطويلة على المرض.
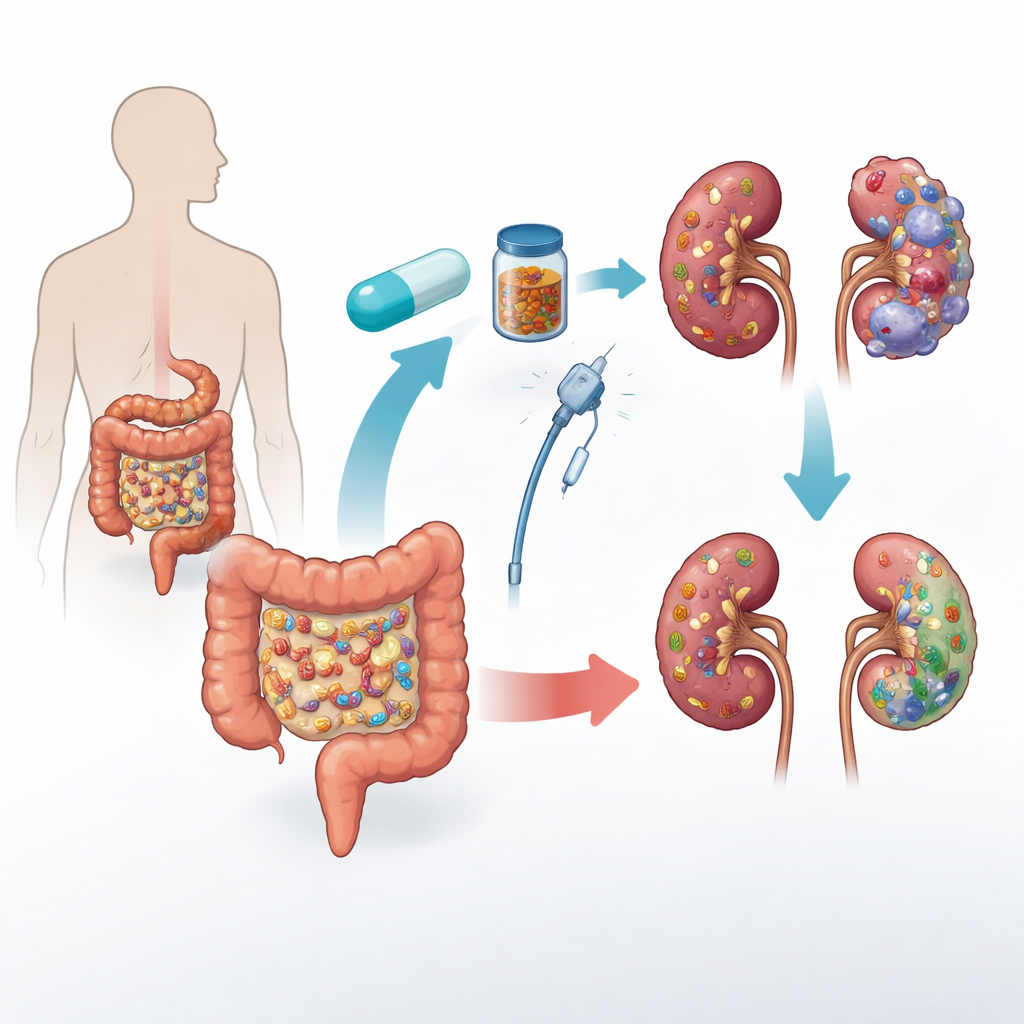
شريك جديد لعلاج المناعة ضد السرطان
ركزت التجربة على سرطان الكلى النقيلي، الشكل الأكثر شيوعاً من سرطان الكلى المتقدم. يتكوّن العلاج القياسي من خط العلاج الأول في كثير من الأحيان من دوائين معاً: بيمبروليزوماب، الذي يساعد خلايا المناعة على التعرف إلى السرطان، وأكسيتينيب، الذي يعيق إمداد الدم للأورام. وحتى مع هذا الثنائي القوي، يعاود الكثير من المرضى نمو السرطان خلال عام ونصف تقريباً. أشارت شواهد سابقة من سرطانات أخرى إلى أن الأشخاص الذين كانت ميكروبات أمعائهم أكثر غنى وتوازناً أميلوا للاستجابة بشكل أفضل للعلاجات المناعية. واستناداً إلى ذلك، اختبرت تجربة تاسيتو ما إذا كان زرع براز من اثنين من مرضى سرطان الكلى الذين حققوا استجابات كاملة وطويلة الأمد للعلاج المناعي يمكن أن يُحسّن النتائج لدى المرضى الذين بدأوا العلاج للتو.
كيف أُجريت التجربة
في هذه الدراسة العشوائية المزدوجة التعمية، تلقى 45 مريضاً مصاباً بسرطان الكلى النقيلي غير المعالج سابقاً بيمبروليزوماب وأكسيتينيب القياسيين. تم تخصيص نصفهم لزرع ميكروبيوتا برازية من متبرع (d-FMT) والنصف الآخر لكبسولات ومحلول وهمي (p-FMT). خضع الجميع لثلاث إجراءات على مدى ستة أشهر: أولاً حقن عبر تنظير القولون، ثم جولتان من الكبسولات المجمدة. لم يعرف لا المرضى ولا الأطباء المعالجون من تلقى المادة المتبرع بها الحقيقية ومن تلقى الدواء الوهمي. الهدف الرئيسي كان معرفة كم من المرضى ظلوا خالين من تدهور السرطان بعد عام من التوزيع العشوائي؛ كما تتبع الفريق مدة البقاء دون تقدم المرض الإجمالية، ومدة الحياة، ومعدلات انكماش الأورام، وكيف تغيّرت ميكروبات الأمعاء مع الوقت.
ماذا حدث للأورام والبقاء على قيد الحياة
على الرغم من أن التجربة أخفقت قليلاً في تحقيق الهدف الإحصائي الرئيسي عند 12 شهراً، فإن الإشارات السريرية كانت لافتة. بعد عام من التوزيع العشوائي، لم يشهد 70٪ من المرضى في مجموعة المتبرعين تطور المرض مقارنةً بـ41٪ في مجموعة الدواء الوهمي، وهو فرق كان حديّاً حسب قواعد الإحصاء المعتادة. وعند النظر خلال كامل فترة المتابعة، بلغ الوسيط الزمني للبقاء دون تقدم المرض لدى من تلقوا ميكروبات المتبرعين 24 شهراً، مقابل 9 أشهر فقط في مجموعة الدواء الوهمي. كما كانت نسبة الأشخاص الذين تراجعت أورامهم (استجابة جزئية أو كاملة) أعلى مع زرع المتبرع: 52٪ مقابل 32٪. ومالت معدلات البقاء الكلي أيضاً لصالح مجموعة المتبرع (41 مقابل 28.3 شهراً وقت التحليل)، وإن لم يكن هذا الفرق قد أصبح ثابتاً إحصائياً بعد، وربما يعود ذلك إلى أن عدد الوفيات لا يزال محدوداً.
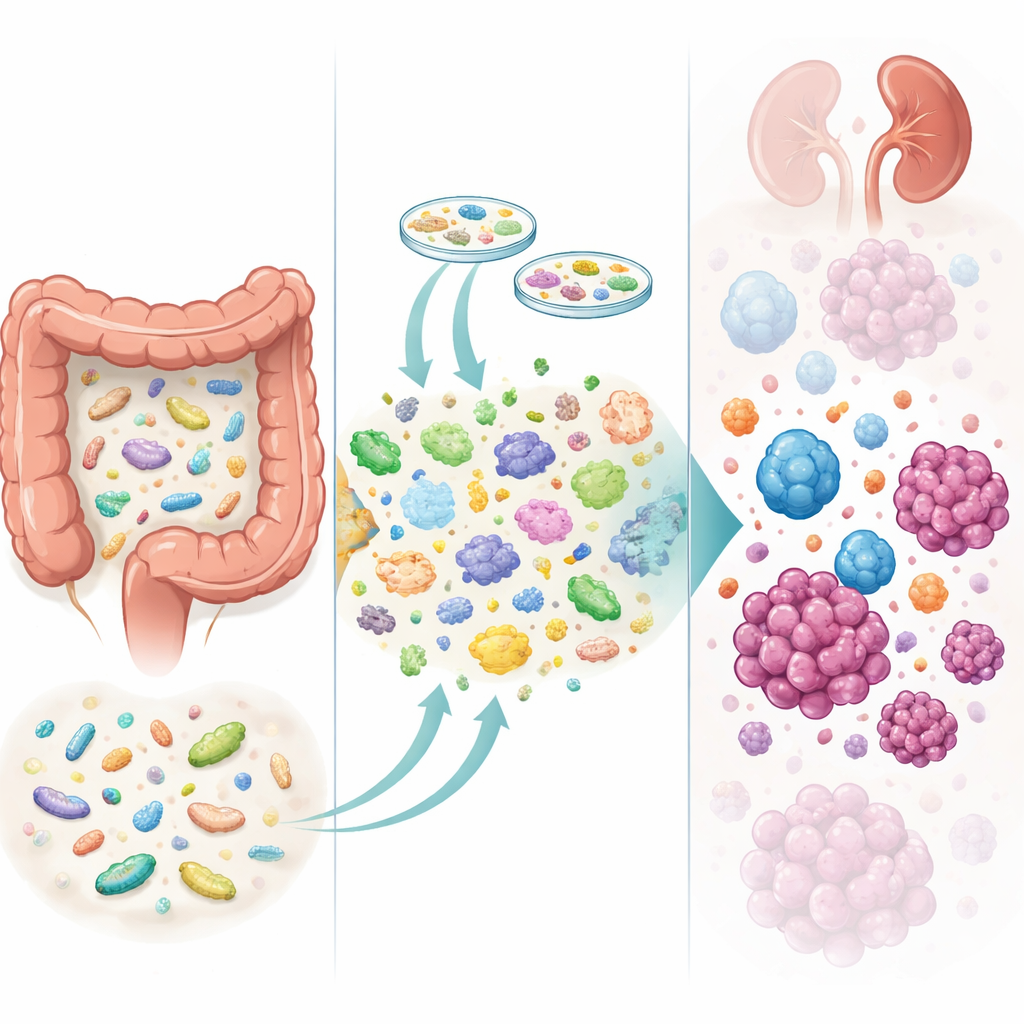
كيف تغيّرت الميكروبات
لفهم ما كان يحدث داخل الأمعاء، جمع الفريق أكثر من 240 عينة براز قبل وبعد العلاج. أظهر تسلسل الحمض النووي بعمق عالٍ أن المرضى الذين تلقوا مادة المتبرع اكتسبوا عددًا أكبر من الأنواع الميكروبية وحدثت لديهم تحولات أكبر في تركيب أمعائهم مقارنةً بمن تلقوا الدواء الوهمي. بعبارة أخرى، كان للزرع أثر واضح على تكوين الميكروبيوم. ومع ذلك، لم تكن مجرد زيادة عدد سلالات المتبرع ضماناً لنتائج أفضل. بل كانت التفاصيل هي الحاسمة: ارتبط اكتساب بكتيريا مفيدة معينة، مثل سلالة من Blautia wexlerae التي تنتج أحماضاً دهنية قصيرة السلسلة المفيدة، بسيطرة أطول على المرض. أما اكتساب سلالات أخرى، بما في ذلك قريبة حديثة الوصف من الميكروب المعروف Akkermansia muciniphila، فارتبط بتقصير مدة السيطرة. وبالمثل، بدا أن فقدان بعض القاطنين الأصليين في الأمعاء، مثل الإشريكية القولونية الالتهابية (Escherichia coli)، كان أمراً مفيداً، في حين أن خسارة نوع يكسر النشا يُدعى Ruminococcus bromii كانت تميل لأن تكون علامة سيئة.
السلامة ومن قد يستفيد أكثر
كانت الإجراءات مقبولة عموماً من ناحية التحمل. كانت الآثار الجانبية المرتبطة مباشرة بالزرع — سواء عبر تنظير القولون أو الكبسولات — نادرة ومعظمها خفيف، ولم تُسجّل وفيات أو عدوى ناتجة عن مادة المتبرع. ووقعت الآثار الجانبية المعتادة للبيمبروليزوماب والأكسيتينيب، مثل الإسهال وتغيرات إنزيمات الكبد، بمعدلات مماثلة لما يُرى في الممارسة القياسية. وعندما نظر الباحثون خصيصاً إلى المرضى الذين كانت لديهم توقعات أولية أسوأ، بدا أن فوائد زرع المتبرع كانت أكبر: إذ حقق هؤلاء المرضى سيطرة أطول بكثير على المرض ومعدلات استجابة أعلى إذا تلقوا ميكروبات المتبرع بدلاً من الدواء الوهمي. وهذا يوحي بأن استراتيجيات قائمة على الميكروبيوم قد تكون مفيدة بشكل خاص للأشخاص ذوي الوضع الأضعف في البداية.
ماذا يعني هذا للمرضى
بالنسبة لشخص يواجه سرطان كلى متقدم، تلمّح هذه النتائج إلى مستقبل قد لا يقتصر العلاج فيه على الأدوية فقط، بل يشمل أيضاً ضبط المجتمع الميكروبي في الأمعاء. في هذه التجربة الصغيرة نسبياً، بدا أن زرعات البراز المفحوصة بعناية من مستجيبين استثنائيين آمنة وأطالت الوقت حتى تدهور السرطان، وقد تحسّن البقاء على المدى البعيد عند إضافتها إلى العلاج المناعي القياسي. وتُظهر النتائج أيضاً أن ليست كل الميكروبات متساوية — فالاكتسابات والخسائر البكتيرية المحددة تبدو أكثر أهمية من مجرد زيادة عامة في سلالات المتبرع. ستحتاج هذه المقاربات إلى تجارب أكبر وخلائط ميكروبية مصفوفة بدقة على شكل حبوب قبل أن تصبح روتينية، لكن الرسالة واضحة: قد تصبح الميكروبات في أمعائنا حلفاء أقوياء في مكافحة السرطان.
الاستشهاد: Porcari, S., Ciccarese, C., Heidrich, V. et al. Fecal microbiota transplantation plus pembrolizumab and axitinib in metastatic renal cell carcinoma: the randomized phase 2 TACITO trial. Nat Med 32, 1316–1324 (2026). https://doi.org/10.1038/s41591-025-04189-2
الكلمات المفتاحية: ميكروبيوم الأمعاء, زرع ميكروبيوتا برازية, علاج نقاط تفتيش المناعة, سرطان الكلى النقيلي, مناعة السرطان