Clear Sky Science · fr
STRATEGIC-1 : essai de phase III randomisé, ouvert, multicentrique GERCOR-PRODIGE-39 à lignes multiples chez des patients atteints de cancer colorectal métastatique inopérable RAS/BRAF sauvages
Pourquoi l’ordre des traitements compte
Pour les personnes vivant avec un cancer colorectal avancé (du côlon ou du rectum) qui s’est propagé et ne peut pas être retiré chirurgicalement, la médecine a beaucoup progressé : les médecins disposent aujourd’hui de plusieurs combinaisons médicamenteuses puissantes pour ralentir la maladie. Mais une grande question reste en grande partie sans réponse : l’ordre d’administration de ces médicaments a‑t‑il vraiment une influence sur la durée de contrôle de la maladie et la survie des patients ? L’essai STRATEGIC‑1 a été conçu pour tester, de manière rigoureuse, si commencer par une combinaison moderne plutôt qu’une autre conduisait à des résultats à long terme clairement supérieurs.
Deux stratégies différentes
Dans cette large étude internationale, les chercheurs se sont concentrés sur un groupe de patients dont les tumeurs ne présentaient pas certaines altérations génétiques courantes (dans les gènes RAS et BRAF). Ces patients bénéficient d’un groupe de médicaments qui bloquent un signal de surface des cellules cancéreuses (EGFR), ainsi que de traitements qui privent les tumeurs de nouveaux vaisseaux sanguins (thérapie anti‑angiogénique). L’essai a comparé deux « plans de jeu » complets, pas seulement des médicaments isolés. Un plan (bras A) commençait par une base chimiothérapeutique appelée FOLFIRI associée à un anticorps bloquant l’EGFR, puis passait à une autre chimiothérapie (FOLFOX) couplée à un bloqueur des vaisseaux sanguins (bévacizumab). L’autre plan (bras B) débutait par une chimiothérapie à base d’oxaliplatine et du bévacizumab, puis basculait vers une chimiothérapie à base d’irinotécan toujours associée au bévacizumab, en réservant la thérapie anti‑EGFR pour plus tard. 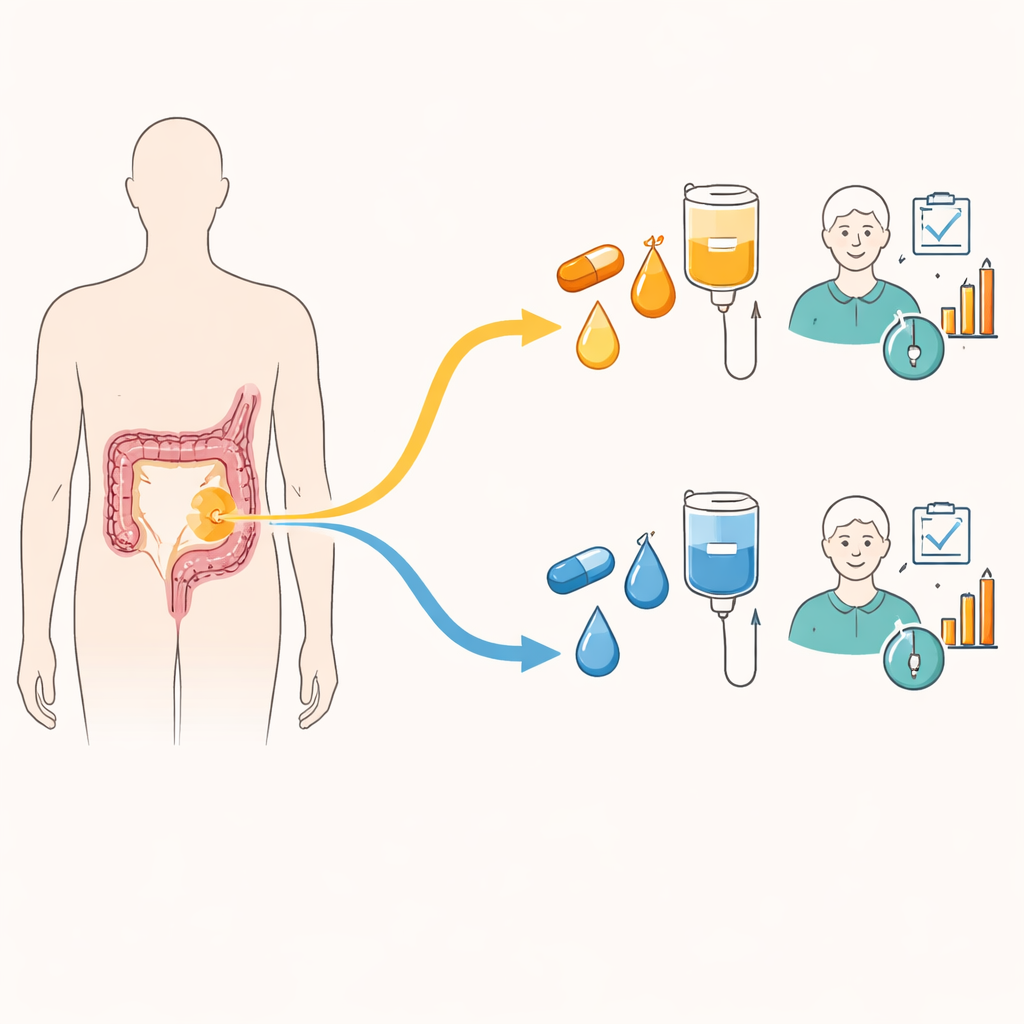
Mesurer le contrôle dans le temps
Plutôt que de ne considérer que la première phase de traitement, l’équipe a utilisé un étalon plus large appelé « durée du contrôle de la maladie ». Celui‑ci additionne, sur plusieurs lignes thérapeutiques, la durée pendant laquelle la maladie de chaque patient est restée maîtrisée avant une progression nette. Ils ont également suivi la survie globale (la durée de vie des patients), le taux de régression tumorale, la possibilité de réaliser des interventions chirurgicales pour retirer des foyers tumoraux, les effets indésirables et la qualité de vie. Plus de 260 personnes atteintes d’un cancer colorectal métastatique inopérable et non traitées antérieurement ont été incluses dans l’étude et ont reçu l’une des deux stratégies, puis ont été suivies en moyenne pendant plus de cinq ans.
Résultats à long terme similaires
Le résultat principal est que le temps global pendant lequel la maladie est restée contrôlée était presque identique entre les deux plans : environ 23 mois dans chaque groupe. La survie globale était également globalement comparable : autour de 40 mois pour ceux ayant commencé par la stratégie basée sur l’EGFR et environ 34 mois pour ceux ayant débuté par le bévacizumab, une différence qui n’a pas atteint le seuil de certitude statistique fixé par l’étude. Les effets indésirables dans les deux groupes correspondaient à ce que les médecins connaissent déjà pour ces traitements, et les problèmes graves liés au traitement survenaient à des fréquences similaires. De façon importante, retarder le début de l’un ou l’autre type de traitement ciblé (inhibiteur de l’EGFR dans un bras, bévacizumab dans l’autre) n’a pas modifié de façon significative la survie ni la durée pendant laquelle la maladie était maintenue sous contrôle.
Réponses précoces et localisation tumorale
Où les deux stratégies différaient, c’était la fréquence de rétrécissement des tumeurs avec le traitement de première ligne. Lorsque les patients commençaient par le schéma incluant l’inhibiteur de l’EGFR, plus de huit patients sur dix présentaient une réduction tumorale mesurable, contre environ deux‑tiers dans le groupe ayant reçu le bévacizumab en premier. Ce schéma était encore plus marqué chez les personnes dont la tumeur primitive se situait sur le côté gauche du côlon ou du rectum, un sous‑groupe déjà connu pour mieux répondre aux inhibiteurs de l’EGFR. Cependant, ces différences précoces de réduction tumorale ne se sont pas traduites par une durée de contrôle ou une survie nettement plus longues sur l’ensemble du groupe. Lorsque les patients sont passés aux traitements de deuxième et troisième lignes, les résultats sont de nouveau apparus globalement similaires entre les deux stratégies. 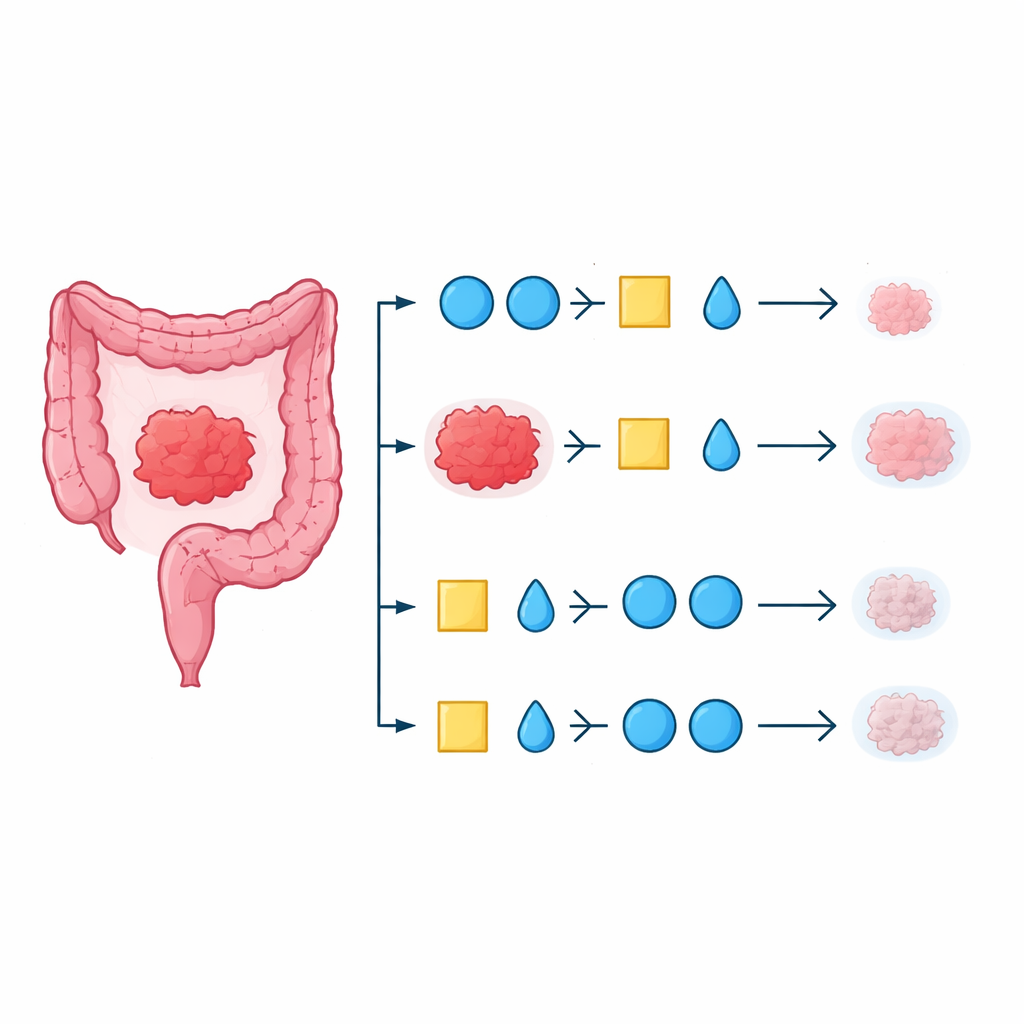
Ce que cela signifie pour les patients
Pour les patients et les cliniciens, STRATEGIC‑1 apporte à la fois des éléments rassurants et des nuances. Il montre que, dans le cadre des standards de soins actuels, il n’existe pas une séquence « miracle » unique entre ces deux grandes familles de médicaments qui modifie de façon spectaculaire la durée de vie de la plupart des patients atteints de ce type de cancer colorectal métastatique. Commencer par un schéma incluant un inhibiteur de l’EGFR peut offrir une probabilité plus élevée de réduction tumorale précoce — utile lorsque l’on recherche une diminution rapide — mais le parcours global, en termes de durée totale de contrôle de la maladie et de survie globale, reste remarquablement similaire entre les stratégies comparées. L’étude souligne aussi que les mesures globales du contrôle à long terme ne constituent peut‑être pas le seul guide pour choisir l’ordre des traitements. Les décisions seront probablement adaptées au cas par cas, en tenant compte du côté tumoral, des caractéristiques moléculaires, des objectifs et de la tolérance du patient, tandis que la recherche future cherchera des moyens plus précis d’assortir la bonne séquence au bon patient.
Citation: Chibaudel, B., Dourthe, LM., André, T. et al. STRATEGIC-1: multiple-line, randomized, open-label GERCOR-PRODIGE-39 phase III trial in unresectable RAS/BRAF wild-type metastatic colorectal cancer. Sig Transduct Target Ther 11, 133 (2026). https://doi.org/10.1038/s41392-026-02639-y
Mots-clés: cancer colorectal métastatique, séquençage des thérapies ciblées, inhibiteurs de l’EGFR, bévacizumab, essais de stratégie de traitement