Clear Sky Science · de
Hybrid-Stacking-Ensemble-Lernen zur genauen Diagnose von Lungenembolie mit tabellarischen klinischen Daten
Warum das für die Patientenversorgung wichtig ist
Eine Lungenembolie ist ein Blutgerinnsel in der Lunge, das innerhalb von Minuten tödlich sein kann, wenn es übersehen wird. Ärztinnen und Ärzte sind stark auf komplexe Bildgebung und ihre eigene Beurteilung angewiesen, um es rechtzeitig zu erkennen. Diese Studie untersucht, wie intelligente Computersysteme routinemäßige klinische Informationen — statt nur Bilder — nutzen können, um Patienten zu markieren, die möglicherweise ein verborgenes Gerinnsel haben, und so in überfüllten Kliniken schnellere und verlässlichere Entscheidungen zu unterstützen.
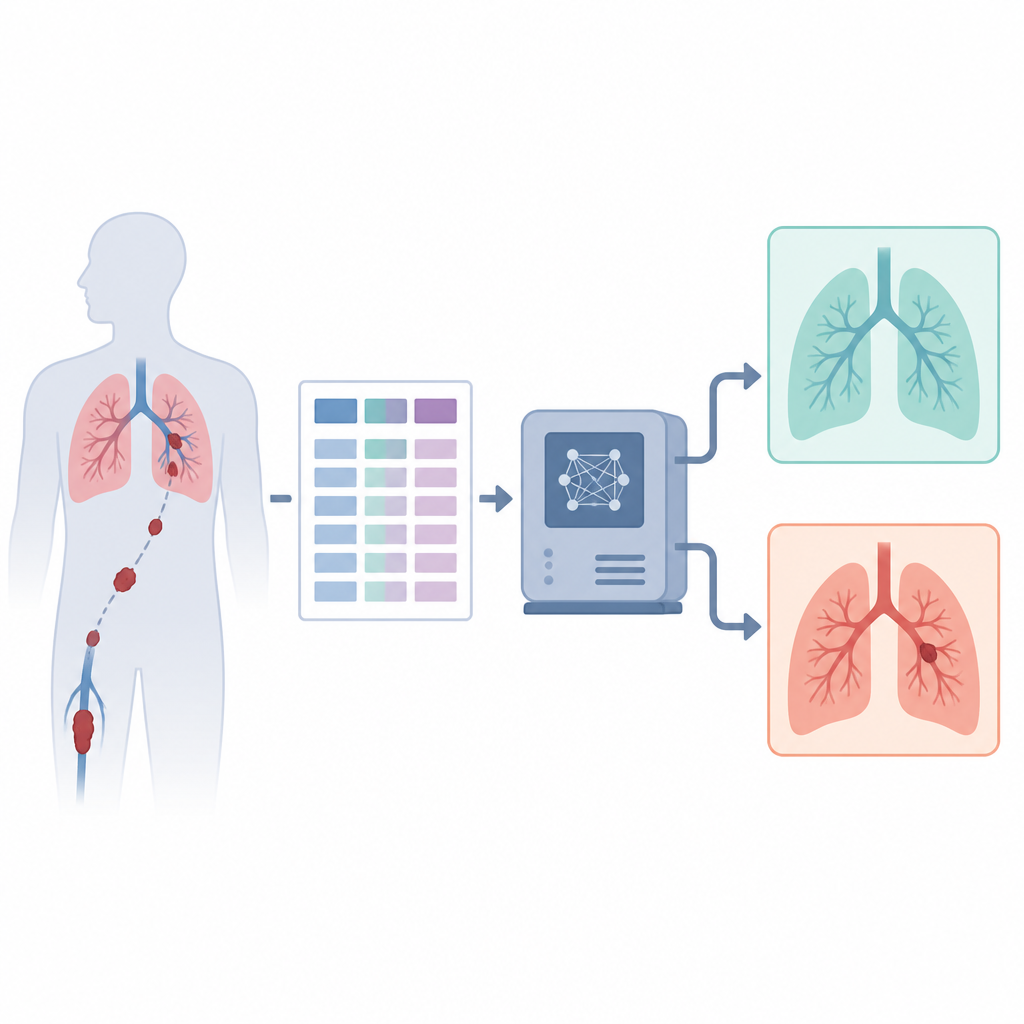
Die Gefahr verborgener Lungenembolien
Lungenembolie ist nach Herzinfarkt und Schlaganfall eine der häufigsten lebensbedrohlichen Herz‑ und Lungennotfälle. Gerinnsel, die in die Lunge gelangen, können plötzlich den Blutfluss blockieren, die rechte Herzhälfte belasten und den Körper mit Sauerstoff unterversorgen. Viele Patientinnen und Patienten sterben, bevor jemand erkennt, was vor sich geht. Wird der Zustand jedoch schnell erkannt und behandelt, steigt die Überlebenschance dramatisch. Diese Lücke zwischen stiller Gefahr und lebensrettendem Handeln treibt die Suche nach Werkzeugen an, die Ärztinnen und Ärzten helfen, schneller die richtige Diagnose zu stellen.
Beschränkungen aktueller Tests und Scores
Heute ist der Haupttest für Lungenembolie eine spezielle CT-Aufnahme des Brustkorbs. Obwohl diese Untersuchungen leistungsfähig sind, benötigen sie teure Geräte, Experten zur Auswertung und Zeit. Standardisierte klinische Scores und einzelne Machine‑Learning‑Modelle, die auf Basisdaten der Patientinnen und Patienten arbeiten, haben zwar geholfen, verpassen aber oft subtile Muster in großen, heterogenen klinischen Datensätzen. Da Krankenhäuser immer mehr digitale Aufzeichnungen sammeln, wächst der Bedarf an intelligenteren Systemen, die aus vielen unterschiedlichen klinischen Hinweisen gleichzeitig lernen und für Klinikpersonal dennoch verlässlich und nachvollziehbar bleiben.
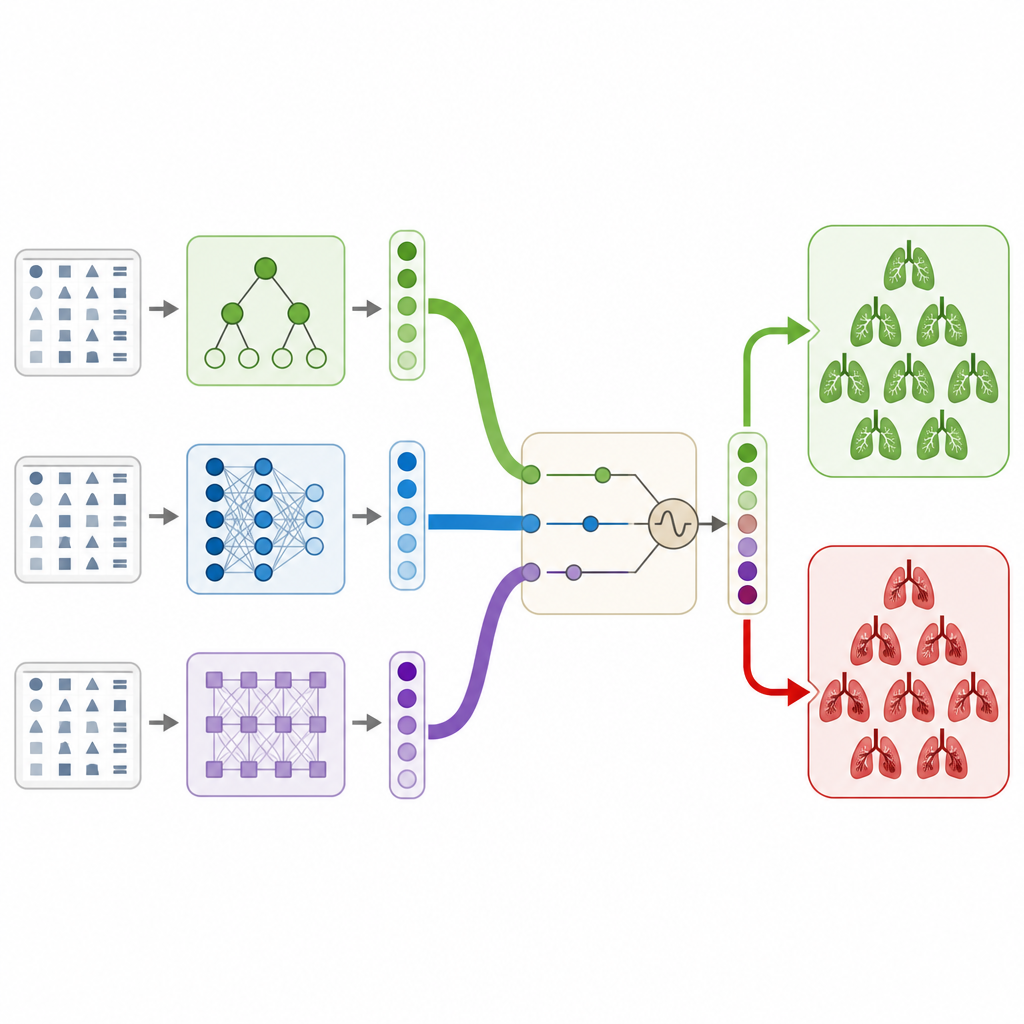
Ein Team aus Modellen arbeitet zusammen
Die Autoren gehen dieses Problem an, indem sie nur die strukturierten klinischen Informationen aus einem großen öffentlichen CT‑Datensatz verwenden, ohne die Bilder selbst auszuwerten. Sie bauen ein hybrides Stacking‑Ensemble auf, das man sich am besten als Gremium verschiedener Computermodelle vorstellen kann, die gemeinsam darüber abstimmen, ob bei einem Patienten ein Gerinnsel vorliegt. Das Gremium umfasst zwei baumbasierte Modelle, ein klassisches neuronales Netz und ein modernes Transformer‑Modell, das für tabellarische Daten entwickelt wurde. Jedes Modell liefert eine Wahrscheinlichkeit für das Vorliegen eines Gerinnsels, und ein abschließendes einfaches Modell lernt, wie diese Einschätzungen so zu einer Entscheidung kombiniert werden können, dass Overfitting vermieden und das Verhalten stabil gehalten wird.
Die Natur als Leitfaden für die Abstimmung
Um das Beste aus diesem Gremium herauszuholen, verwenden die Forschenden eine naturinspirierte Suchmethode namens Marine Predators Algorithm. Diese Methode erkundet viele Kombinationen interner Einstellungen für jedes Modell und zahlreiche Möglichkeiten, ihre Ausgaben zu gewichten — ähnlich virtuellen Jägern, die ein großes Meer nach den besten Fanggründen absuchen. Mithilfe von Kreuzvalidierung, um Zufallsergebnisse auszuschließen, findet der Algorithmus eine Konfiguration, die verbessert, wie gut das Gesamtsystem Patienten mit und ohne Gerinnsel trennt, verglichen mit den Einzelmodellen oder einfacheren Abstimmungsschemata.
Wie gut das System arbeitet und was es lernt
Im öffentlichen RSNA‑Lungenembolie‑Datensatz erreicht das kombinierte System eine Gesamtgenauigkeit von etwa 92 Prozent und zeigt eine starke Trennschärfe zwischen positiven und negativen Fällen. Damit übertrifft es alle Einzelmodelle und mehrere Standardmethoden der Kombination. Die Autorinnen und Autoren nutzen anschließend Erklärungswerkzeuge, um zu sehen, welche klinischen Felder die Vorhersagen am stärksten beeinflussen. Merkmale, die direkt das Vorhandensein und die Seite des Gerinnsels beschreiben, sowie Messgrößen für die Belastung der rechten Herzhälfte haben den größten Einfluss, während technische Bildqualitätskennzeichen nur wenig bewirken. Dieses Muster stimmt mit medizinischem Wissen überein und legt nahe, dass das Modell sich auf klinisch sinnvolle Signale statt auf Rauschen konzentriert.
Was das für künftige Diagnosen bedeutet
Kurz gesagt zeigt diese Arbeit, dass ein sorgfältig abgestimmtes Team vielfältiger Computermodelle gewöhnliche klinische Daten nutzen kann, um Lungenembolien genauer zu erkennen als einzelne Verfahren. Obwohl das System noch außerhalb des hier verwendeten Datensatzes getestet werden muss und weder Bildgebung noch Ärztinnen und Ärzte ersetzt, bietet es einen praktischen Weg zu Unterstützungswerkzeugen, die Hochrisikopatienten früher hervorheben, Fehldiagnosen verringern und vorhandene Klinikdaten in der realen Versorgung besser nutzbar machen.
Zitation: Abdelhamid, A., Moustafa, H.ED., Nafea, H.B. et al. Harnessing hybrid stacking ensemble learning for accurate pulmonary embolism diagnosis using tabular clinical data. Sci Rep 16, 15051 (2026). https://doi.org/10.1038/s41598-026-49331-3
Schlüsselwörter: Lungenembolie, klinische Daten, Ensemble-Lernen, Machine Learning, medizinische Diagnose