Clear Sky Science · de
Immunmodulierende Impfstoffe, die Antigene des Tumormikromilieus anvisieren: jüngste Fortschritte in der Onkologie und darüber hinaus
Die körpereigenen Bremsen in Krebsziele verwandeln
Krebs überlebt oft nicht, weil unser Immunsystem schwach wäre, sondern weil Tumoren lernen, sich hinter den körpereigenen „Bremsen“ zu verstecken, die normalerweise schädliche Entzündungen verhindern. Dieser Artikel beleuchtet eine neue Behandlungsform, immunmodulierende Impfstoffe (IMVs), die das Immunsystem darauf trainieren, diese Bremsen selbst zu erkennen und anzugreifen. Für Leserinnen und Leser bietet er einen Einblick, wie Impfstoffe künftig nicht nur Infektionen verhindern, sondern auch das innere Umfeld des Körpers umgestalten könnten, damit es Krebs und möglicherweise hartnäckige Infektionen besser bekämpfen kann.
Wie Tumoren eine schützende Nachbarschaft aufbauen
Statt als isolierte Knoten zu wachsen, leben Tumoren in einer komplexen Nachbarschaft aus Stütz- und Immunzellen sowie Blutgefäßen – dem Tumormikromilieu. Viele dieser umgebenden Zellen sind „Regulatoren“, deren normale Aufgabe es ist, das Immunsystem nach einer Infektion zu beruhigen und Autoimmunität zu verhindern. Im Krebsfall werden sie jedoch gekapert. Spezialisierte Immunzellen, narbenbildende Bindegewebszellen und Gefäßzellen beginnen Moleküle freizusetzen, die Immunzellen Nährstoffe vorenthalten, ihnen Signale zum Ruhemodus geben oder ihren Eintritt in den Tumor blockieren. Zusammen formen sie einen mehrschichtigen Schutzschild, der viele Krebsarten selbst gegen moderne Medikamente, die Immunbremsen lösen – wie PD‑1‑Checkpoint‑Inhibitoren – resistent macht. 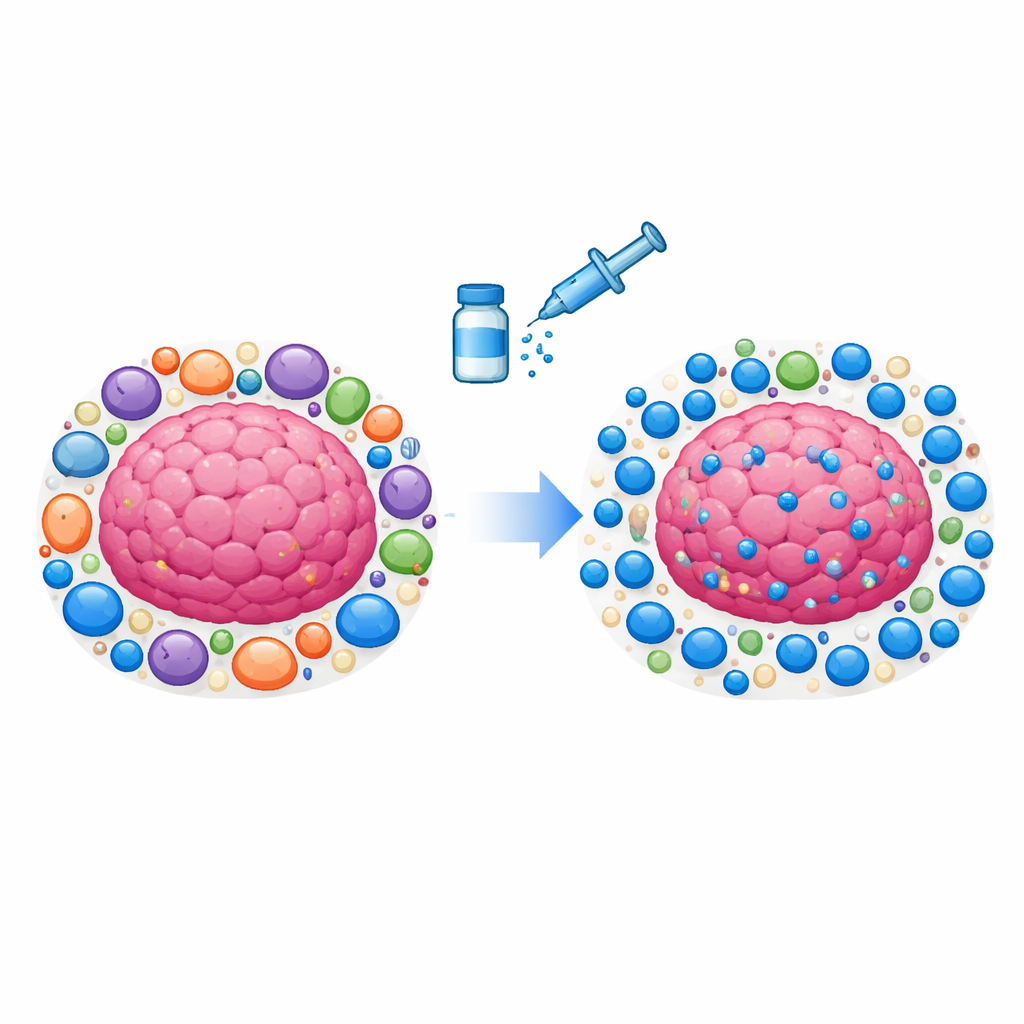
Anti-Regulatorische T-Zellen: Die inneren Wachhunde des Immunsystems
Das Review hebt eine unerwartete Entdeckung hervor: In unserem Körper gibt es von Natur aus kleine Mengen an T‑Zellen, die speziell jene unterdrückenden Moleküle und die Zellen, die sie produzieren, erkennen. Diese „anti‑regulatorischen T‑Zellen“ oder anti‑Tregs sind kein besonderer Zelltyp, sondern gewöhnliche Helfer‑ und Killer‑T‑Zellen, deren Zielproteine zufällig IDO, PD‑L1, Arginase‑1 und TGF‑β sind – Schlüsselakteure bei Immunsuppression und Narbenbildung. Sobald sie aktiviert sind, können anti‑Tregs unterdrückende Zellen direkt töten oder sie durch Freisetzung entzündlicher Botenstoffe umlernen. Effektiv überwachen sie die Regulatoren und verhindern, dass das Immunsystem dauerhaft im „Bremsen‑an“-Zustand verharrt. Wichtig ist, dass solche Zellen selbst bei gesunden Menschen gefunden werden, was darauf hindeutet, dass sie Teil des normalen immunologischen Gleichgewichts und kein Krankheitszeichen sind.
Impfstoffe, die das Schutzschild des Krebses anvisieren, nicht nur die Krebszellen
Traditionelle Krebsimpfstoffe versuchen, T‑Zellen auf Marker der Tumorzellen selbst zu trainieren. IMVs gehen einen anderen Weg: Sie enthalten kurze Proteinfragmente aus den unterdrückenden Molekülen und aus den Stütz-Zellen des Tumormikromilieus – zusammengefasst als Antigene des Tumormikromilieus. Nach der Impfung expandieren anti‑Tregs und suchen jede Zelle auf, die diese Antigene zeigt, sei es eine Krebszelle, eine Immunzelle oder ein Fibroblast, der eine steife, ausschließende Narbe bildet. Killer‑T‑Zellen entfernen diese Zellen direkt, während Helfer‑T‑Zellen das Gebiet mit Signalen fluten, die die Antigenpräsentation verbessern, weitere Effektorzellen anlocken und starre Gewebsbarrieren aufweichen. Diese zweigleisige Wirkung kann einen „kalten“, schlecht infiltrierten Tumor in einen „heißen“, entzündeten Tumor verwandeln, der für andere Immuntherapien deutlich zugänglicher ist. 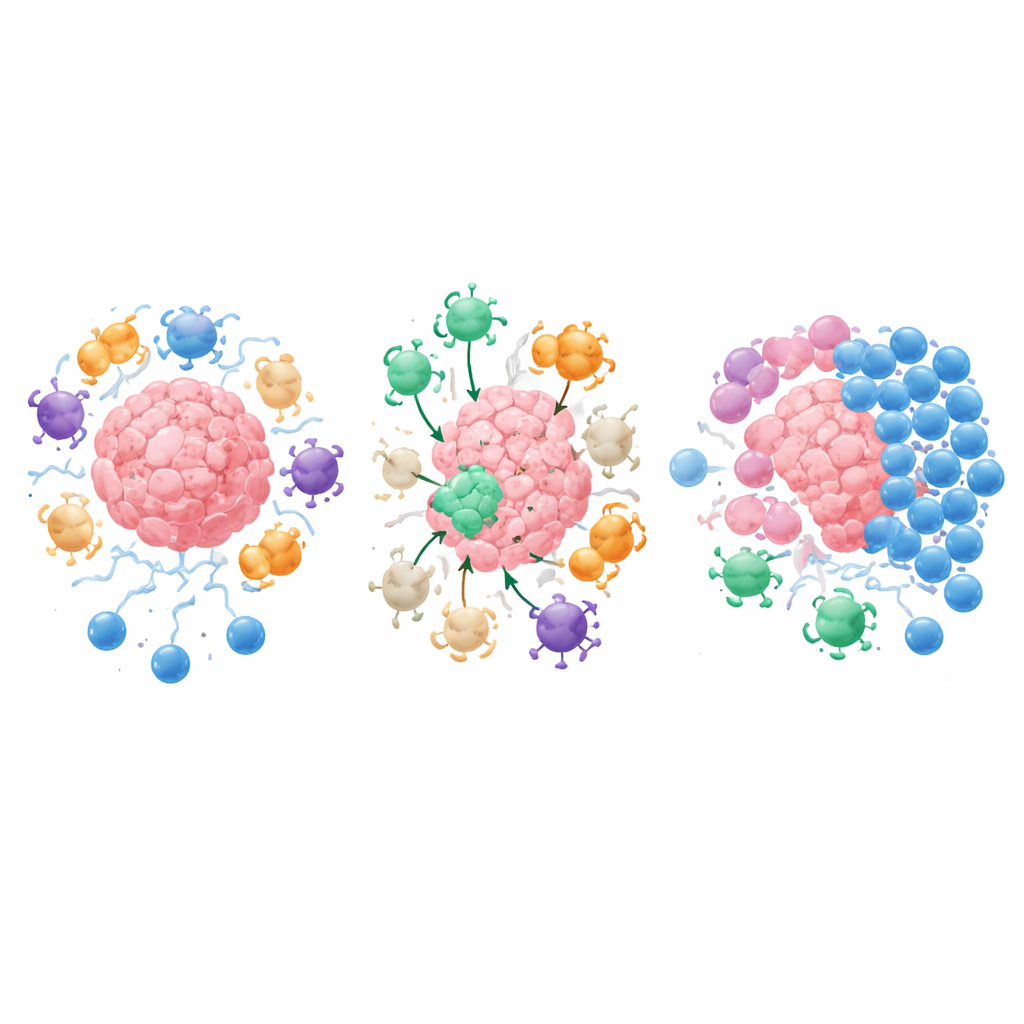
Belege aus Tierstudien und frühen klinischen Studien
In mehreren Mausmodellen verlangsamten Impfstoffe gegen Moleküle wie IDO, PD‑L1, Arginase und TGF‑β das Tumorwachstum, reduzierten immunsuppressive Zellen und erhöhten die Zahl von tumorkillenden T‑Zellen im Tumor. Diese Effekte waren noch stärker in Kombination mit PD‑1‑Checkpoint‑Medikamenten. Frühe Humanstudien spiegeln diese Ergebnisse weitgehend wider: Peptid- und mRNA‑basierte IMVs erwiesen sich als sicher und lösen zuverlässig messbare T‑Zell‑Antworten gegen ihre Zielmoleküle aus, oft begleitet von verringerten Zahlen oder Aktivität suppressiver Zellen in Blut- und Tumorproben. Eine Phase‑II‑Melanomstudie, die einen IDO/PD‑L1‑Impfstoff mit Anti‑PD‑1‑Therapie kombinierte, berichtete über hohe Ansprechraten und langanhaltende Kontrolle; eine größere Phase‑III‑Studie zeigte insgesamt ein längeres progressionsfreies Überleben, mit dem deutlichsten Nutzen bei Patientinnen und Patienten, die PD‑1‑Blockade erstmals erhielten und bei Tumoren, die anfänglich PD‑L1‑negativ waren.
Blick über den Krebs hinaus: Infektionen und mögliche künftige Anwendungen
Die gleichen unterdrückenden Mechanismen, die Tumoren nutzen, treten offenbar auch bei chronischen Infektionen und bei schweren akuten Infektionen älterer oder gebrechlicher Patienten auf. Der Artikel argumentiert, dass das IMV‑Konzept – gegen die überaktiven körpereigenen Bremsen zu impfen – langfristig helfen könnte, persistente Viren zu eliminieren oder die Wirksamkeit von Standardimpfungen bei älteren Menschen zu verbessern, indem lokale Immunumgebungen umgestaltet werden. Gleichzeitig mahnt er zur Vorsicht bei Autoimmunerkrankungen, wo ein zu starkes Herunterfahren der Regulation Selbstangriffe verschlimmern könnte. Insgesamt lautet die Schlussfolgerung, dass IMVs eine neue Ebene der Immuntherapie hinzufügen: Anstatt nur mehr Soldaten auszurüsten, demontieren sie die Festung des Gegners. In Kombination mit bestehenden Medikamenten und einem früheren Einsatz im Krankheitsverlauf könnten sie dem eigenen Immunsystem von mehr Patientinnen und Patienten helfen, dauerhafte Kontrolle über Krebs und andere schwer behandelbare Erkrankungen zu erreichen.
Zitation: Andersen, M.H. Immune modulatory vaccines targeting tumor microenvironment antigens: recent advances in oncology and beyond. Sig Transduct Target Ther 11, 130 (2026). https://doi.org/10.1038/s41392-026-02710-8
Schlüsselwörter: Tumormikroumgebung, Krebsimpfstoffe, Immun-Checkpoint, T-Zell-Therapie, Immuntherapie