Clear Sky Science · ar
لقاحات معدِّلة للمناعة تستهدف مستضدات البيئة المصاحبة للأورام: التقدّم الحديث في علم الأورام وما بعده
تحويل فرامل الجسم إلى أهداف علاجية للسرطان
غالبًا لا ينجو السرطان لأن جهازنا المناعي ضعيف، بل لأن الأورام تتعلّم الاختباء خلف «فرامل» الجسم نفسها التي تهدف عادةً إلى منع الالتهاب الضار. تستعرض هذه المقالة نوعًا جديدًا من العلاجات، لقاحات تعديل المناعة (IMVs)، التي تُعلّم الجهاز المناعي التعرف على تلك الفرامل ومهاجمتها. تقدم للقارئ لمحة عن كيف أن اللقاحات قد تُستخدم قريبًا ليس فقط للوقاية من العدوى، بل أيضًا لإعادة توصيل البيئة الداخلية للجسم بحيث تصبح أفضل في مكافحة السرطان وربما العدوى المستعصية.
كيف تبني الأورام حيًّا واقيًا حولها
بدلًا من النمو ككتل معزولة، تعيش الأورام داخل حي معقّد مكوّن من خلايا داعمة، أوعية دموية، وخلايا مناعية يُطلق عليه البيئة المصاحبة للورم. العديد من هذه الخلايا المحيطة هي «مُنظِّمات» تعمل عادةً على تهدئة الجهاز المناعي بعد العدوى ومنع أمراض المناعة الذاتية. لكن في السرطان تُستغلّ هذه الوظائف لصالح الورم. تبدأ خلايا مناعية متخصّصة، وخلايا مكوِّنة للندبة، وخلايا الأوعية الدموية بإفراز جزيئات تحرم الخلايا المناعية من المغذيات، أو تُشير لها بالتراجع، أو تمنع دخولها إلى الورم. معًا تشكّل درعًا متعدد الطبقات يجعل العديد من السرطانات مقاومة حتى للأدوية الحديثة التي ترفع الفرامل المناعية، مثل مثبطات نقطة التفتيش PD‑1. 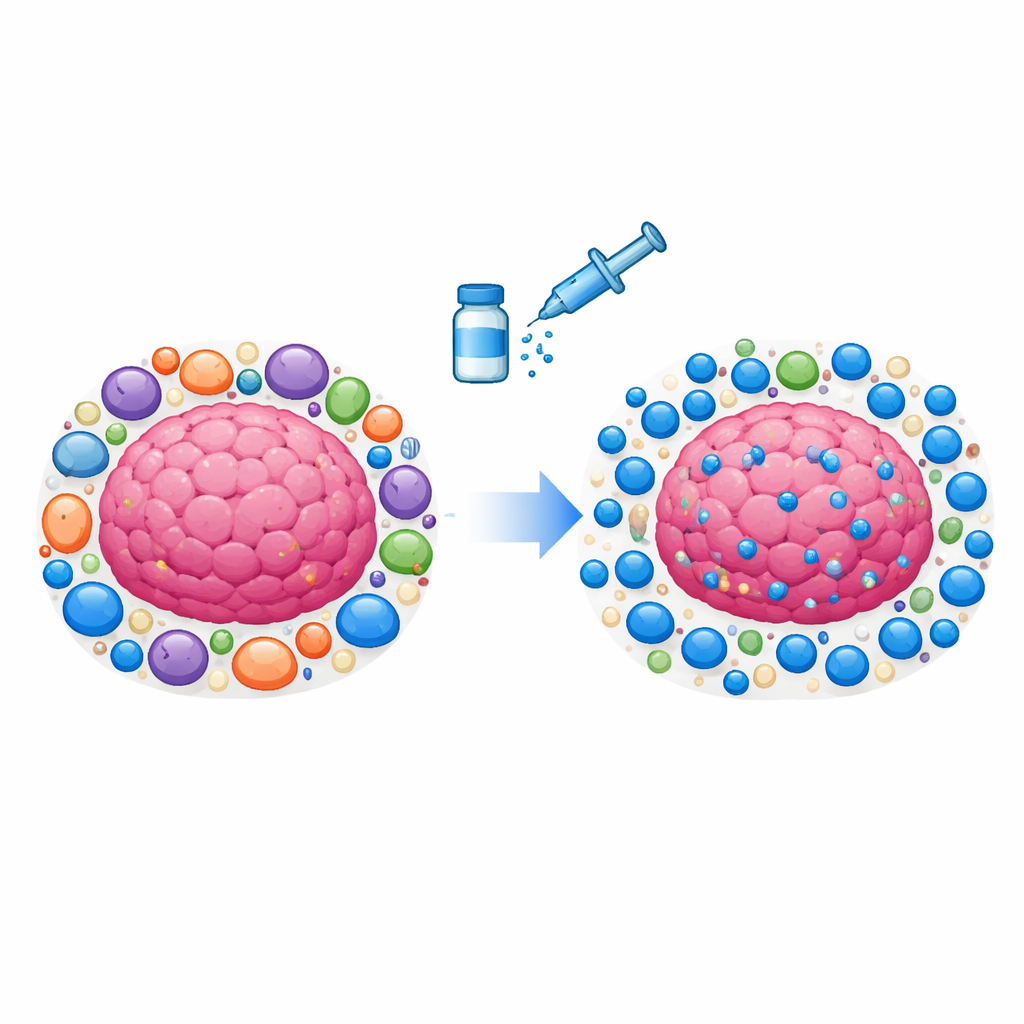
الخلايا التائية المضادة للتنظيم: مراقبو الجهاز المناعي الداخليون
تُبرز المراجعة اكتشافًا غير متوقع: يحمل جسمنا طبيعيًا أعدادًا صغيرة من الخلايا التائية التي تتعرف تحديدًا على هذه الجزيئات الكابحة والخلايا التي تُنتجها. هذه «الخلايا التائية المضادة للتنظيم»، أو anti‑Tregs، ليست نوعًا خاصًا من الخلايا بل خلايا تائية مساعدة وقاتلة عادية تستهدف بروتينات مثل IDO، وPD‑L1، والأرجيناز‑1، وTGF‑β—وهم لاعبون رئيسيون في كبح المناعة وتكوين الندبات النسيجية. عند تنشيطها، يمكن لـ anti‑Tregs قتل الخلايا الكابحة مباشرة أو إعادة برمجتها بإفراز رسائل التهابية. في الواقع، هي تراقب المنظّمات وتمنع قفل الجهاز المناعي في حالة «الفرامل مفعّلة» بشكل دائم. ومن المهم أن مثل هذه الخلايا توجد حتى في الأشخاص الأصحّاء، ما يشير إلى أنها جزء من توازن مناعي طبيعي بدلاً من علامة على المرض.
لقاحات تستهدف ملاذ السرطان، لا الخلايا السرطانية وحدها
تحاول لقاحات السرطان التقليدية تدريب الخلايا التائية على التعرف إلى علامات على الخلايا السرطانية نفسها. تتخذ لقاحات IMV نهجًا مختلفًا: فهي تحتوي على قطع قصيرة من بروتينات الجزيئات الكابحة والخلايا الداعمة في حيّ الورم—المسماة مجتمعة مستضدات البيئة المصاحبة للورم. بعد التطعيم، تتوسع anti‑Tregs وتتجه إلى أي خلية تعرض هذه المستضدات، سواء كانت خلية سرطانية، أو خلية مناعية، أوليفروبلاست يساهم في بناء ندبة صلبة تحول دون الدخول. تزيل الخلايا التائية القاتلة هذه الخلايا مباشرة، بينما تملأ الخلايا المساعدة المنطقة بإشارات تعزز عرض المستضدات، وتجتذب مقاتلين إضافيين، وتلين الحواجز النسيجية الصلبة. يمكن لهذا الفعل ذي الحدّين أن يحوّل الورم «البارد» ذا النفاذية المنخفضة إلى ورم «ساخن» ملتهب يصبح أكثر قابلية للعلاجات المناعية الأخرى. 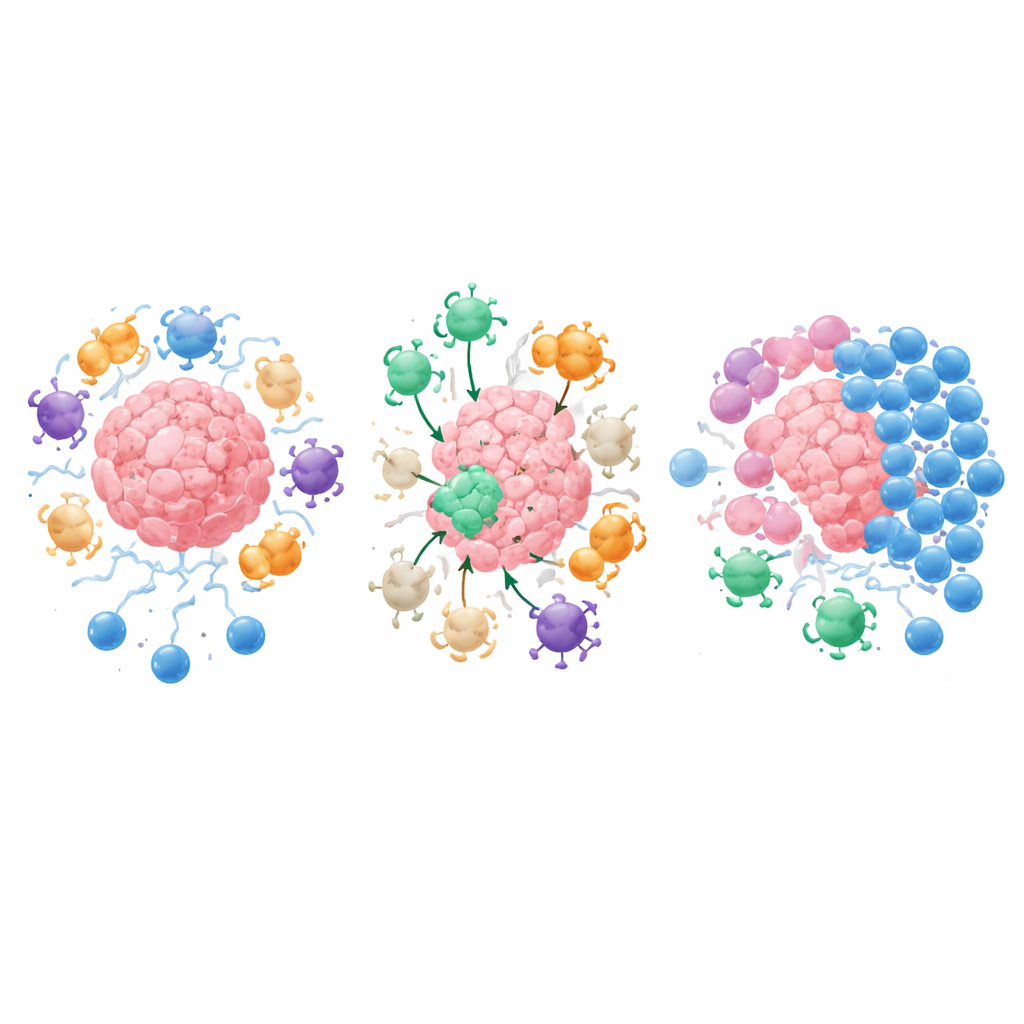
دلائل من دراسات حيوانية وتجارب سريرية مبكرة
في نماذج فأرية متعددة، أبطأت اللقاحات التي تستهدف جزيئات مثل IDO، وPD‑L1، والأرجيناز، وTGF‑β نمو الأورام، وقلّلت الخلايا الكابحة للمناعة، وزادت الخلايا التائية القاتلة داخل الأورام. كانت هذه التأثيرات أقوى عند الجمع مع أدوية مثبطة لنقطة التفتيش PD‑1. تعكس التجارب البشرية المبكرة هذه النتائج إلى حد كبير: فقد أثبتت لقاحات IMV المعتمدة على الببتيد والـmRNA أمانها وتحفّز بشكل متكرر استجابات قابلة للقياس من الخلايا التائية ضد أهدافها، غالبًا مع انخفاض أعداد أو نشاط الخلايا الكابحة في عينات الدم والورم. أبلغت دراسة من المرحلة الثانية في الميلانوما جمعت لقاح IDO/PD‑L1 مع علاج مضاد لـPD‑1 عن معدلات استجابة عالية وتحكّم طويل الأمد، وأظهرت تجربة أكبر من المرحلة الثالثة بقاءً أطول دون تقدم للمرض بشكل عام، مع أوضح فائدة لدى المرضى الذين تلقوا حصر PD‑1 للمرة الأولى وفي الأورام التي كانت في البداية سلبية لـPD‑L1.
التطلع إلى ما وراء السرطان: العدوى والاستخدامات المستقبلية
تظهر الحيل الكابحة نفسها التي تستخدمها الأورام أيضًا في العدوى المزمنة وفي العدوى الحادة الشديدة لدى المسنين أو الضعفاء. يجادل المقال بأن مفهوم IMV—التلقيح ضد فرامل الجسم المفرطة النشاط—قد يساعد في نهاية المطاف على تطهير الفيروسات المستمرة أو تعزيز الاستجابات للقاحات القياسية لدى كبار السن عن طريق إعادة تشكيل البيئات المناعية المحلية. وفي الوقت نفسه، يحذّر من ضرورة الحذر في أمراض المناعة الذاتية، حيث قد يؤدي تقليل التنظيم بشكل مفرط إلى تفاقم الاعتداءات الموجهة ضد الذات. في المجمل، الخلاصة أن لقاحات IMV تضيف طبقة جديدة للعلاج المناعي: فبدلاً من تجنيد جنود أكثر فقط، فإنها تفكك حصن العدو. عند استخدامها بالاشتراك مع الأدوية الحالية وبالتحرك مبكرًا في مسار المرض، قد تساعد هذه الاستراتيجية المزيد من المرضى على استعادة سيطرة مناعية دائمة على السرطان وأمراض أخرى صعبة العلاج.
الاستشهاد: Andersen, M.H. Immune modulatory vaccines targeting tumor microenvironment antigens: recent advances in oncology and beyond. Sig Transduct Target Ther 11, 130 (2026). https://doi.org/10.1038/s41392-026-02710-8
الكلمات المفتاحية: البيئة المصاحبة للورم, لقاحات السرطان, منع نقاط التفتيش المناعية, علاج الخلايا التائية, المناعة المُعدَّلة