Clear Sky Science · zh
用于预测局部递送的吸入药物剂量的高分辨率全肺计算机模型
这对肺病患者为何重要
数以百万计的哮喘、慢性阻塞性肺病或肺纤维化患者依赖吸入器,但医生仍无法确切看到药物在每个人肺内的落点。药物是否真正到达病灶,还是大多滞留在咽喉和大气道?由于在活体中难以测量,吸入药物的开发通常缓慢且昂贵,剂量常根据粗略平均值而非个体需求来设定。该研究提出了一个详尽的人体肺部计算模型,能够逐一预测每个患者每个微小吸入颗粒的去向与沉积位置,可能彻底改变吸入药物的设计与处方方式。
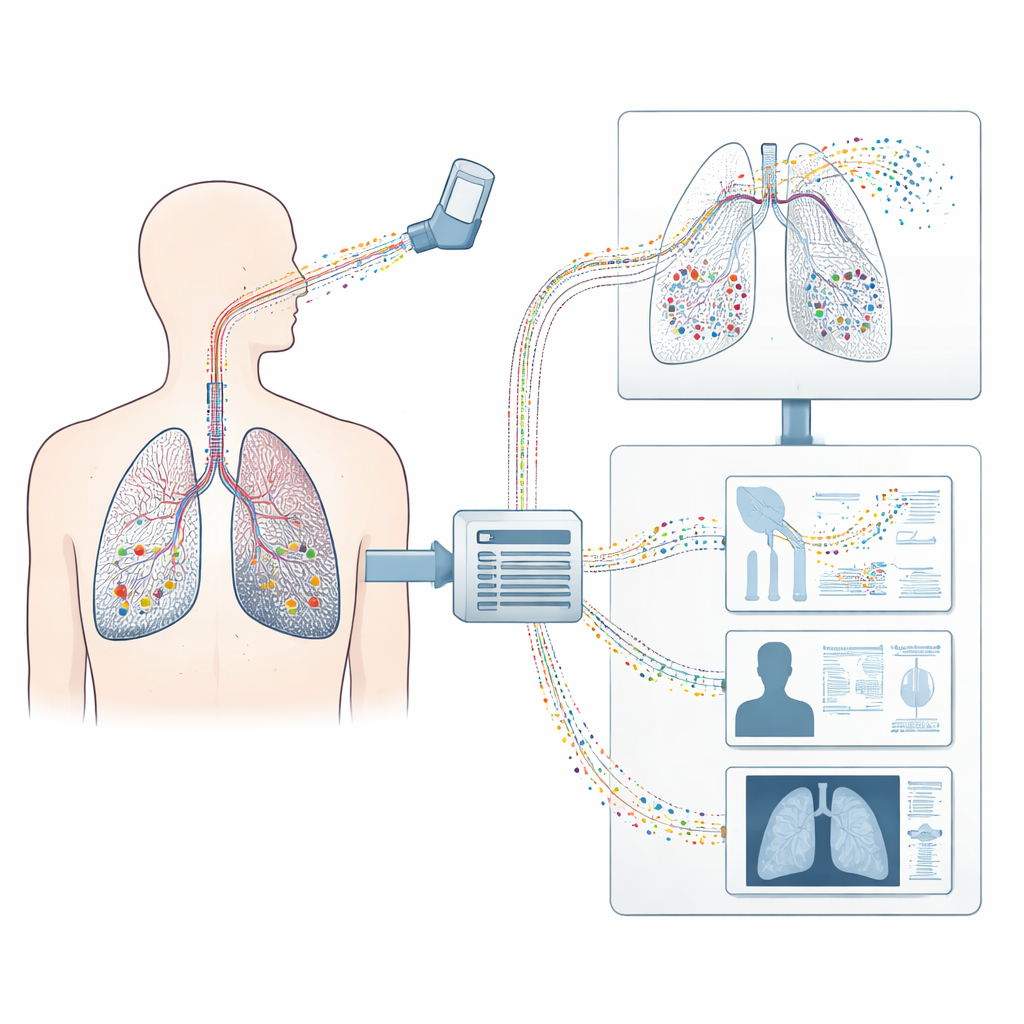
将肺部扫描变成虚拟孪生体
研究人员以标准医学CT扫描为起点,构建出个人肺部的三维“数字孪生”。他们在数字上提取肺表面、不同肺叶和可见气道的形状。由于CT只能看到较大的分支,一种特殊的生长算法补全了缺失的小气道以及进行气体交换的数亿个葡萄状肺泡。结果是完整的导气道分支树,连接着大量简化的肺泡单元,以及驱动呼吸运动的胸壁和膈等周围结构。该完整模型同时捕捉了几何形态和健康或病变肺组织的力学行为。
用物理而非猜测追踪每个颗粒
在这个数字肺之上,团队运行了基于物理的气流和组织运动模拟,使其随真实记录的呼吸模式做进出气的动态变化。随后释放代表吸入药物的虚拟颗粒,逐一计算它们在随动空气中被携带、碰撞、减速,最终粘附在气道壁或肺泡表面,或在呼气时被带走的路径。不同于将肺视为一组管道或一维“喇叭形”简化模型的方法,这种方法解析了从气管到最深处的完整三维路径。它在呼吸周期的每一时刻追踪每个颗粒,生成药物最终落点的高分辨率“地图”。
与健康志愿者的真实扫描数据比对
为验证计算预测是否反映现实,作者将结果与早期临床研究中六名吸入放射性气溶胶的健康志愿者的核成像数据进行了比较。该研究使用SPECT/CT扫描来可视化颗粒在肺内的沉积位置。在两种颗粒尺寸和两种呼吸模式下进行的十次不同吸入实验中,模型预测了每个肺叶到达的药物质量以及药物是更多沉积在中央还是外围区域。这些预测与基于扫描的测量高度吻合,典型差异仅为几个百分点。模型还再现了影像中观察到的小颗粒更易深入组织的趋势,这是此前整肺模拟很少定量捕捉到的现象。
聚焦深部组织与病变区域
由于虚拟肺包含了每一代气道以及整个肺泡区,它能揭示影像难以提供的细节。研究人员分析了吸入剂量在大气道与细小气体交换组织之间的分布,以及其如何随呼吸方式和颗粒大小变化。他们还构建了一个特发性肺纤维化肺的模型,这种疾病会使部分组织变硬并形成瘢痕。通过对CT上可见的纤维化区域赋予更高的刚度,他们发现这些病变区域每单位体积所接受的药物约少40%。这表明标准剂量可能恰恰对最需要药物的区域治疗不足,且药物与装置设计可能需要为病变肺进行调整。
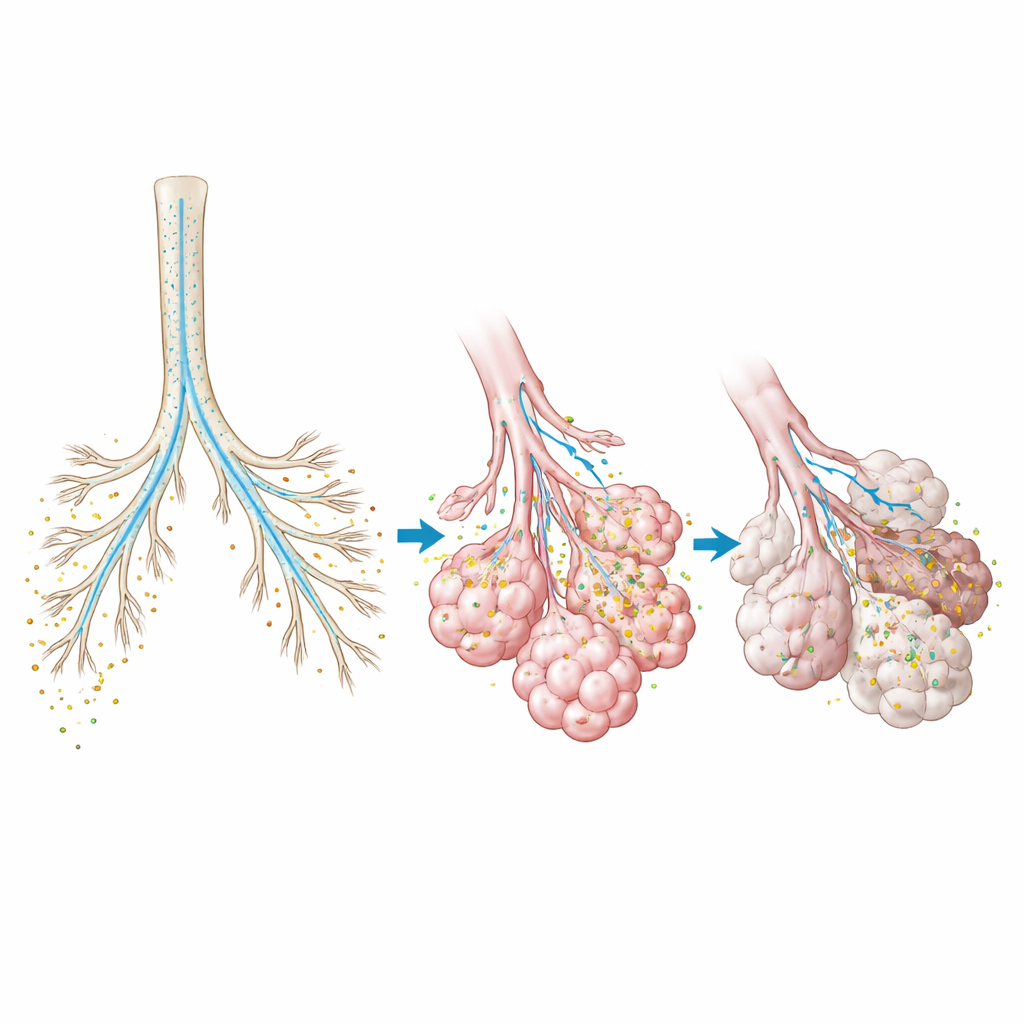
从更优吸入器到更少放射性扫描
简言之,这项工作表明,从患者扫描构建的计算模型可以准确预测吸入药物在其肺内的落点,而无需让患者接受额外的放射或侵入性检测。此类工具可帮助工程师设计将更多药物递送到目标区域的吸入器,帮助医生依据每种疾病模式选择适合的颗粒大小和呼吸指导,并为监管机构提供评估仿制吸入器是否与品牌产品等效的方法。借助快速、主要自动化的模型生成和高效计算,作者认为虚拟肺试验最终可补充甚至替代许多核成像研究,使吸入治疗的开发与个性化更安全、更快且更经济。
引用: Grill, M.J., Biehler, J., Wichmann, KR. et al. In silico high-resolution whole lung model to predict the locally delivered dose of inhaled drugs. Commun Med 6, 188 (2026). https://doi.org/10.1038/s43856-026-01459-z
关键词: 吸入药物递送, 肺部建模, 气溶胶沉积, 个性化医疗, 计算模拟