Clear Sky Science · pl
Model komputerowy całych płuc o wysokiej rozdzielczości in silico do przewidywania lokalnie dostarczanej dawki leków wziewnych
Dlaczego to ma znaczenie dla osób z chorobami płuc
Miliony osób z astmą, POChP czy bliznowaceniem płuc polegają na inhalatorach, a mimo to lekarze wciąż nie mogą dokładnie zobaczyć, gdzie lek osiada w płucach konkretnego pacjenta. Czy substancja naprawdę dociera do zmienionych chorobowo miejsc, czy też głównie zatrzymuje się w gardle i dużych drogach oddechowych? Ponieważ trudno to zmierzyć u żywych osób, rozwój leków wziewnych jest wolny i kosztowny, a dawki często ustala się na podstawie przybliżonych uśrednień zamiast potrzeb indywidualnego pacjenta. W pracy tej przedstawiono szczegółowy model komputerowy ludzkiego płuca, który potrafi przewidzieć, pacjent po pacjencie, dokąd trafia i gdzie osiada każda drobna cząstka wdychanego leku, co może zrewolucjonizować projektowanie i przepisywanie leków wziewnych.
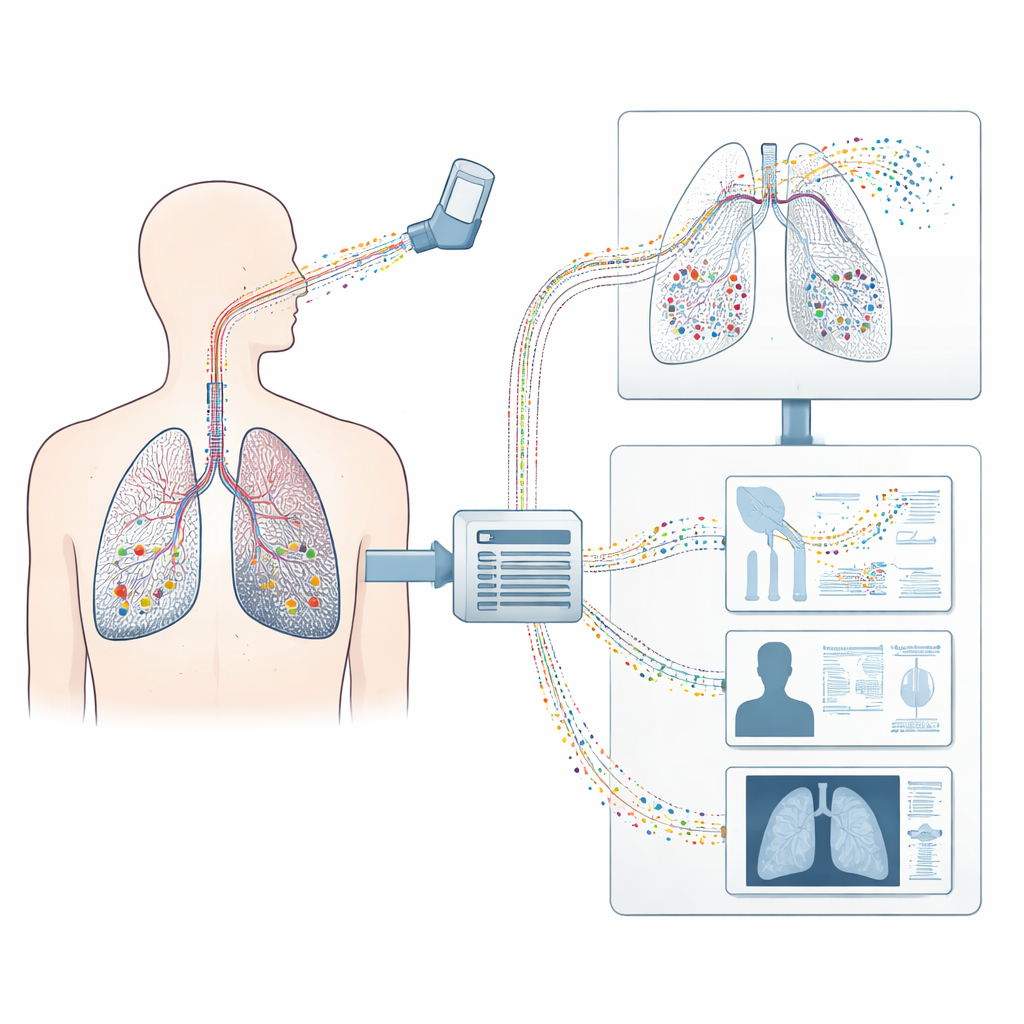
Przekształcanie skanu płuc w wirtualne bliźniacze
Naukowcy zaczynają od standardowego skanu CT i budują trójwymiarowego „cyfrowego bliźniaka” płuc pacjenta. Cyfrowo wydobywają kształt powierzchni płuc, poszczególne płaty oraz widoczne oskrzela. Ponieważ CT widzi tylko większe rozgałęzienia, specjalny algorytm wzrostu uzupełnia brakujące mniejsze drogi oddechowe oraz pół miliarda gronopodobnych pęcherzyków, w których zachodzi wymiana gazowa. Wynikiem jest kompletne drzewo rozgałęzień przewodzących powietrze połączone z niezliczonymi uproszczonymi jednostkami pęcherzykowymi, oraz otaczające struktury takie jak ściana klatki piersiowej i przepona, które napędzają ruch oddechowy. Pełny model odzwierciedla zarówno geometrię, jak i zachowanie mechaniczne zdrowej i chorobowo zmienionej tkanki płucnej.
Śledzenie każdej cząstki za pomocą fizyki, nie zgadywania
Na tym cyfrowym płucu zespół uruchamia symulację opartą na prawach fizyki przepływu powietrza i ruchu tkanki podczas oddychania zgodnie z rzeczywistym zarejestrowanym wzorcem oddechowym. Następnie uwalniają wirtualne cząstki reprezentujące lek wziewny i obliczają ich trajektorie jedną po drugiej, gdy są niesione przez poruszające się powietrze, odbijają się, zwalniają i ostatecznie przylegają do ścian dróg oddechowych lub powierzchni pęcherzykowych, albo zostają wydalone podczas wydechu. W przeciwieństwie do starszych uproszczonych modeli traktujących płuca jako zestaw rurek lub jednowymiarowe „trąbki”, podejście to rozwiązuje pełne trójwymiarowe ścieżki od tchawicy aż do najgłębszych obszarów. Śledzi każdą cząstkę w każdym momencie cyklu oddechowego, dając mapę o wysokiej rozdzielczości pokazującą dokładnie, gdzie trafia lek.
Dopasowanie do rzeczywistych skanów u zdrowych ochotników
Aby sprawdzić, czy przewidywania komputera odzwierciedlają rzeczywistość, autorzy porównali wyniki z danymi obrazowania nuklearnego z wcześniejszego badania klinicznego przeprowadzonego na sześciu zdrowych ochotnikach, którzy inhalowali radioaktywny aerozol. Tamto badanie używało skanerów SPECT/CT do wizualizacji miejsc osadzania cząstek w płucach. Dla dziesięciu różnych eksperymentów inhalacyjnych z dwoma rozmiarami cząstek i dwoma wzorcami oddychania model przewidział, ile masy leku trafiło do każdego płata płuca i czy osiadło bardziej centralnie, czy w obszarach obwodowych. Przewidywania te bardzo dobrze zgadzały się z pomiarami ze skanów, z typowymi rozbieżnościami rzędu zaledwie kilku punktów procentowych. Model odtworzył także zależność, że mniejsze cząstki przenikają głębiej w tkankę — efekt widoczny w obrazowaniu, wcześniej nigdy nie uchwycony tak ilościowo przez symulację całych płuc.
Przybliżanie się do głębokiej tkanki i obszarów chorych
Ponieważ wirtualne płuco zawiera każdą generację dróg oddechowych i cały obszar pęcherzykowy, może ujawnić szczegóły, których obrazowanie nie dostarcza łatwo. Naukowcy analizowali, jaka część dawki wziewnej osadza się w dużych drogach oddechowych w porównaniu z drobną, wymieniającą gazy tkanką oraz jak to zmienia się w zależności od stylu oddychania i rozmiaru cząstek. Zbudowali także model płuca z idiopatycznym włóknieniem płuc, chorobą, która usztywnia i bliznowacie fragmenty tkanki. Przypisując wyższą sztywność obszarom włókniejącym widocznym na CT, wykazali, że te zmienione chorobowo strefy otrzymywały około 40% mniej leku na jednostkę objętości niż zdrowsze rejony. Wskazuje to, że standardowe dawkowanie może nie leczyć wystarczająco tych miejsc, które najbardziej potrzebują leku, i że projekt leków oraz urządzeń może wymagać dostosowania do płuc z chorobą.
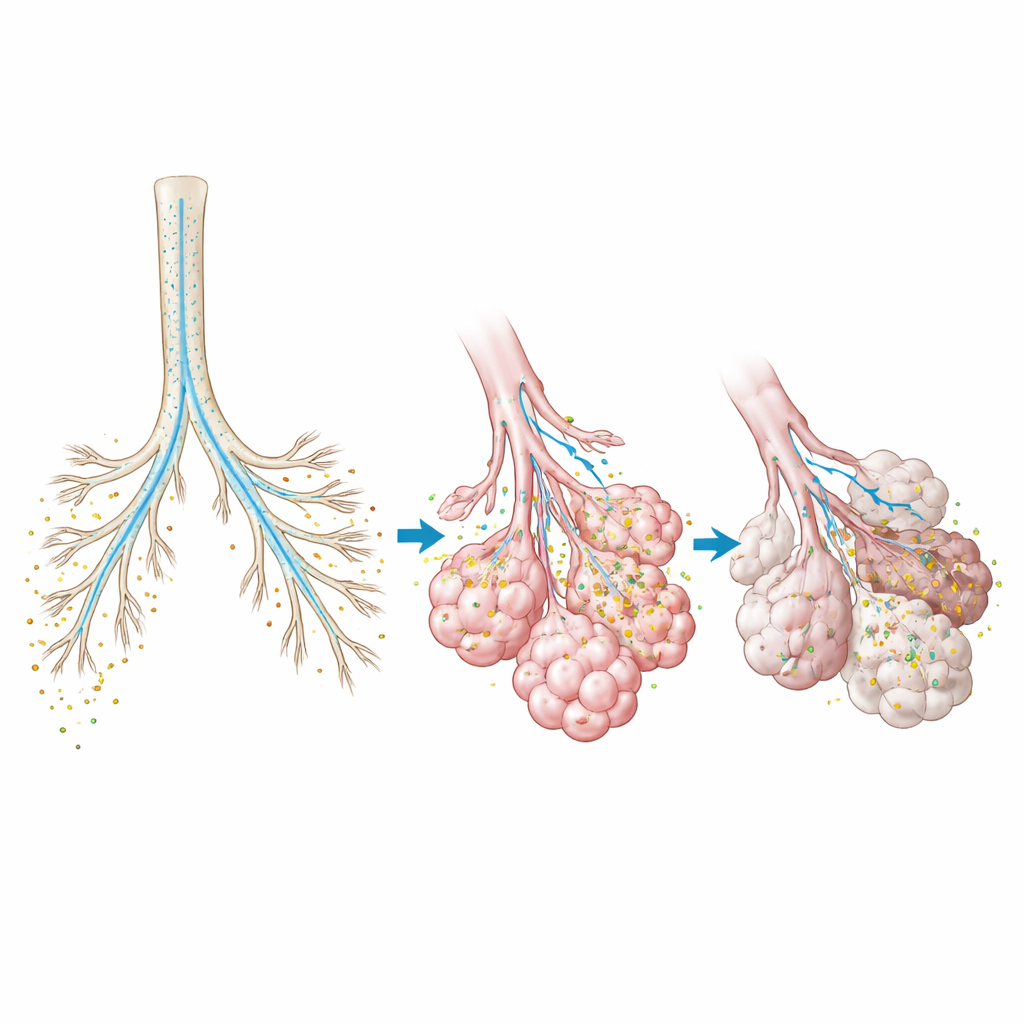
Od lepszych inhalatorów do mniejszej liczby skanów radiologicznych
Mówiąc prościej, praca ta pokazuje, że model komputerowy zbudowany na podstawie skanu pacjenta może dokładnie przewidzieć, gdzie lek wziewny wyląduje w jego płucach, bez narażania na dodatkowe promieniowanie czy inwazyjne badania. Takie narzędzie mogłoby pomóc inżynierom projektować inhalatory dostarczające więcej leku do odpowiednich rejonów, pomóc lekarzom wybrać rozmiar cząstek i instrukcje oddechowe dostosowane do wzorca chorobowego pacjenta, a regulatorom dać sposób na sprawdzenie, czy inhalator generyczny naprawdę odpowiada produktowi markowemu. Dzięki szybkiemu, w dużej mierze zautomatyzowanemu generowaniu modeli i wysokiej efektywności obliczeniowej autorzy twierdzą, że wirtualne próby płuc mogłyby w przyszłości uzupełniać lub nawet zastąpić wiele badań obrazowania nuklearnego, czyniąc rozwój i personalizację terapii wziewnych bezpieczniejszymi, szybszymi i tańszymi.
Cytowanie: Grill, M.J., Biehler, J., Wichmann, KR. et al. In silico high-resolution whole lung model to predict the locally delivered dose of inhaled drugs. Commun Med 6, 188 (2026). https://doi.org/10.1038/s43856-026-01459-z
Słowa kluczowe: dostarczanie leków wziewnych, modelowanie płuc, osadzanie aerozolu, medycyna spersonalizowana, symulacja komputerowa