Clear Sky Science · ru
Ин силуко модель всего лёгкого с высоким разрешением для прогнозирования локально доставленной дозы ингалируемых препаратов
Почему это важно для людей с заболеваниями лёгких
Миллионы людей с астмой, ХОБЛ или рубцеванием лёгких зависят от ингаляторов, но врачи по‑прежнему не могут точно увидеть, где именно в лёгких каждого человека оседает лекарство. Попадает ли препарат в поражённые участки или в основном задерживается в горле и крупных дыхательных путях? Поскольку это трудно измерить в живом человеке, разработка ингалируемых препаратов идёт медленно и дорого, а дозы часто устанавливают, опираясь на усреднённые данные, а не на потребности конкретного пациента. В этом исследовании представлен подробный компьютерный модель лёгкого человека, которая способна предсказывать для каждого пациента, куда попадает и оседает каждая крошечная частица ингалятора, что потенциально может изменить подход к проектированию и назначению ингалируемых лекарств.
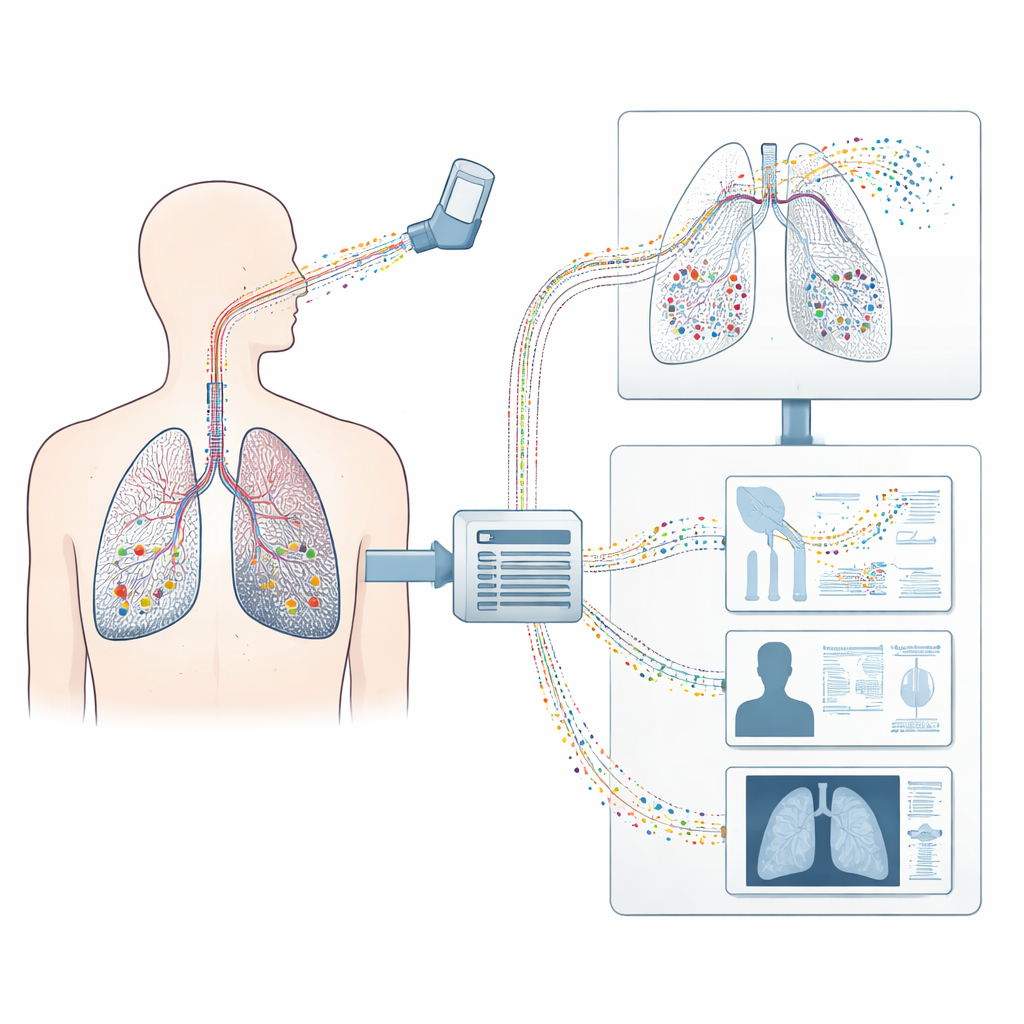
Преобразование снимка лёгкого в виртуального двойника
Исследователи начинают со стандартного медицинского КТ‑снимка и строят трёхмерный «цифровой двойник» лёгких пациента. Они цифровым способом выделяют форму поверхностей лёгких, отдельные доли и видимые дыхательные пути. Поскольку КТ видит только более крупные ветви, специальный алгоритм роста заполняет недостающие мелкие бронхи и полмиллиарда гроздевидных альвеол, где происходит газообмен. В результате получается полное ветвление проводящих дыхательных путей, связанное с многочисленными упрощёнными альвеолярными единицами, а также окружающие структуры — стенка грудной клетки и диафрагма, обеспечивающие дыхательное движение. Эта полная модель отражает как геометрию, так и механическое поведение здоровой и поражённой ткани лёгкого.
Прослеживание каждой частицы при помощи физических законов, а не догадок
Поверх этого цифрового лёгкого команда запускает физически обоснованную симуляцию потока воздуха и движения ткани при вдохе и выдохе по реальной записанной дыхательной траектории. Затем они выпускают виртуальные частицы, представляющие ингалируемое лекарство, и вычисляют их траектории по‑одной: как частицы переносятся движущимся воздухом, отскакивают, замедляются и в конечном итоге прилипают к стенкам дыхательных путей или альвеолярным поверхностям, либо снова выносятся при выдохе. В отличие от старых упрощённых моделей, рассматривавших лёгкое как набор труб или одномерные «трубы», этот подход разрешает полные трёхмерные пути от трахеи до самых глубоких областей. Модель отслеживает каждую частицу в каждый момент дыхательного цикла, давая высокоразрешающую «карту» точного местоположения препарата.
Сопоставление с реальными сканами у здоровых добровольцев
Чтобы проверить, отражают ли компьютерные прогнозы реальность, авторы сравнили свои результаты с данными ядерной визуализации из предыдущего клинического исследования, в котором шесть здоровых добровольцев вдыхали радиоактивный аэрозоль. В том исследовании использовали SPECT/CT‑сканеры для визуализации мест отложения частиц в лёгких. Для десяти различных экспериментов ингаляции с двумя размерами частиц и двумя дыхательными режимами модель предсказала, какая доля массы препарата достигала каждой доли лёгкого и оседала ли она в центральных или периферических областях. Эти предсказания очень хорошо соответствовали измерениям по сканам, с типичными расхождениями всего в несколько процентных пунктов. Модель также воспроизвела тот факт, что более мелкие частицы проникают глубже в ткань — эффект, наблюдавшийся в визуализации, но никогда ранее так количественно не захваченный в модели всего лёгкого.
Приближение к глубокой ткани и поражённым областям
Поскольку виртуальное лёгкое включает каждое поколение дыхательных путей и всю альвеолярную область, оно может выявлять детали, которые визуализация даёт с трудом. Исследователи проанализировали, какая часть вдыхаемой дозы откладывается в крупных дыхательных путях по сравнению с тонкой тканью, обменивающей газ, и как это меняется в зависимости от стиля дыхания и размера частиц. Они также создали модель лёгкого с идиопатическим лёгочным фиброзом — заболеванием, которое уплотняет и рубцует участки ткани. Присвоив более высокую жёсткость фиброзным зонам, видимым на КТ, они показали, что эти поражённые участки получали примерно на 40% меньше лекарства на единицу объёма, чем более здоровые области. Это указывает на то, что стандартные дозировки могут недолечивать именно те регионы, которым больше всего нужна терапия, и что дизайн препаратов и устройств может потребовать адаптации для поражённых лёгких.
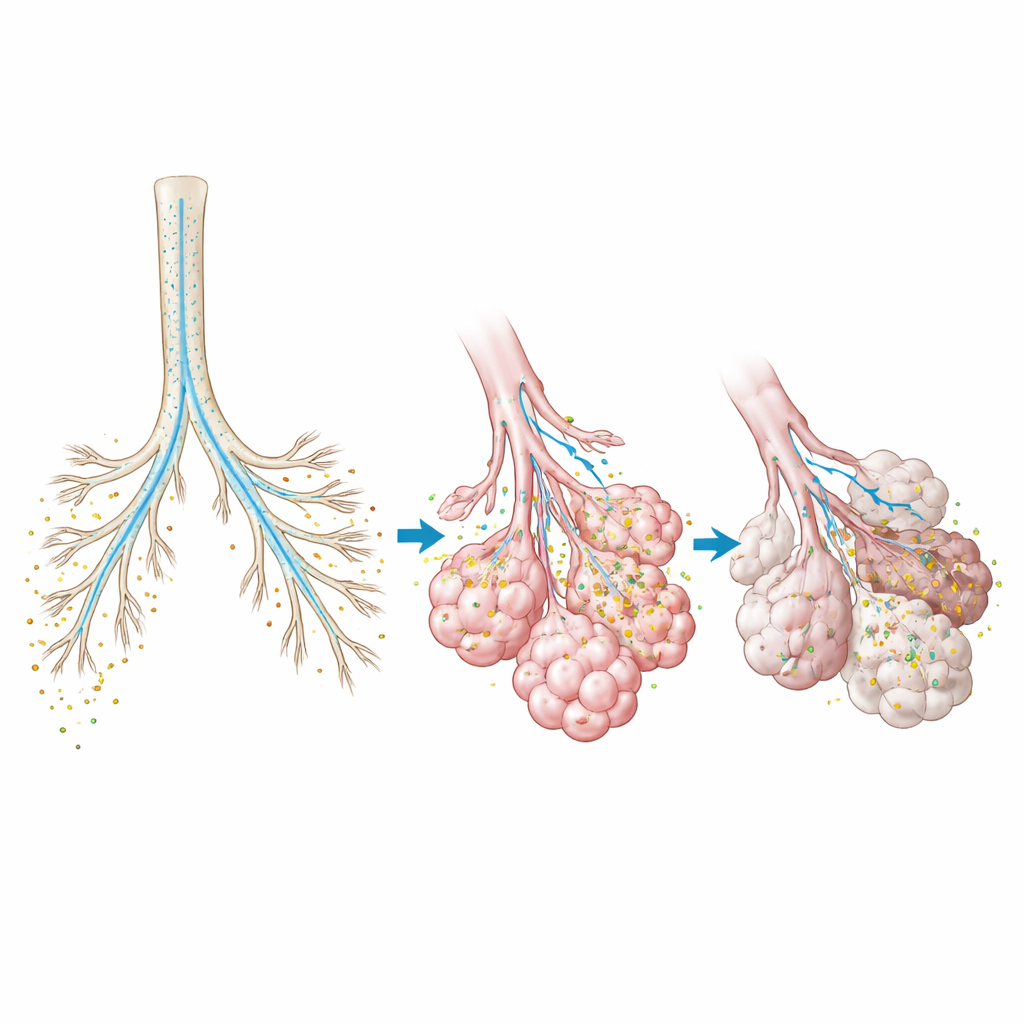
От улучшения ингаляторов до сокращения числа радиоактивных сканов
Проще говоря, эта работа показывает, что компьютерная модель, построенная по КТ‑снимку пациента, может точно предсказать, куда в его лёгких попадёт ингалируемое лекарство, без дополнительного облучения или инвазивных исследований. Такой инструмент может помочь инженерам проектировать ингаляторы, доставляющие больше препарата в нужные области, помочь врачам выбирать размер частиц и инструкции по дыханию в соответствии с паттерном заболевания конкретного пациента, а также дать регуляторам способ проверить, соответствует ли дженерик оригинальному препарату. Благодаря быстрой, в основном автоматизированной генерации моделей и высокой вычислительной эффективности авторы утверждают, что виртуальные клинические испытания лёгких в будущем могут дополнить или даже заменить многие исследования с ядерной визуализацией, сделав разработку и персонализацию ингалируемых терапий более безопасной, быстрой и дешёвой.
Цитирование: Grill, M.J., Biehler, J., Wichmann, KR. et al. In silico high-resolution whole lung model to predict the locally delivered dose of inhaled drugs. Commun Med 6, 188 (2026). https://doi.org/10.1038/s43856-026-01459-z
Ключевые слова: доставка ингалируемых препаратов, моделирование лёгких, отложение аэрозоля, персонализированная медицина, компьютерное моделирование