Clear Sky Science · tr
İnteraktif yüksek çözünürlüklü tüm akciğer modeli ile inhale ilaçların lokal olarak bırakılan dozu tahmin etme
Akciğer hastaları için bunun önemi nedir
Astım, KOAH veya akciğer skarı olan milyonlarca insan inhaler kullanıyor, ancak doktorlar hâlâ ilacın her kişinin akciğerinde tam olarak nereye ulaştığını göremiyor. İlaç gerçekten hastalıklı bölgelere mi gidiyor yoksa çoğunlukla boğazda ve büyük hava yollarında mı takılıyor? Canlı insanlar içinde bunu ölçmek zor olduğundan inhale ilaç geliştirme yavaş ve maliyetli oluyor ve dozlar sıklıkla bireysel hastanın ihtiyaçları yerine kaba ortalamalara göre belirleniyor. Bu çalışma, her hastada her bir küçük inhale partikülün nereye gittiğini ve nerede biriktiğini tahmin edebilen ayrıntılı bir bilgisayar modeli tanıtıyor; bu, inhale ilaçların tasarımı ve reçetelenme biçimini kökten değiştirebilir.
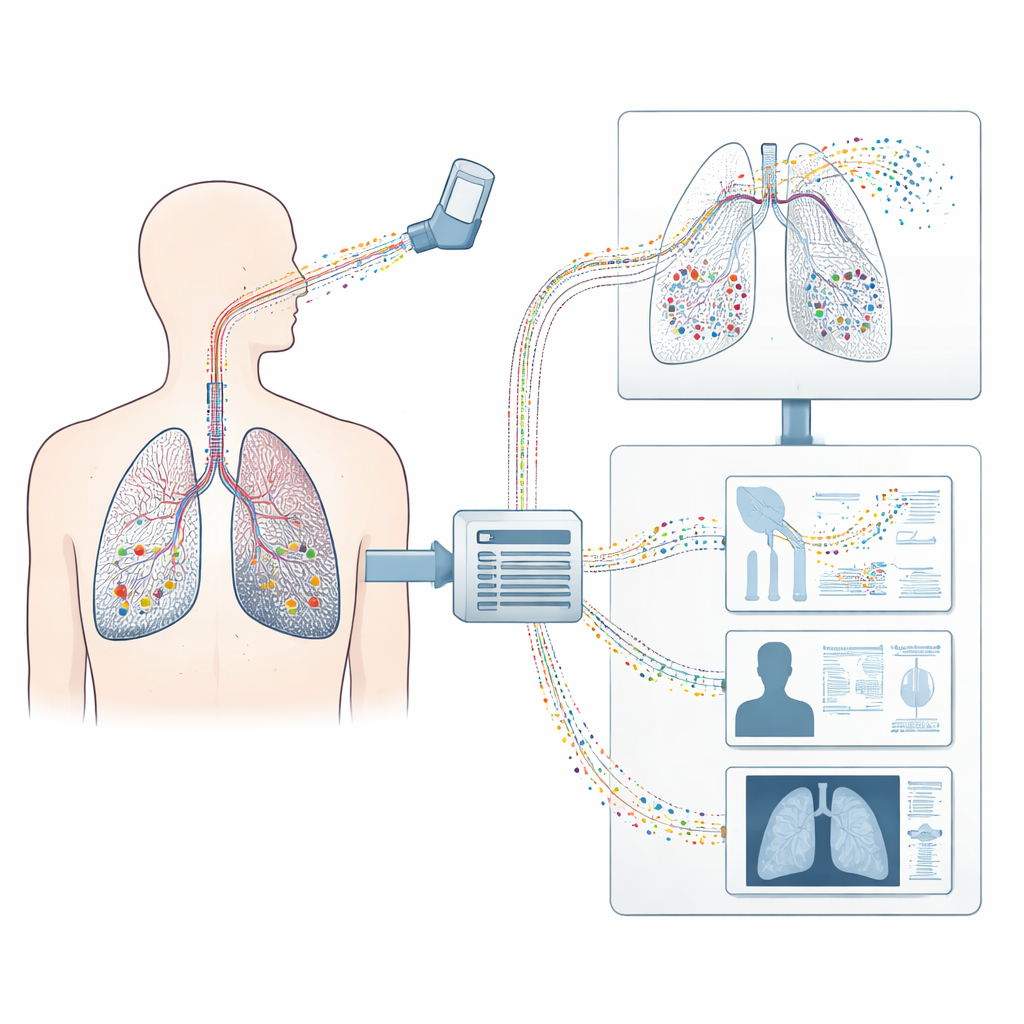
Bir akciğer taramasını sanal bir ikizine dönüştürmek
Araştırmacılar standart bir tıbbi BT taramasından başlayarak kişinin akciğerlerinin üç boyutlu bir “dijital ikizini” inşa ediyor. Akciğer yüzeylerinin, farklı lobların ve görülebilen hava yollarının şeklini dijital olarak çıkarıyorlar. BT sadece daha büyük dalları görebildiği için, eksik daha küçük hava yollarını ve gaz alışverişinin gerçekleştiği yarım milyar üzüm tanesi görünümündeki alveolleri dolduran özel bir büyüme algoritması kullanılıyor. Ortaya çıkan yapı, sayısız basitleştirilmiş alveoler birime bağlı tam bir iletici havayolu ağacı ve solunum hareketini sağlayan göğüs duvarı ile diyafram gibi çevre yapıları içeriyor. Bu tam model, hem geometriyi hem de sağlıklı ve hastalıklı akciğer dokusunun mekanik davranışını yakalıyor.
Tahminler yerine fizik kurallarıyla her partikülü izlemek
Bu dijital akciğer üzerinde ekip, bir kişinin gerçek kaydedilmiş bir solunum deseni boyunca nefes alıp verirken hava akışı ve doku hareketinin fiziksel tabanlı bir simülasyonunu çalıştırıyor. Ardından inhale edilen ilacı temsil eden sanal partiküller salıyorlar ve bunların hareketli hava tarafından taşınırken tek tek yollarını hesaplıyorlar; çarpma, yavaşlama ve sonunda hava yolları duvarlarına veya alveoler yüzeylere yapışma ya da ekshalasyon sırasında tekrar dışarı çıkma gibi olguları izliyorlar. Akciğeri bir dizi tüp veya tek boyutlu “trampet”ler olarak ele alan eski basitleştirilmiş modellerin aksine, bu yaklaşım soluk borusundan en derin bölgelere kadar tam üç boyutlu yolları çözümleyebiliyor. Her bir partikülü solunum döngüsünün her anında takip ederek ilacın tam olarak nerede biriktiğine dair yüksek çözünürlüklü bir “harita” sunuyor.
Sağlıklı gönüllülerde gerçek taramalarla uyum
Bilgisayar tahminlerinin gerçekliği yansıtıp yansıtmadığını test etmek için yazarlar, önceki bir klinik çalışmada radyoaktif aerosol soluyan altı sağlıklı gönüllüden elde edilen nükleer görüntüleme verileriyle sonuçlarını karşılaştırdılar. O çalışma, partiküllerin akciğerlere nerede yerleştiğini görselleştirmek için SPECT/BT tarayıcıları kullandı. İki partikül boyutu ve iki solunum deseniyle yapılan on farklı inhalasyon deneyi için model, her bir akciğer lobuna ne kadar ilaç kütlesinin ulaştığını ve ilacın daha merkezi mi yoksa periferik bölgelere mi yerleştiğini tahmin etti. Bu tahminler, tipik olarak yalnızca birkaç yüzdelik puanlık sapmayla tarama temelli ölçümlerle yakın şekilde eşleşti. Model ayrıca daha küçük partiküllerin dokuya daha derin nüfuz etme eğilimini yeniden üretti; bu etki görüntülemede gözlemlenmişti ancak tüm akciğer simülasyonu tarafından bu kadar niceliksel olarak yakalanmamıştı.
Derin doku ve hastalıklı alanlara yakın çekim
Sanal akciğer her kuşak hava yolunu ve tüm alveoler bölgeyi içerdiği için görüntülemenin kolayca sağlayamadığı ayrıntıları ortaya koyabiliyor. Araştırmacılar inhale edilen dozumun ne kadarının büyük hava yollarında ve ne kadarının ince, gaz değişimi yapan dokuda çöktüğünü ve bunun solunum tarzı ile partikül boyutuna göre nasıl değiştiğini analiz ettiler. Ayrıca doku bölgelerini sertleştiren ve yara bırakan idiyopatik pulmoner fibrozisi olan bir akciğer modeli oluşturdular. BT’de görülen fibrotik bölgelere daha yüksek sertlik atayarak bu hastalıklı bölgelerin birim hacim başına sağlıklı bölgelere göre yaklaşık %40 daha az ilaç aldığı gösterildi. Bu, standart dozlamanın en çok ilaca ihtiyaç duyan bölgeleri yeterince tedavi etmeyebileceğini ve ilaç ile cihaz tasarımlarının hastalıklı akciğerler için uyarlanması gerekebileceğini öne sürüyor.
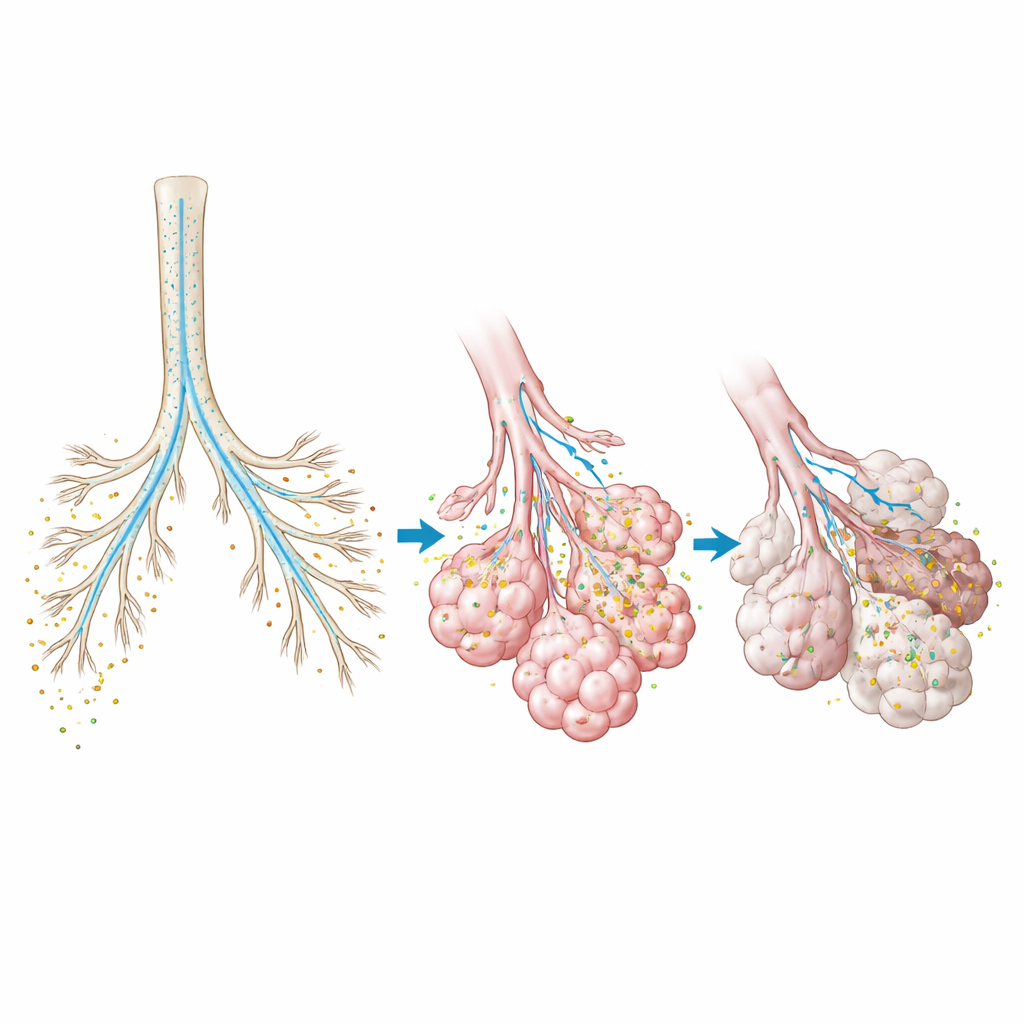
Daha iyi inhalerlerden daha az radyoaktif taramaya
Basitçe söylemek gerekirse, bu çalışma bir hastanın taramasından oluşturulan bilgisayar modelinin inhale edilen ilacın akciğerlerinin neresine düşeceğini doğru şekilde öngörebileceğini gösteriyor; bunu yaparken hastayı ek radyasyona ya da invaziv testlere maruz bırakmıyor. Böyle bir araç, ilacı doğru bölgelere daha etkili ulaştıran inhalerlerin tasarlanmasında mühendislerin işine yarayabilir, doktorların partikül boyutu ve solunum talimatlarını her hastanın hastalık desenine göre seçmesine yardımcı olabilir ve düzenleyicilere bir jenerik inhalerin marka ürünle gerçekten eşdeğer olup olmadığını test etme yolu sunabilir. Hızlı, büyük ölçüde otomatik model üretimi ve yüksek hesaplama verimliliği ile yazarlar, sanal akciğer denemelerinin nihayetinde birçok nükleer görüntüleme çalışmasını tamamlayabileceğini veya hatta yerini alabileceğini, böylece inhale tedavilerin geliştirilmesini ve kişiselleştirilmesini daha güvenli, daha hızlı ve daha düşük maliyetli hale getirebileceğini savunuyorlar.
Atıf: Grill, M.J., Biehler, J., Wichmann, KR. et al. In silico high-resolution whole lung model to predict the locally delivered dose of inhaled drugs. Commun Med 6, 188 (2026). https://doi.org/10.1038/s43856-026-01459-z
Anahtar kelimeler: inhale ilaç uygulaması, akciğer modellemesi, aerosol çökeltimi, kişiselleştirilmiş tıp, hesaplamalı simülasyon