Clear Sky Science · zh
核仁定位的 KANSL2 作为胶质母细胞瘤细胞核糖体生物发生的表观遗传调控因子
这对脑癌有什么意义
胶质母细胞瘤是最致命的脑癌之一,部分原因在于其细胞具有异常强的生长能力并且在治疗后易于复发。本研究揭示了细胞核内一种鲜为人知的蛋白质 KANSL2 如何帮助这些肿瘤细胞强化其内部的蛋白质制造工厂——核糖体。研究表明 KANSL2 直接促进核糖体的生成,这一发现指出了可能被利用来减缓或阻止胶质母细胞瘤生长的新薄弱点。
开启一个隐秘的生长开关
研究人员首先探讨了 KANSL2 在胶质母细胞瘤细胞中是否只是存在,还是与其侵袭性行为直接相关。通过使用将肿瘤组织与正常脑组织比较的大型公共数据集,他们发现 KANSL2 在胶质母细胞瘤中持续性地高表达。KANSL2 水平最高的肿瘤同时显示出更强的“类干细胞”特征——这些细胞能自我更新并更能抵抗治疗。基因分析进一步显示,高水平的 KANSL2 与参与核糖体构建的基因活性升高密切相关,提示该蛋白可能是连接干性、增长与核糖体生成的关键开关。
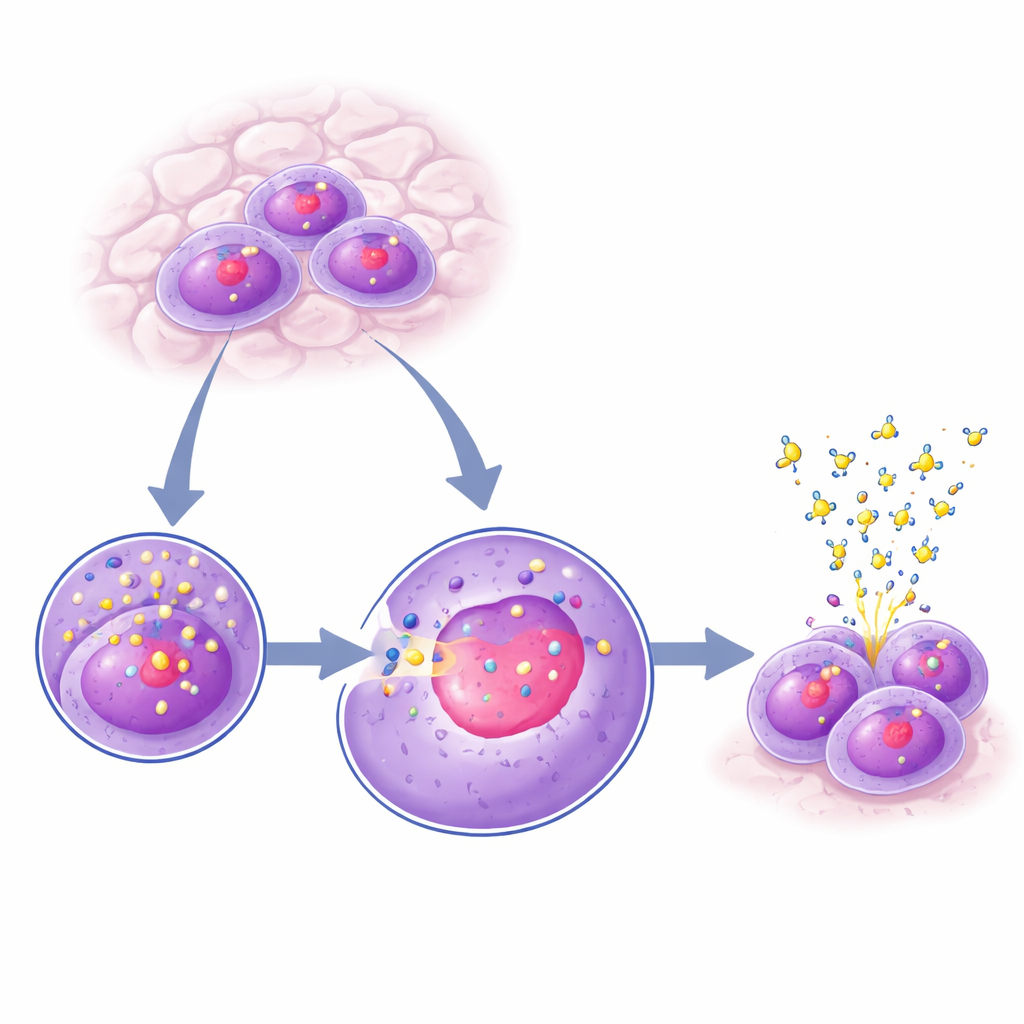
在细胞的制造中心发现 KANSL2
每个细胞核中都有核仁,这是一个密集的区域,也是核糖体诞生之处。通过对不同细胞类型进行染色并在显微镜下观察,研究团队注意到 KANSL2 在核内并非均匀分布:它在核仁中富集。这种富集是动态的——在 DNA 复制前后(细胞周期的 G1 和 G2 期)最为明显,而在 DNA 复制期间(S 期)较弱。当研究者用一种特异性抑制合成核糖体 RNA 的酶的药物处理细胞时,尽管 KANSL2 在细胞内的总量并未改变,但其在核仁中的存在显著下降。这表明当核糖体生产活跃时 KANSL2 会被吸引到核仁,而在该过程被关闭时则离开。
从表观遗传标记到核糖体产出
KANSL2 隶属于一类以修饰 DNA 包装方式而著称的蛋白复合体,主要通过在组蛋白上添加小的化学标记来发挥作用。这些标记可使 DNA 松弛,从而使基因更易被读取。在胶质母细胞瘤细胞中,降低 KANSL2 水平会导致组蛋白 H4 上特定标记的广泛丧失,包括存在于编码核糖体 RNA 的 DNA 片段处。通过染色质免疫沉淀实验,作者证明了 KANSL2 减少会导致核糖体 DNA 启动子处的乙酰化程度下降,而该区域控制着核糖体 RNA 转录的起始。与此一致,缺失 KANSL2 的细胞产生的初始核糖体 RNA 转录本(45S)及其加工产物(28S)减少,而过表达 KANSL2 则增加这些 RNA 种类并提升由核糖体 DNA 启动子驱动的报告子活性。综合来看,这些结果表明 KANSL2 作为表观遗传调控因子,直接上调核糖体 RNA 的发生。
对蛋白质生产系统的连锁影响
KANSL2 的影响超出了少数分子标志物。当团队使用一种标记新合成蛋白质的方法测量新蛋白合成时,KANSL2 降低的胶质母细胞瘤细胞明显吸收更少标记,表明它们的核糖体活性下降。对来自患者的胶质母细胞瘤球体——更能模拟肿瘤的三维培养物——进行整体 RNA 测序显示,沉默 KANSL2 导致与核糖体组装、核糖体蛋白和 RNA 加工相关基因的广泛下调。在细胞水平上,过表达 KANSL2 的细胞增殖更快,而敲低 KANSL2 的细胞分裂变慢并积聚在细胞周期的早期阶段,直接将核糖体产出与增殖联系起来。
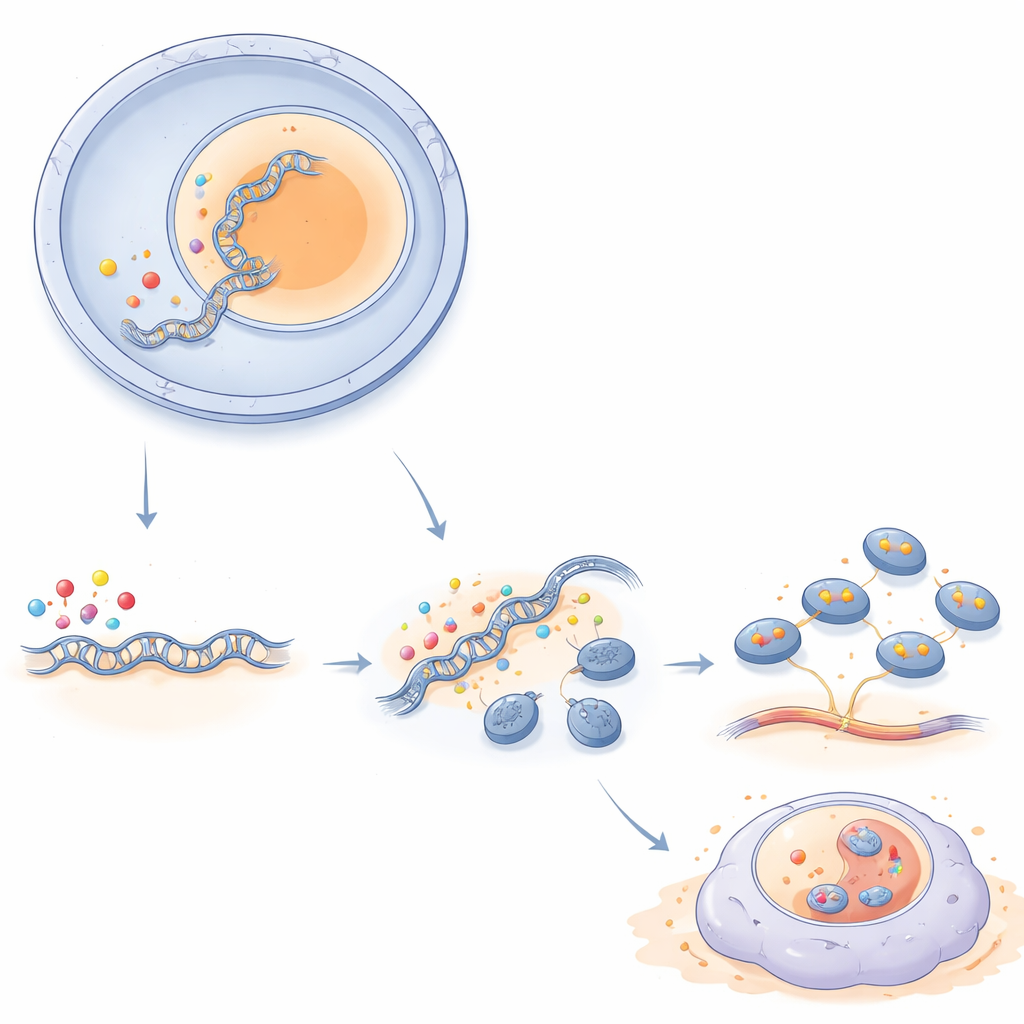
顽固性脑瘤中的新弱点
通过将 KANSL2 与核糖体生成的控制联系起来,本研究解释了胶质母细胞瘤细胞如何维持快速生长和保持类干细胞特性所需的高强度生物合成负荷。KANSL2 在细胞周期的关键窗口迁入核仁,帮助通过组蛋白乙酰化松开核糖体 DNA,从而提升核糖体 RNA 和核糖体的生物发生。由于这些过程在侵袭性肿瘤中尤其亢进,而在正常脑细胞中较不活跃,靶向 KANSL2 或其相关通路可能为抑制肿瘤生长同时保护健康组织提供途径,使其成为未来治疗策略中的有吸引力候选对象。
引用: Budnik, N., Canedo, L., Morellato, A.E. et al. Nucleoli-localized KANSL2 as an epigenetic regulator of ribosome biogenesis in glioblastoma cells. Commun Biol 9, 535 (2026). https://doi.org/10.1038/s42003-026-09808-3
关键词: 胶质母细胞瘤, 核糖体生物发生, 核仁, 表观遗传调控, KANSL2