Clear Sky Science · fr
KANSL2 localisé dans les nucléoles comme régulateur épigénétique de la biogenèse des ribosomes dans les cellules de glioblastome
Pourquoi cela compte pour le cancer du cerveau
Le glioblastome est l’une des formes les plus létales de cancer du cerveau, en partie parce que ses cellules sont particulièrement aptes à croître rapidement et à rebondir après les traitements. Cette étude révèle comment une protéine peu connue du noyau cellulaire, appelée KANSL2, aide ces cellules tumorales à suralimenter leurs usines internes de protéines, les ribosomes. En montrant que KANSL2 favorise directement la production de ribosomes, le travail met en évidence une nouvelle vulnérabilité potentielle qui pourrait être exploitée pour ralentir ou arrêter la croissance du glioblastome.
Activer un interrupteur de croissance caché
Les chercheurs ont d’abord cherché à savoir si KANSL2 est simplement présent dans les cellules de glioblastome ou s’il est activement lié à leur comportement agressif. En utilisant de larges jeux de données publics comparant les tissus tumoraux au cerveau normal, ils ont constaté que KANSL2 est systématiquement plus abondant dans le glioblastome. Les tumeurs présentant les niveaux les plus élevés de KANSL2 montraient également des signatures plus marquées de comportement « de type souche » — des cellules capables de s’auto-renouveler et de résister aux thérapies. L’analyse des gènes a en outre révélé qu’un KANSL2 élevé s’accompagne d’une activité augmentée des gènes impliqués dans la construction des ribosomes, suggérant que cette protéine pourrait être un interrupteur clé reliant stemness, croissance et production de ribosomes.
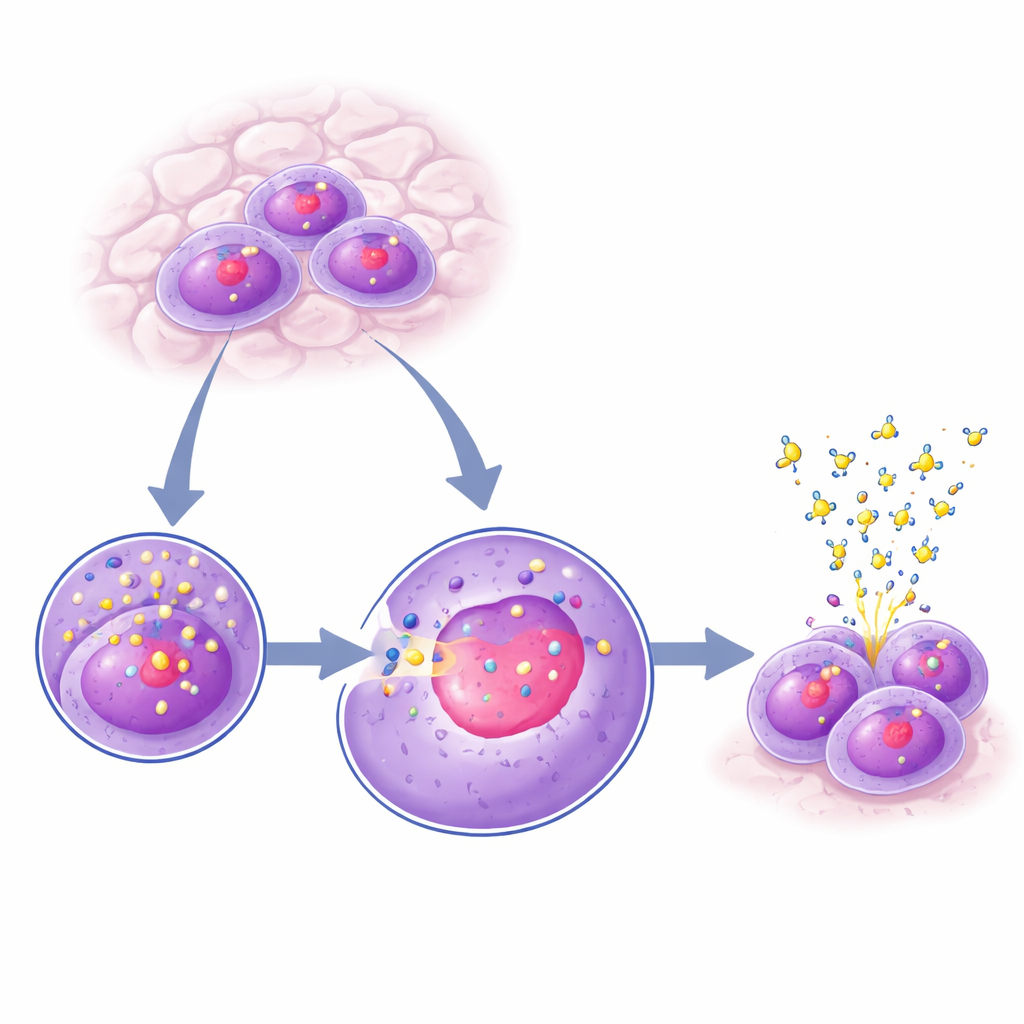
Localiser KANSL2 dans le centre de production de la cellule
À l’intérieur de chaque noyau cellulaire se trouve le nucléole, un point dense où naissent les ribosomes. En marquant différents types cellulaires et en observant au microscope, l’équipe a observé que KANSL2 n’est pas réparti uniformément dans le noyau : il se concentre dans le nucléole. Cet enrichissement est dynamique — il est maximal juste avant et juste après la réplication de l’ADN (phases G1 et G2 du cycle cellulaire) et plus faible pendant la réplication de l’ADN (phase S). Lorsque les chercheurs ont utilisé un médicament qui bloque spécifiquement l’enzyme responsable de la synthèse de l’ARN ribosomique, le composant central des ribosomes, la présence de KANSL2 dans le nucléole a fortement diminué, même si sa quantité totale dans la cellule n’a pas changé. Cela suggère que KANSL2 est attiré vers le nucléole lorsque la production de ribosomes est active et qu’il s’en éloigne lorsque ce processus est arrêté.
Des marques épigénétiques à la production de ribosomes
KANSL2 fait partie d’un ensemble plus large de protéines connues pour modifier le conditionnement de l’ADN, principalement en ajoutant de petites marques chimiques sur les protéines histones. Ces marques peuvent desserrer la structure de l’ADN, rendant les gènes plus accessibles à la lecture. Dans les cellules de glioblastome, la réduction du niveau de KANSL2 a entraîné une perte étendue de marques spécifiques sur l’histone H4, y compris au niveau des régions d’ADN qui codent pour l’ARN ribosomique. Par immunoprécipitation de la chromatine, les auteurs ont montré qu’un moindre KANSL2 s’accompagne d’une moindre acétylation au promoteur de l’ADN ribosomique, une région qui contrôle le démarrage de la transcription de l’ARN ribosomique. Conformément à cela, les cellules dépourvues de KANSL2 produisaient moins du transcript initial d’ARN ribosomique (45S) et de sa forme maturée (28S), tandis que la surexpression de KANSL2 augmentait ces espèces d’ARN et stimulait l’activité d’un rapporteur sous contrôle du promoteur de l’ADN ribosomique. Ensemble, ces résultats indiquent que KANSL2 agit comme un régulateur épigénétique qui augmente directement la machinerie d’ARN ribosomique.
Ondulations dans le système de production protéique
L’impact de KANSL2 dépassait quelques marqueurs moléculaires. Lorsque l’équipe a mesuré la synthèse de nouvelles protéines à l’aide d’une méthode de marquage des protéines fraîchement synthétisées, les cellules de glioblastome avec un KANSL2 réduit incorporaient nettement moins de marqueur, signe que leurs ribosomes étaient moins actifs. Le séquençage ARN en masse de sphéroïdes de glioblastome dérivés de patients — cultures tridimensionnelles qui reproduisent mieux les tumeurs — a montré que l’inhibition de KANSL2 entraînait une baisse généralisée des gènes nécessaires à l’assemblage des ribosomes, des protéines ribosomiques et du traitement de l’ARN. Au niveau cellulaire, les cellules avec un excès de KANSL2 croissaient plus vite, tandis que celles avec KANSL2 réduit ralentissaient leur division et s’accumulaient dans une phase précoce du cycle cellulaire, reliant ainsi directement la production de ribosomes à la prolifération.
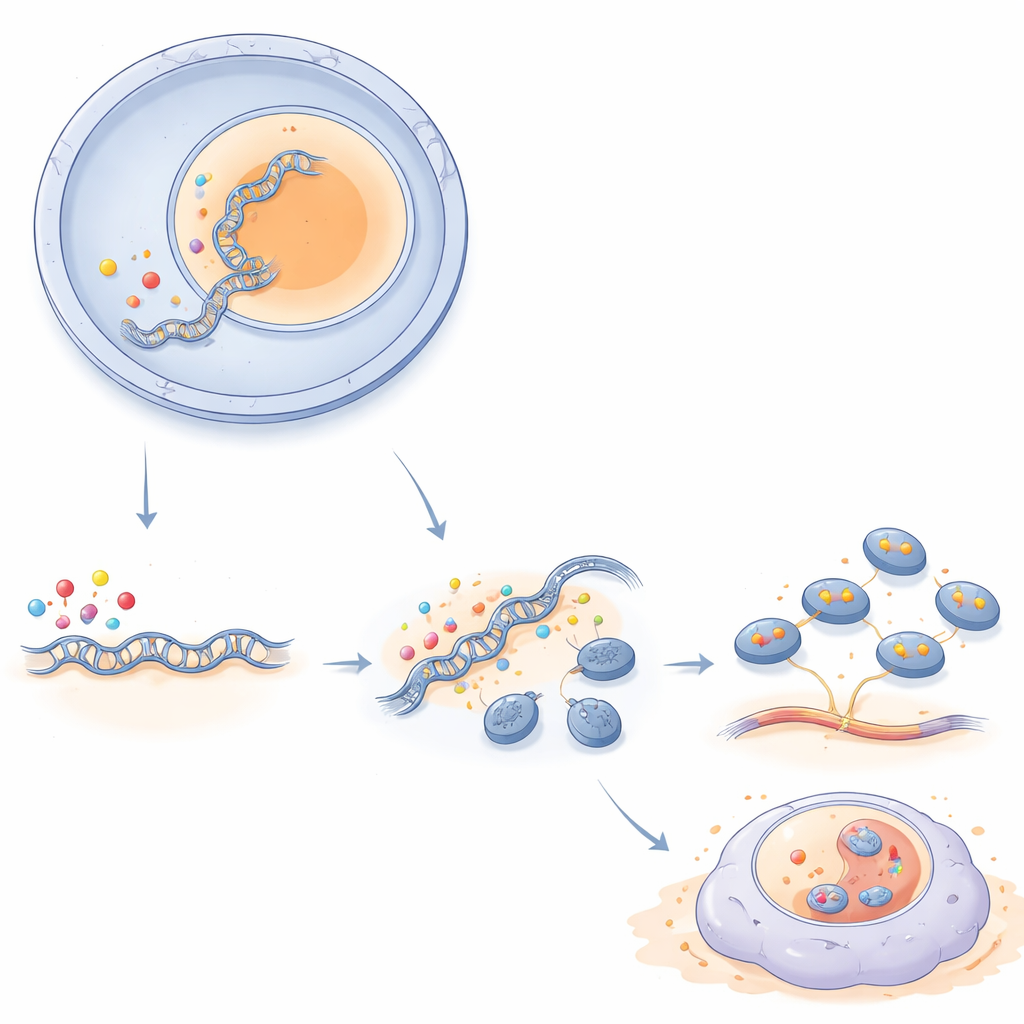
Une nouvelle vulnérabilité dans les tumeurs cérébrales récalcitrantes
En reliant KANSL2 au contrôle de la production de ribosomes, cette étude explique comment les cellules de glioblastome peuvent soutenir la lourde charge biosynthétique requise pour une croissance rapide et le maintien de propriétés de type souche. KANSL2 migre vers le nucléole pendant des fenêtres clés du cycle cellulaire, aide à ouvrir l’ADN ribosomique via l’acétylation des histones et augmente ainsi l’ARN ribosomique et la biogenèse des ribosomes. Parce que ces processus sont particulièrement hyperactifs dans les tumeurs agressives mais moins dans les cellules cérébrales normales, cibler KANSL2 ou ses voies associées pourrait offrir un moyen de freiner la croissance tumorale tout en épargnant les tissus sains, ce qui en fait un candidat intéressant pour de futures stratégies thérapeutiques.
Citation: Budnik, N., Canedo, L., Morellato, A.E. et al. Nucleoli-localized KANSL2 as an epigenetic regulator of ribosome biogenesis in glioblastoma cells. Commun Biol 9, 535 (2026). https://doi.org/10.1038/s42003-026-09808-3
Mots-clés: glioblastome, biogenèse des ribosomes, nucléole, régulation épigénétique, KANSL2