Clear Sky Science · it
KANSL2 localizzato nel nucleolo come regolatore epigenetico della biogenesi dei ribosomi nelle cellule di glioblastoma
Perché questo è importante per il cancro cerebrale
Il glioblastoma è una delle forme più letali di tumore cerebrale, in parte perché le sue cellule sono particolarmente abili nel crescere e riprendersi dopo il trattamento. Questo studio svela come una proteina poco studiata all’interno del nucleo cellulare, chiamata KANSL2, aiuti queste cellule tumorali a potenziare le loro “fabbriche” proteiche interne, i ribosomi. Mostrando che KANSL2 promuove direttamente la produzione di ribosomi, il lavoro individua un nuovo punto debole che potrebbe essere sfruttato per rallentare o arrestare la crescita del glioblastoma.
Accendere un interruttore di crescita nascosto
I ricercatori hanno prima chiesto se KANSL2 sia semplicemente presente nelle cellule di glioblastoma o se sia attivamente collegata al loro comportamento aggressivo. Utilizzando grandi set di dati pubblici che confrontano tessuto tumorale e cervello normale, hanno scoperto che KANSL2 è costantemente più abbondante nel glioblastoma. I tumori con i livelli più alti di KANSL2 mostravano anche segnature più forti di comportamento “simile a cellule staminali” — cellule capaci di auto-rinnovarsi e resistere alle terapie. L’analisi genica ha inoltre rivelato che l’aumento di KANSL2 è associato a una maggiore attività di geni coinvolti nella costruzione dei ribosomi, suggerendo che questa proteina possa essere un interruttore chiave che connette stemness, crescita e produzione di ribosomi.
Trovare KANSL2 nel nucleo produttivo della cellula
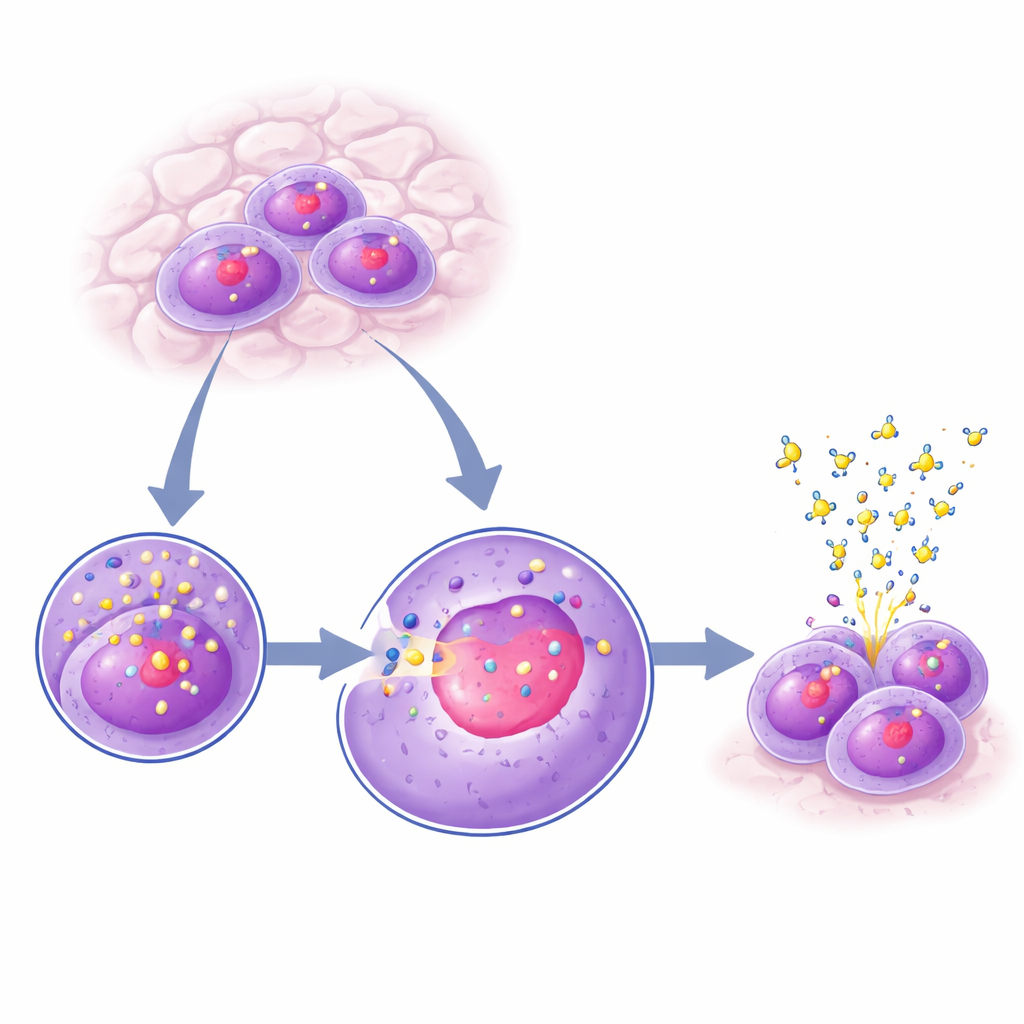
All’interno di ogni nucleo cellulare si trova il nucleolo, una zona densa dove nascono i ribosomi. Colorando diversi tipi cellulari e osservandoli al microscopio, il gruppo ha osservato che KANSL2 non è distribuita uniformemente nel nucleo: si concentra nel nucleolo. Questo arricchimento è dinamico — è massimo subito prima e dopo la duplicazione del DNA (fasi G1 e G2 del ciclo cellulare) e più debole durante la sintesi del DNA (fase S). Quando i ricercatori hanno usato un farmaco che blocca specificamente l’enzima responsabile della sintesi dell’RNA ribosomiale, il componente principale dei ribosomi, la presenza di KANSL2 nel nucleolo è diminuita drasticamente, pur senza cambiamenti nella quantità complessiva della proteina nella cellula. Questo suggerisce che KANSL2 viene attirata nel nucleolo quando la produzione di ribosomi è attiva e si allontana quando quel processo è spento.
Dai marchi epigenetici alla produzione di ribosomi
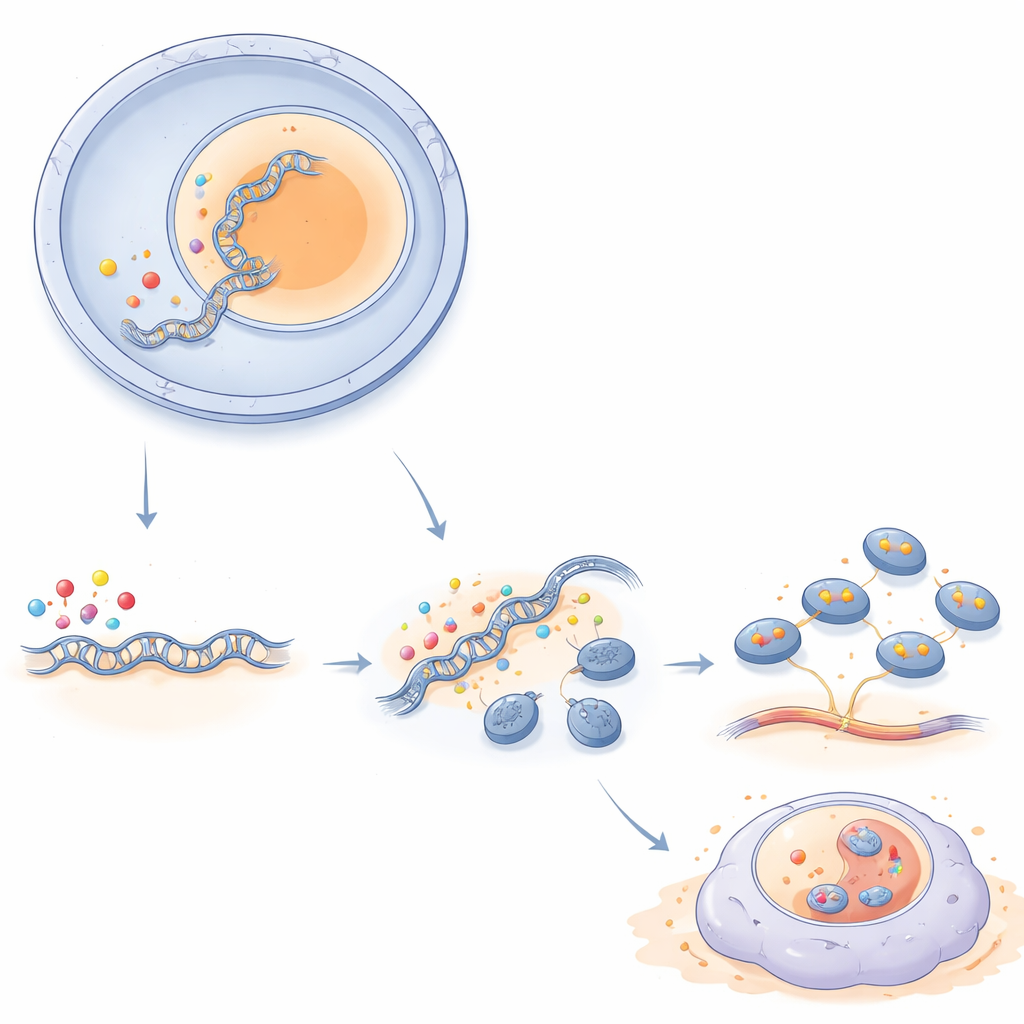
KANSL2 fa parte di un complesso più ampio di proteine noto per modificare il modo in cui il DNA è impacchettato, principalmente tramite l’aggiunta di piccole etichette chimiche sulle proteine istoniche. Questi marchi possono allentare il DNA, rendendo i geni più accessibili alla trascrizione. Nelle cellule di glioblastoma, la riduzione dei livelli di KANSL2 ha portato a una perdita diffusa di specifici marchi sugli istoni H4, incluso nelle regioni di DNA che codificano per l’RNA ribosomiale. Tramite immunoprecipitazione della cromatina, gli autori hanno mostrato che meno KANSL2 significa meno acetilazione nel promotore del DNA ribosomiale, una regione che controlla l’inizio della trascrizione dell’RNA ribosomiale. In coerenza con ciò, le cellule prive di KANSL2 hanno prodotto meno del trascritto iniziale dell’RNA ribosomiale (45S) e della sua forma processata (28S), mentre la sovraespressione di KANSL2 ha aumentato queste specie di RNA e potenziato l’attività di un reporter guidato dal promotore del DNA ribosomiale. Nel complesso, questi risultati indicano che KANSL2 agisce come un regolatore epigenetico che attiva direttamente la macchina dell’RNA ribosomiale.
Effetti a catena sul sistema di produzione proteica
L’impatto di KANSL2 è andato oltre pochi marcatori molecolari. Quando il gruppo ha misurato la sintesi proteica nuova usando un metodo di marcatura che etichetta le proteine appena sintetizzate, le cellule di glioblastoma con KANSL2 ridotto hanno incorporato significativamente meno marcatore, segno che i loro ribosomi erano meno attivi. Il sequenziamento dell’RNA totale di sferoidi di glioblastoma derivati da pazienti — colture tridimensionali che imitano meglio i tumori — ha mostrato che il silenziamento di KANSL2 ha causato un calo diffuso dei geni necessari per l’assemblaggio dei ribosomi, delle proteine ribosomiali e dell’elaborazione dell’RNA. A livello cellulare, le cellule con KANSL2 in eccesso crescevano più rapidamente, mentre quelle con KANSL2 inattivato rallentavano la divisione e si accumulavano in una fase precoce del ciclo cellulare, collegando direttamente la produzione di ribosomi alla proliferazione.
Una nuova vulnerabilità nei tumori cerebrali ostinati
Collegando KANSL2 al controllo della produzione dei ribosomi, questo studio spiega come le cellule di glioblastoma possano sostenere l’elevato carico biosintetico necessario per la rapida crescita e per il mantenimento delle proprietà simili a cellule staminali. KANSL2 si sposta nel nucleolo durante finestre chiave del ciclo cellulare, aiuta ad aprire il DNA ribosomiale tramite acetilazione degli istoni e in tal modo potenzia l’RNA ribosomiale e la biogenesi dei ribosomi. Poiché questi processi sono particolarmente iperattivi nei tumori aggressivi ma meno intensi nelle cellule cerebrali normali, mirare a KANSL2 o alle vie ad essa associate potrebbe offrire un modo per limitare la crescita tumorale risparmiando il tessuto sano, rendendola un candidata interessante per future strategie terapeutiche.
Citazione: Budnik, N., Canedo, L., Morellato, A.E. et al. Nucleoli-localized KANSL2 as an epigenetic regulator of ribosome biogenesis in glioblastoma cells. Commun Biol 9, 535 (2026). https://doi.org/10.1038/s42003-026-09808-3
Parole chiave: glioblastoma, biogenesi dei ribosomi, nucleolo, regolazione epigenetica, KANSL2