Clear Sky Science · de
KANSL2 im Nukleolus als epigenetischer Regulator der Ribosomenbiogenese in Glioblastomzellen
Warum das für Hirntumore wichtig ist
Das Glioblastom zählt zu den tödlichsten Formen von Hirntumoren, unter anderem weil seine Zellen außergewöhnlich gut wachsen und sich nach Therapien erholen können. Diese Studie enthüllt, wie ein vergleichsweise wenig untersuchtes Protein im Zellkern, KANSL2 genannt, diesen Tumorzellen hilft, ihre internen Proteinfabriken, die Ribosomen, zu beschleunigen. Indem gezeigt wird, dass KANSL2 direkt die Ribosomenproduktion fördert, weist die Arbeit auf eine neue Schwachstelle hin, die genutzt werden könnte, um das Wachstum von Glioblastomen zu verlangsamen oder zu stoppen.
Ein versteckter Wachstumsschalter wird aufgedreht
Die Forschenden fragten zunächst, ob KANSL2 nur in Glioblastomzellen vorhanden ist oder aktiv mit ihrem aggressiven Verhalten verknüpft ist. Mithilfe großer öffentlicher Datensätze, die Tumorgewebe mit normalem Gehirn vergleichen, stellten sie fest, dass KANSL2 in Glioblastomen durchgängig stärker exprimiert ist. Tumoren mit den höchsten KANSL2-Werten zeigten zudem stärkere Signale für ein "stammzellähnliches" Verhalten — Zellen, die sich selbst erneuern können und therapieresistent sind. Genanalysen zeigten außerdem, dass hohe KANSL2-Werte mit erhöhter Aktivität von Genen zur Ribosomenbildung einhergehen, was darauf hindeutet, dass dieses Protein ein zentraler Schalter sein könnte, der Stammzellmerkmale, Wachstum und Ribosomenproduktion verbindet.
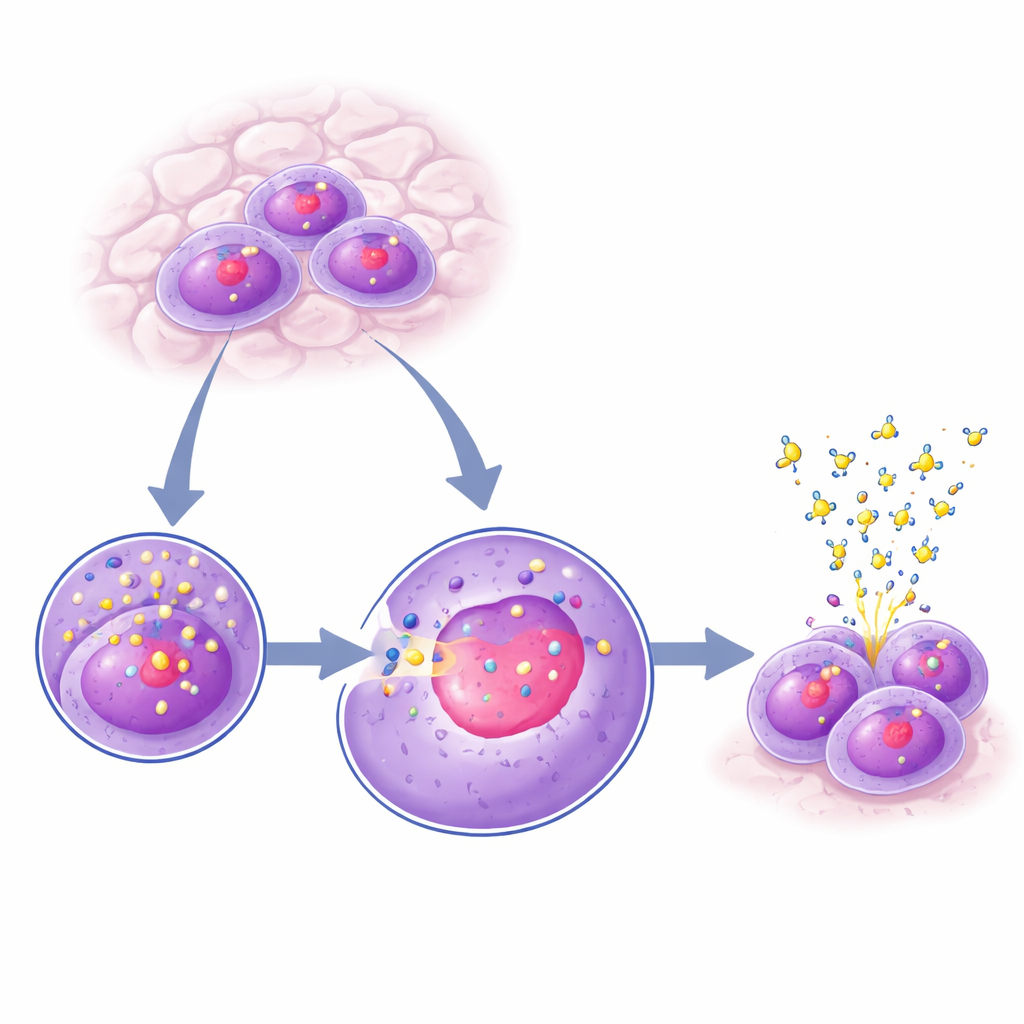
KANSL2 im Fabrikhub der Zelle aufspüren
Im Zellkern sitzt der Nukleolus, ein dichter Bereich, in dem Ribosomen entstehen. Durch Färbung verschiedener Zelltypen und Beobachtung unter dem Mikroskop fanden die Forschenden heraus, dass KANSL2 nicht gleichmäßig im Kern verteilt ist: Es reichert sich im Nukleolus an. Diese Anreicherung ist dynamisch — sie ist am stärksten kurz vor und nach der DNA-Replikation (in den G1- und G2-Phasen des Zellzyklus) und schwächer während der DNA-Synthese (S-Phase). Wenn die Forschenden ein Medikament einsetzten, das spezifisch das Enzym blockiert, das ribosomale RNA herstellt, dem zentralen Baustein der Ribosomen, nahm KANSL2s Präsenz im Nukleolus stark ab, obwohl seine Gesamtmenge in der Zelle gleich blieb. Das legt nahe, dass KANSL2 in den Nukleolus gezogen wird, wenn die Ribosomenproduktion aktiv ist, und ihn verlässt, wenn dieser Prozess heruntergefahren wird.
Von epigenetischen Markern zur Ribosomenleistung
KANSL2 ist Teil eines größeren Proteinverbands, der dafür bekannt ist, wie DNA verpackt wird, vor allem indem er kleine chemische Markierungen an Histonproteinen anbringt. Diese Markierungen können die DNA lockern und Gene leichter ablesbar machen. In Glioblastomzellen führte eine Verringerung von KANSL2 zu einem breiten Verlust bestimmter Histonmarken auf Histon H4, auch an den DNA-Abschnitten, die ribosomale RNA kodieren. Mit Chromatin-Immunpräzipitation zeigten die Autorinnen und Autoren, dass weniger KANSL2 mit geringerer Acetylierung am Promotor der ribosomalen DNA einhergeht — einer Region, die den Beginn der Transkription ribosomaler RNA steuert. Im Einklang damit produzierten Zellen ohne KANSL2 weniger des initialen ribosomalen RNA-Transkripts (45S) und dessen prozessierter Form (28S), während Überexpression von KANSL2 diese RNA-Spezies erhöhte und die Aktivität eines Reporters, der vom ribosomalen DNA-Promotor gesteuert wird, steigerte. Zusammengenommen deuten diese Ergebnisse darauf hin, dass KANSL2 als epigenetischer Regulator direkt die ribosomale RNA-Maschinerie hochfährt.
Auswirkungen auf das gesamte Proteinsystem
Die Auswirkungen von KANSL2 gingen über einzelne molekulare Marker hinaus. Als das Team die Neusynthese von Proteinen mittels einer Markierungsmethode maß, die frisch gebildete Proteine kennzeichnet, integrierten Glioblastomzellen mit reduziertem KANSL2 deutlich weniger Label — ein Hinweis darauf, dass ihre Ribosomen weniger aktiv waren. Bulk-RNA-Sequenzierung von patientenabgeleiteten Glioblastom-Sphäroiden — dreidimensionalen Kulturen, die Tumoren besser nachahmen — zeigte, dass das Stilllegen von KANSL2 zu einem breiten Rückgang von Genen führte, die für Ribosomenaufbau, ribosomale Proteine und RNA-Verarbeitung benötigt werden. Auf zellulärer Ebene wuchsen Zellen mit überschüssigem KANSL2 schneller, während Zellen mit reduziertem KANSL2 ihre Teilung verlangsamten und sich in einer frühen Zellzyklusphase anhäuften, was die Verbindung zwischen Ribosomenleistung und Proliferation verdeutlicht.
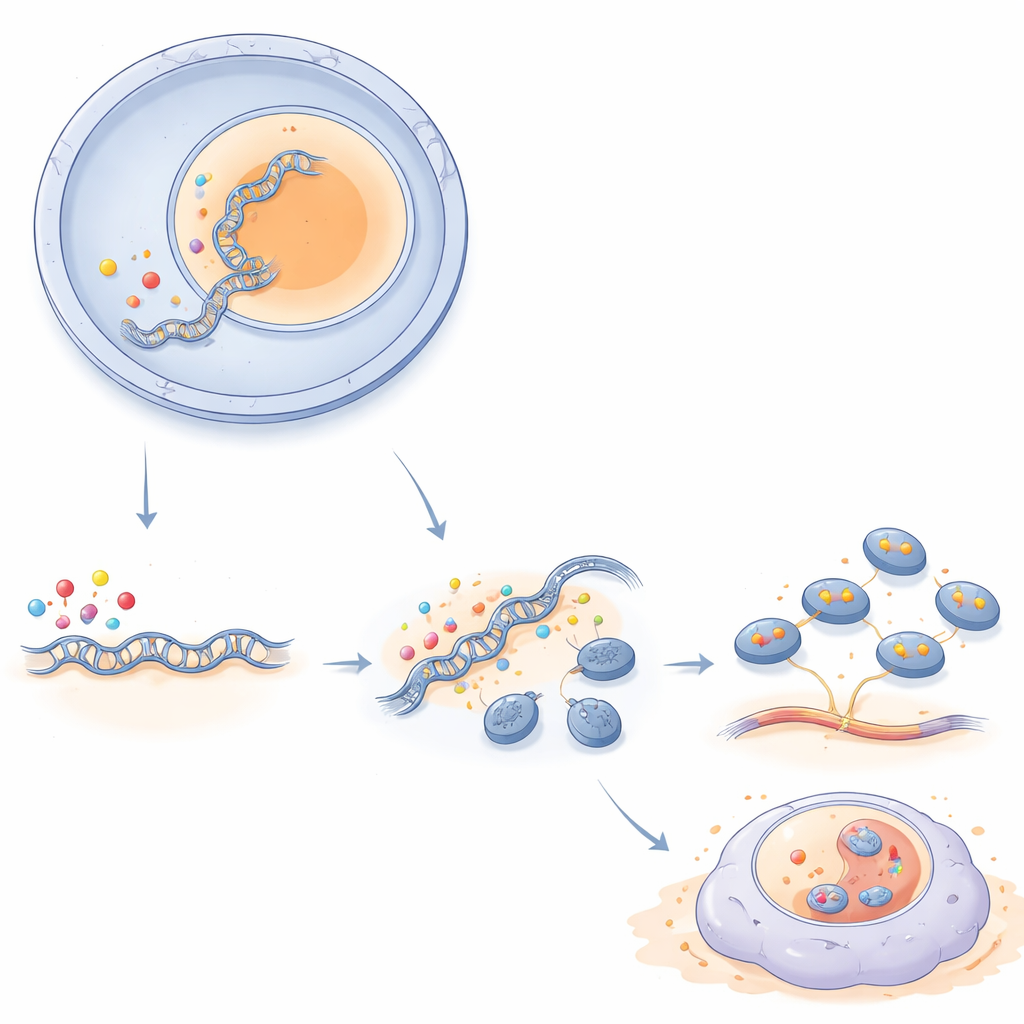
Eine neue Verwundbarkeit in hartnäckigen Hirntumoren
Indem die Studie KANSL2 mit der Kontrolle der Ribosomenproduktion verknüpft, erklärt sie, wie Glioblastomzellen die hohe biosynthetische Belastung aufrechterhalten können, die für schnelles Wachstum und die Erhaltung stammzellähnlicher Eigenschaften erforderlich ist. KANSL2 wandert während wichtiger Fenster des Zellzyklus in den Nukleolus, trägt durch Histonacetylierung zur Öffnung der ribosomalen DNA bei und steigert dadurch ribosomale RNA sowie die Ribosomenbiogenese. Da diese Prozesse in aggressiven Tumoren besonders hyperaktiv sind, aber in normalen Gehirnzellen weniger ausgeprägt, könnte die gezielte Blockade von KANSL2 oder seiner assoziierten Wege eine Möglichkeit bieten, das Tumorwachstum zu bremsen und dabei gesundes Gewebe zu schonen — was KANSL2 zu einem attraktiven Kandidaten für künftige therapeutische Ansätze macht.
Zitation: Budnik, N., Canedo, L., Morellato, A.E. et al. Nucleoli-localized KANSL2 as an epigenetic regulator of ribosome biogenesis in glioblastoma cells. Commun Biol 9, 535 (2026). https://doi.org/10.1038/s42003-026-09808-3
Schlüsselwörter: Glioblastom, Ribosomenbiogenese, Nukleolus, epigenetische Regulation, KANSL2