Clear Sky Science · zh
基于人工智能的单细胞棕榈酰化景观解析在胃癌中识别出一种多细胞预后程式
这项癌症研究为何重要
胃癌仍然是全球最致命的癌症之一,部分原因在于许多患者确诊较晚且对现有治疗反应不佳。该研究提出了一个看似简单却有重大意义的问题:一种加在蛋白质上的微小化学“标签”——棕榈酰化——如何重塑肿瘤内的多种细胞类型?这些信息能否被转化为强有力的预测工具,识别出病情更差、可能受益于新疗法的患者?
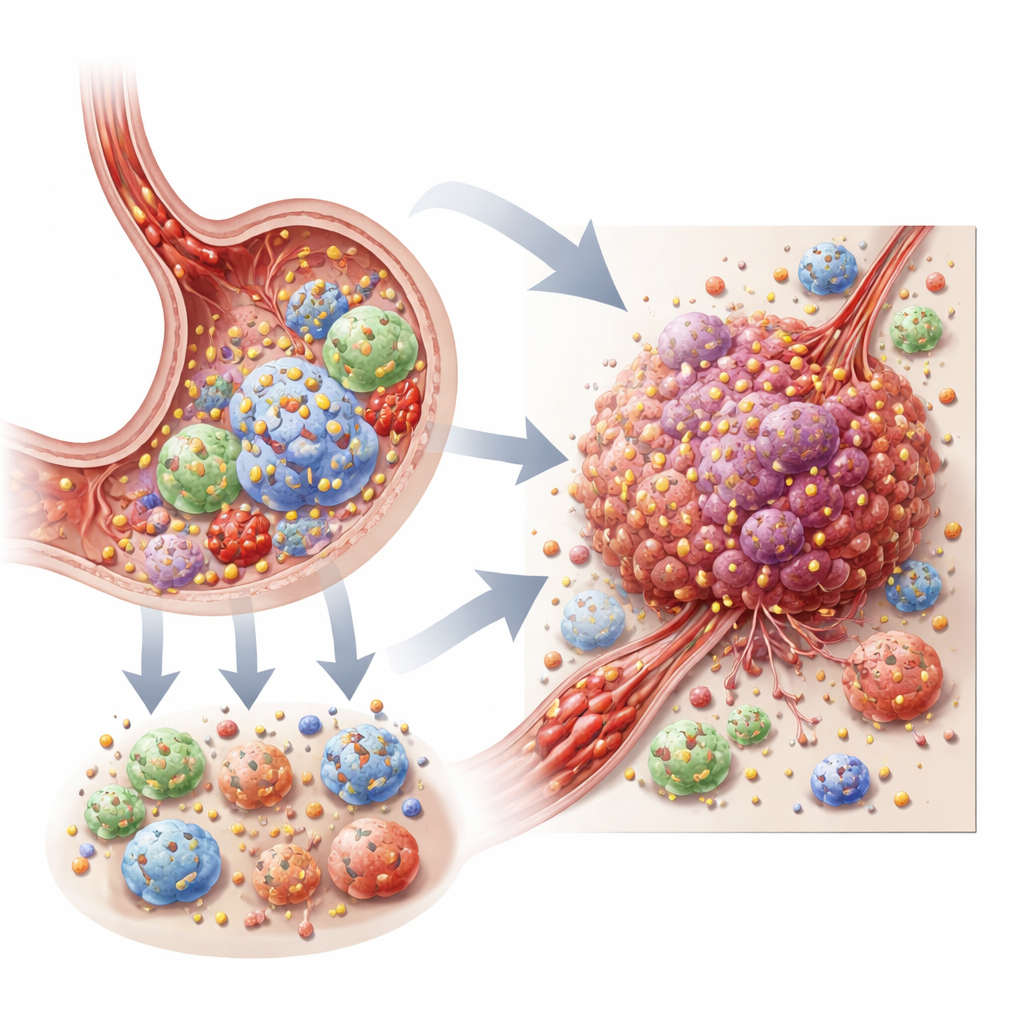
蛋白质上的化学开关
棕榈酰化是一种类似脂质的小分子附加修饰,细胞将其添加到许多蛋白质上,尤其是位于或靠近细胞膜的那些。添加或去除这一标签会改变蛋白质在细胞内的位置以及其信号强度,有点像调整天线的位置。早期研究提示棕榈酰化有助于胃肿瘤逃避免疫监视并抵抗化疗,但这些研究多集中在单个蛋白或对整个肿瘤的平均信号上。当前工作则利用人工智能和大规模测序,从单细胞层面观察棕榈酰化相关活动如何塑造由癌细胞、免疫细胞、血管和支持性结缔组织组成的整个肿瘤“生态系统”。
逐个细胞解读肿瘤
研究者分析了来自25例胃肿瘤中近12万单个细胞的基因活性,并将其与显示每个细胞在组织切片中位置的空间图谱以及多组基于整体样本的大型患者队列相结合。利用机器学习工具,他们为每个细胞计算了一个棕榈酰化评分,然后检视哪些细胞类型倾向于“棕榈酰化高”。结果发现,一类得分高的独特癌细胞群在已发生转移的肿瘤中显著富集。这些细胞提升了脂质代谢和关键生长通路,同时表现出既高度侵袭又更易发生程序性细胞死亡的奇特组合,提示一种有利于扩散的风险—回报权衡。
肿瘤内部的敌对邻域
超越癌细胞本身,团队发现棕榈酰化高的状态也出现在特定类型的免疫细胞、成纤维细胞和血管内皮细胞中,这些细胞聚集在肿瘤的低氧区。某些巨噬细胞和树突状细胞在棕榈酰化高时,伴随强烈的信号去抑制攻击性的T细胞并促进有利于肿瘤的炎症;这些细胞每有一点增加,患者死亡风险就显著上升。同样,棕榈酰化高的成纤维细胞在肿瘤周围形成僵硬的纤维化屏障,而棕榈酰化高的血管内皮细胞则与富含生长因子的区域一致,助长新生但脆弱的血管。共同作用下,这些协调的细胞状态形成了一个自我强化的免疫抑制且促进转移的生态位。
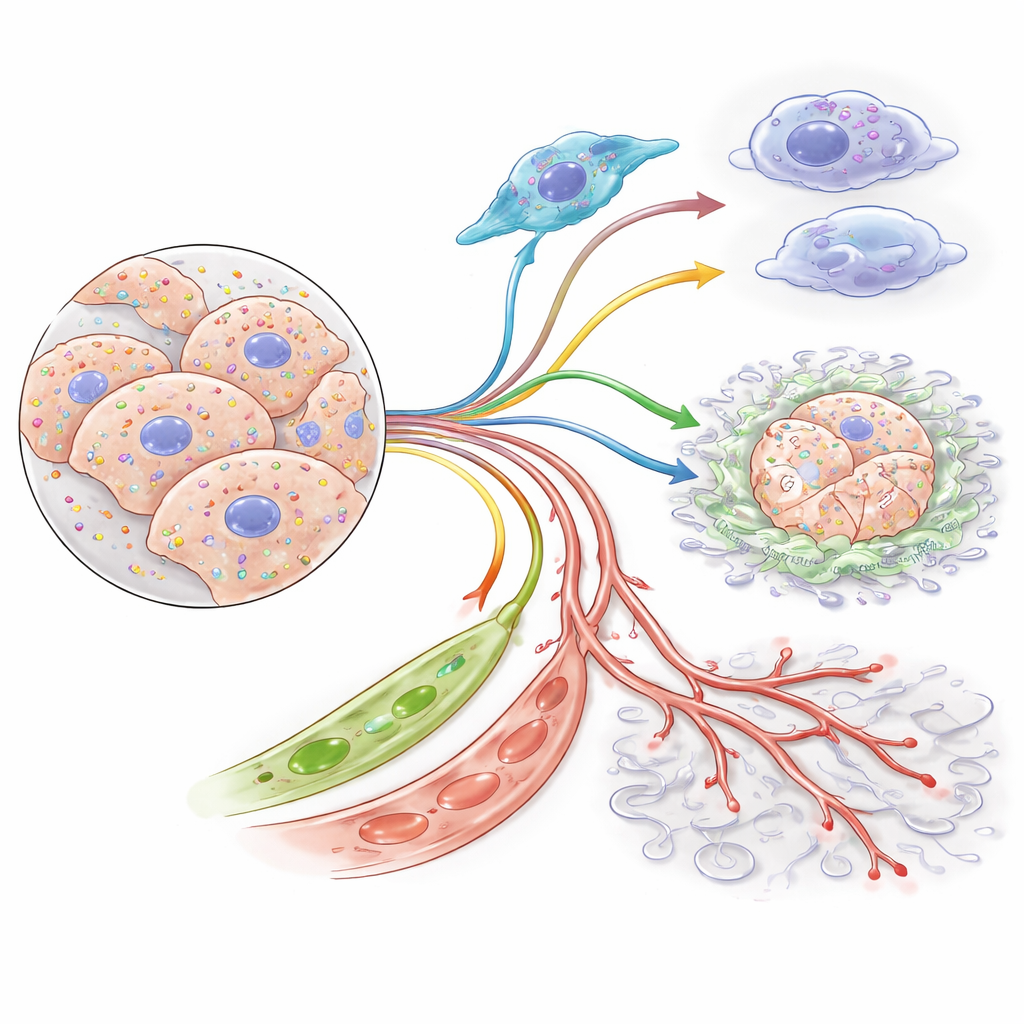
可预测患者结局的基因特征
由于在临床上逐个细胞检测肿瘤并不现实,作者将他们的发现提炼为一组包含87个基因的“特征签名”,用于从常规肿瘤样本中捕捉这一多细胞棕榈酰化程式。将该评分应用于超过1200名来自多个数据集的患者后,它能明确将人群分为高风险和低风险组,二者的5年生存率相差30个百分点以上,即使在调整肿瘤分期后仍然显著。高风险肿瘤表现出与依赖特定生长和应激通路一致的DNA突变、DNA甲基化改变和蛋白激活模式。随后进行的计算药物筛选指出了该系统的薄弱环节,包括帮助保持过度活跃信号蛋白稳定和功能的HSP90及PI3K/MAPK网络组分。
新的驱动因子与治疗路径
在与这一危险程式相关的众多基因中,团队挑选了一个名为SH3BGRL的基因进行更深入的实验验证。在细胞培养和小鼠模型中,下调SH3BGRL使胃癌细胞增殖减慢、侵袭能力下降并增加细胞死亡;上调则产生相反效果。SH3BGRL表达降低的肿瘤形成了更小的肿块,分裂细胞更少、死亡细胞更多,支持其作为棕榈酰化相关网络中功能性驱动因子的角色。这些结果表明,针对SH3BGRL本身或其关联通路,可能有助于瓦解由棕榈酰化高状态支撑的致命生态系统。
这对患者意味着什么
简而言之,这项研究表明一个单一的生化主题——蛋白质棕榈酰化——有助于协调胃癌中的多种“祸源”:侵袭性的肿瘤细胞、抑制性的免疫细胞、硬化的结缔组织和过度生长的血管。通过将这一程式以基因评分的形式捕捉,医生未来可能更准确地预测哪些患者面临更大风险,并将他们匹配到阻断肿瘤关键依赖性的治疗方案。尽管仍需前瞻性临床试验和对棕榈酰化蛋白更直接的测量,但这项工作将这种微妙的脂质修饰定位为预测结局和设计联合治疗的有希望的切入点,特别是在一种历来难治的癌症中。
引用: Xu, J., Hu, Y., Qiao, Q. et al. AI-enabled single-cell dissection of the palmitoylation landscape identifies a multicellular prognostic program in gastric cancer. npj Precis. Onc. 10, 160 (2026). https://doi.org/10.1038/s41698-026-01359-4
关键词: 胃癌, 棕榈酰化, 肿瘤微环境, 单细胞RNA测序, 癌症预后