Clear Sky Science · ar
تفكيك مستوى بالميتويلاشن على مستوى الخلية الواحدة بتمكين الذكاء الاصطناعي يحدد برنامجًا تنبؤيًا متعدد الخلايا في سرطان المعدة
لماذا تهم هذه الدراسة عن السرطان
لا يزال سرطان المعدة من بين أكثر أنواع السرطان فتكًا على مستوى العالم، ويرجع ذلك جزئيًا إلى أن العديد من المرضى يُشخَّصون في مراحل متأخرة ولا يستجيبون جيدًا للعلاجات الحالية. تطرح هذه الدراسة سؤالًا يبدو بسيطًا لكنه ذو تداعيات كبيرة: كيف يعيد وسم كيميائي طفيف يضاف إلى البروتينات — يُسمى بالميتويلاشن — تنظيم أنواع الخلايا المتعددة داخل الورم، وهل يمكن تحويل هذه المعلومات إلى متنبئ قوي يحدد أي المرضى قد تكون نتائجهم سيئة وقد يستفيدون من علاجات جديدة؟
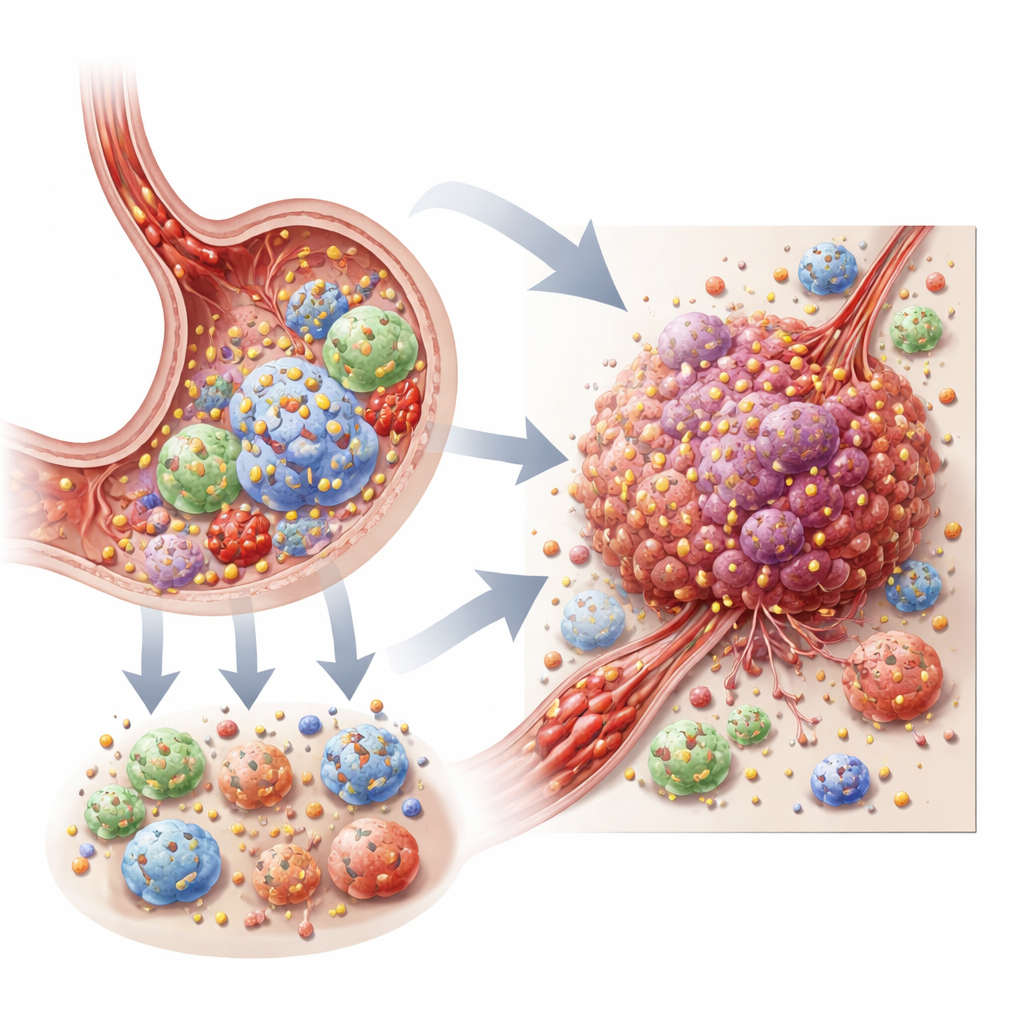
مفتاح كيميائي على البروتينات
البالميتويلاشن هو ارتباط صغير شبيه بالدهون تضعه الخلايا على العديد من البروتينات، خصوصًا تلك الموجودة في أو قرب أغشية الخلايا. يمكن أن يغير إضافة هذا الوسم أو إزالته مكان تواجد البروتين داخل الخلية ومدى قوة إشارته، أشبه بتغيير موضع هوائي استقبال. أشارت أعمال سابقة إلى أن البالميتويلاشن يساعد أورام المعدة على الهروب من الجهاز المناعي ومقاومة العلاج الكيميائي، لكن هذه الدراسات ركزت على بروتينات فردية أو على إشارات مجمعة عبر أورام كاملة. تستخدم الدراسة الحالية بدلاً من ذلك الذكاء الاصطناعي والتسلسل واسع النطاق لرؤية كيفية تشكيل نشاط المرتبط بالبالميتويلاشن لـ"نظام البيئة" الكامل للورم — خلية بخلاياها — بما في ذلك الخلايا السرطانية والخلايا المناعية والأوعية الدموية والأنسجة الضامة المساندة.
قراءة الأورام خلية خلية
حلل الباحثون نشاط الجينات في ما يقرب من 120000 خلية مفردة مأخوذة من 25 ورمًا معديًا، ودمجوا ذلك مع خرائط مكانية تُظهر موضع كل خلية في شرائح نسيجية، بالإضافة إلى مجموعات مرضى كبيرة مقاسة بطريقة مجمعة. باستخدام أدوات تعلم آلي، حسبوا درجة بالميتويلاشن لكل خلية، ثم تحققوا من أنواع الخلايا التي تميل لأن تكون "عالِية البالميتويلاشن". وجدوا أن مجموعة مميزة من الخلايا السرطانية ذات الدرجات العالية كانت غنية بشكل كبير في الأورام النقيليّة — تلك التي انتشرت بالفعل. هذه الخلايا رفعت من استقلاب الدهون ومسارات نمو رئيسية وأظهرت مزيجًا غريبًا من كونها شديدة الغزو لكنها أيضًا أكثر ميلاً للموت الخلوي المبرمج، ما يشير إلى مقايضة مخاطرة–مكافأة تُفضّل الانتشار.
حيٍّ عدائي داخل الورم
عند النظر إلى ما وراء الخلايا السرطانية نفسها، اكتشف الفريق أن حالات عالية البالميتويلاشن ظهرت في أنواع محددة من الخلايا المناعية والليفية وخلايا بطانة الأوعية الدموية التي تتجمع معًا في جيوب منخفضة الأكسجين داخل الورم. بعض البلعميات والخلايا الشجرية، عند ارتفاع مستوى البالميتويلاشن فيها، ارتبطت بإشارات قوية تُسكت الخلايا التائية المهاجمة وتعزز الالتهاب المؤيد للورم؛ كل زيادة متواضعة في تواجدها ارتبطت بارتفاع حاد في خطر الوفاة. وبالمثل، شكلت الخلايا الليفية عالية البالميتويلاشن حواجز ليفية صلبة حول الأورام، وتوافقت خلايا بطانة الأوعية ذات البالميتويلاشن العالي مع مناطق غنية بعوامل النمو التي تغذي أوعية دموية جديدة وهشة. معًا، شكلت هذه الحالات الخلوية المنسقة موئلًا معزِّزًا ذاتيًا، مثبطًا للمناعة ومُعززًا للنقائل.
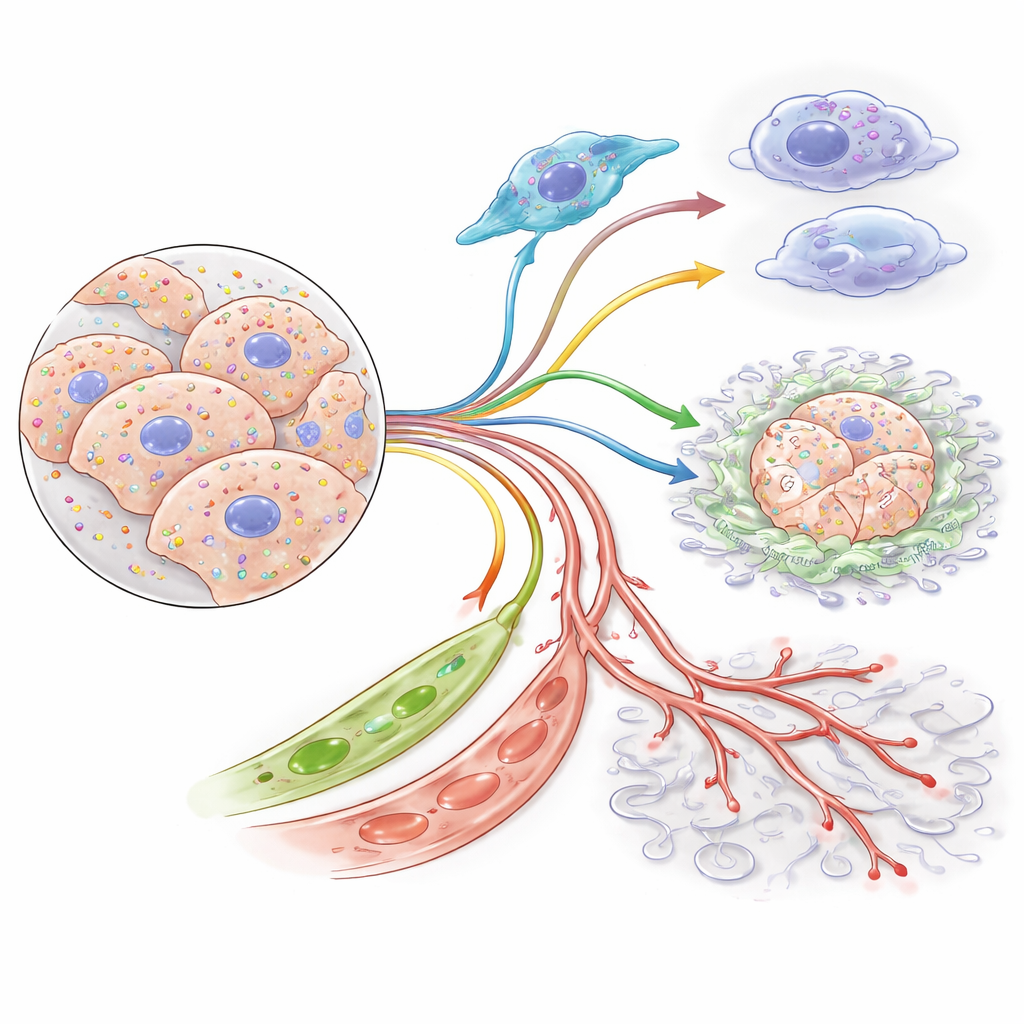
توقيع جيني يتنبأ بمآل المريض
نظرًا لأن فحص كل خلية في الورم بشكل روتيني غير عملي في العيادة، صاغ المؤلفون استنتاجاتهم في "توقيع" جيني مكوَّن من 87 جينًا يلتقط البرنامج متعدد الخلايا المرتبط بالبالميتويلاشن من عينات أورام عادية. عند تطبيقه على أكثر من 1200 مريض عبر مجموعات بيانات متعددة، فصلت هذه الدرجة بوضوح الأفراد إلى مجموعات عالية ومنخفضة المخاطر اختلفت فيها نسبة البقاء لخمس سنوات بأكثر من ثلاثين نقطة مئوية، حتى بعد احتساب مرحلة الورم. أظهرت الأورام عالية المخاطر نمطًا من طفرات الحمض النووي وتغيرات في مثيلة الحمض النووي وتفعيل بروتيني يتوافق مع الاعتماد الكبير على مسارات نمو وإجهاد معينة. أشارت فحوصات أدوية حاسوبية بعد ذلك إلى نقاط ضعف في هذا النظام، بما في ذلك مكونات شبكات HSP90 وPI3K/MAPK التي تساعد في الحفاظ على استقرار البروتينات ذات الإشارات المفرطة ووظيفتها.
عامل جديد وسبل نحو العلاج
من بين العديد من الجينات المرتبطة بهذا البرنامج الخطر، اختار الفريق واحدًا اسمه SH3BGRL لاختبارات تجريبية أعمق. في ثقافات الخلايا ونماذج الفأر، أدى خفض تعبير SH3BGRL إلى بطء نمو خلايا سرطان المعدة، وانخفاض غزوها، وزيادة موت الخلايا؛ بينما أدى رفعه إلى التأثير المعاكس. شكلت الأورام ذات مستويات SH3BGRL المخفضة كتلًا أصغر بها خلايا قلية الانقسام ومزيد من الخلايا الميتة، مما يدعم دورها كسائق وظيفي داخل الشبكة المرتبطة بالبالميتويلاشن. تشير هذه النتائج إلى أن استهداف SH3BGRL نفسه، أو مساراته المرتبطة، قد يساعد في تفكيك النظام البيئي القاتل الذي تدعمه حالات عالية البالميتويلاشن.
ما الذي يعنيه هذا للمرضى
بعبارات بسيطة، تظهر هذه الدراسة أن موضوعًا كيميائيًا حيويًّا واحدًا — بالميتويلاشن البروتينات — يساعد في تنسيق عدة "جهات فاعلة سيئة" في سرطان المعدة: خلايا ورمية عدوانية، خلايا مناعية كابحة، نسيج ضام يتصلب، وأوعية دموية متضخمة. من خلال التقاط هذا البرنامج في درجة مبنية على الجينات، قد يتمكن الأطباء يومًا ما من التنبؤ بشكل أفضل بمن يواجهون أعظم المخاطر ومطابقتهم مع علاجات تحجب الاعتماد الرئيسي للأورام. بينما لا تزال هناك حاجة إلى تجارب سريرية مستقبلية وقياس أكثر مباشرة للبروتينات المبالميتوية، فإن الدراسة تضع هذا الوسم الدهني الدقيق كمقبض واعد لكل من التنبؤ بالنتائج وتصميم علاجات تركيبية في سرطان يصعب علاجه بشكل ملحوظ.
الاستشهاد: Xu, J., Hu, Y., Qiao, Q. et al. AI-enabled single-cell dissection of the palmitoylation landscape identifies a multicellular prognostic program in gastric cancer. npj Precis. Onc. 10, 160 (2026). https://doi.org/10.1038/s41698-026-01359-4
الكلمات المفتاحية: سرطان المعدة, البالميتويلاشن, البيئة الدقيقة للورم, تسلسل RNA أحادي الخلية, تكهنات السرطان