Clear Sky Science · ja
単一細胞解析とAIが明らかにしたパルミトイル化の景観:胃がんにおける多細胞予後プログラムの同定
このがん研究が重要な理由
胃(胃がん)は依然として世界で最も致死率の高いがんの一つであり、その一因は多くの患者が進行してから診断され、現行治療に十分に反応しないことにあります。本研究は一見単純だが意味深い問いを立てます:タンパク質に付加される微細な化学的「タグ」であるパルミトイル化は、腫瘍内の多様な細胞群をどのように再編成し、その情報を使って予後不良な患者を予測し、新しい治療の恩恵を受けうる患者を特定できるか?
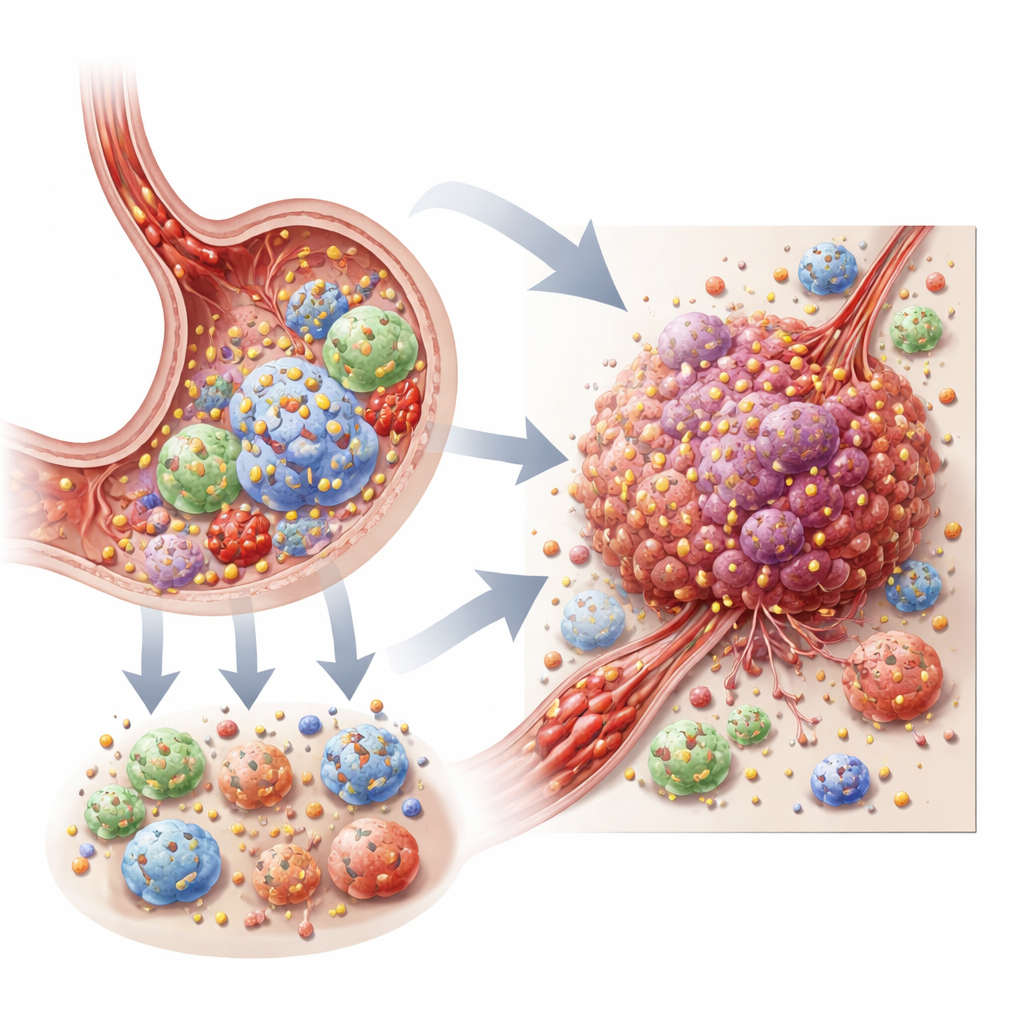
タンパク質に付く化学的スイッチ
パルミトイル化は多くのタンパク質、特に細胞膜付近にあるものに付く脂肪様の小さな付加修飾です。このタグの付加・除去は、アンテナの位置を変えるようにタンパク質の細胞内局在やシグナル強度を変え得ます。これまでの研究は、パルミトイル化が胃腫瘍の免疫逃避や化学療法耐性に寄与することを示唆していましたが、それらは個々のタンパク質や腫瘍全体の平均信号に注目したものでした。本研究では代わりに人工知能と大規模シーケンスを用いて、細胞ごとにパルミトイル化関連の活動ががん細胞、免疫細胞、血管、支持結合組織を含む腫瘍の「生態系」をどのように形作るかを明らかにします。
腫瘍を一細胞ずつ読む
研究者らは25個の胃腫瘍から採取した約12万個の個々の細胞の遺伝子発現を解析し、それぞれの細胞が組織切片のどこに位置するかを示す空間マップや、大規模な患者コホートのバルクデータと結び付けました。機械学習ツールを用いて各細胞にパルミトイル化スコアを算出し、どの種類の細胞が「パルミトイル化高」になりやすいかを調べました。その結果、高スコアを示す明確ながん細胞群が転移性腫瘍、すなわち既に広がっている腫瘍で強く濃縮していることが分かりました。これらの細胞は脂質代謝と主要な増殖経路を活性化し、高い浸潤性を示す一方でプログラム化された細胞死に陥りやすいという興味深い組み合わせを示しており、転移を促すリスクとリターンのトレードオフを示唆しています。
腫瘍内部の敵対的な近隣環境
がん細胞自身を越えて見ていくと、パルミトイル化高の状態は特定の免疫細胞、線維芽細胞、血管内皮細胞などにも現れ、それらが腫瘍の低酸素ポケットに集積していることが分かりました。特定のマクロファージや樹状細胞はパルミトイル化高のとき、攻撃するT細胞を抑え腫瘍に有利な炎症を促す強いシグナルと結び付き、その存在がわずかに増えるだけで死亡リスクが急増しました。同様に、パルミトイル化高の線維芽細胞は腫瘍の周囲に硬く線維化した障壁を形成し、パルミトイル化高の血管内皮細胞は成長因子に富む領域と整合して新生で脆弱な血管を育みます。これらの協調した細胞状態は、自己強化的で免疫抑制的、かつ転移促進的なニッチを形成していました。
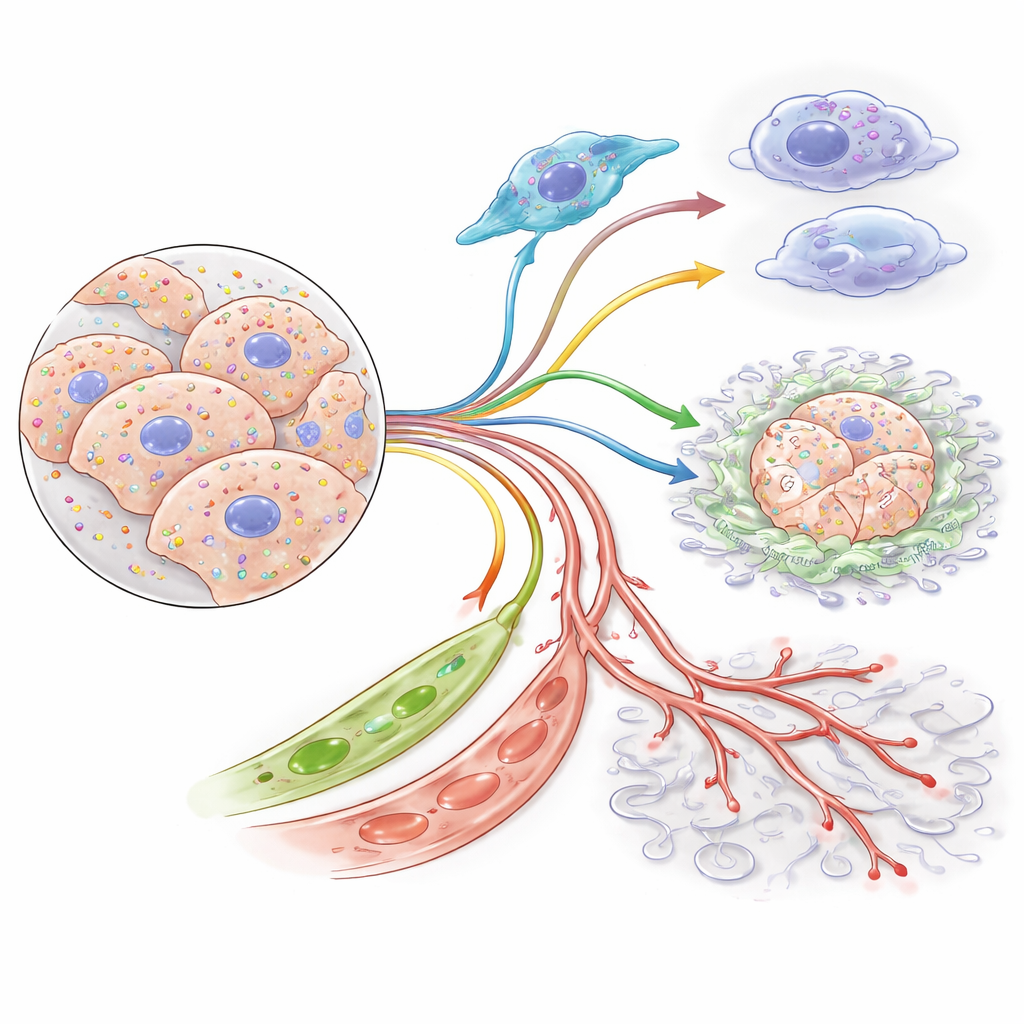
患者転帰を予測する遺伝子署名
臨床で腫瘍の個々の細胞すべてを定期的に調べることは現実的でないため、著者らは通常の腫瘍試料から多細胞のパルミトイル化プログラムを捉える87遺伝子の「署名」に研究結果を集約しました。これを複数のデータセットで1,200人以上の患者に適用すると、このスコアは患者を高リスク群と低リスク群に明確に分け、腫瘍ステージを考慮しても5年生存率は30パーセントポイント以上の差が出ました。高リスク腫瘍は特定の成長やストレス経路に依存していることを示すDNA変異、DNAメチル化の変化、タンパク質活性化のパターンを示しました。計算機上の薬剤スクリーニングは、このシステムの弱点としてHSP90やPI3K/MAPKネットワークの構成要素など、過活動なシグナルタンパク質の安定化や機能維持を支える部分を指摘しました。
新たなドライバーと治療への道筋
この危険なプログラムに関連する多くの遺伝子の中で、チームはSH3BGRLという遺伝子を選んで実験的に詳しく検証しました。細胞培養やマウスモデルでは、SH3BGRLの発現を下げると胃がん細胞の増殖が遅くなり、浸潤が減り、細胞死が増加しました。一方、発現を上げると逆の効果が見られました。SH3BGRLが低い腫瘍は分裂細胞が少なく死滅細胞が多い小さな塊を形成し、パルミトイル化関連ネットワーク内で機能的なドライバーとしての役割を支持します。これらの結果は、SH3BGRL自体やその連結経路を標的にすることで、パルミトイル化高の状態が支える致命的な生態系を解体できる可能性を示唆します。
患者にとっての意味
平たく言えば、本研究は一つの生化学的テーマ――タンパク質のパルミトイル化――が、攻撃的ながん細胞、抑制的な免疫細胞、硬化する結合組織、過剰に発達した血管といった複数の「悪役」を協調させることを示しています。このプログラムを遺伝子ベースのスコアで捉えることで、医師は将来的にリスクの高い患者をより正確に予測し、腫瘍の主要な依存性をブロックする治療に割り当てる可能性があります。前向きな臨床試験やパルミトイル化タンパク質のより直接的な測定がまだ必要ですが、この微細な脂質修飾は予後予測と併用療法設計の両面で有望な手掛かりとなる位置づけができます。
引用: Xu, J., Hu, Y., Qiao, Q. et al. AI-enabled single-cell dissection of the palmitoylation landscape identifies a multicellular prognostic program in gastric cancer. npj Precis. Onc. 10, 160 (2026). https://doi.org/10.1038/s41698-026-01359-4
キーワード: 胃がん, パルミトイル化, 腫瘍微小環境, 単一細胞RNAシーケンシング, がん予後