Clear Sky Science · zh
TCF4 三核苷酸重复扩增驱动费克斯(Fuchs)角膜内皮营养不良中独特的蛋白质组学特征
为何这类眼病重要
随着年龄增长,导致需要角膜移植的最常见原因之一是称为费克斯角膜内皮营养不良的疾病。在这种疾病中,角膜的内表面——本应清晰光滑的窗面——出现微小隆起并发生肿胀,从而使视力模糊。医生早已知道基因 TCF4 中一段重复的 DNA 序列大幅增加罹患费克斯的风险,但他们并不清楚这种额外的遗传“口吃”如何实际损害维持角膜透明的细胞。这项研究通过直接观察受影响细胞内的蛋白质,试图把那一处神秘的 DNA 变化与眼睛的日常功能联系起来。
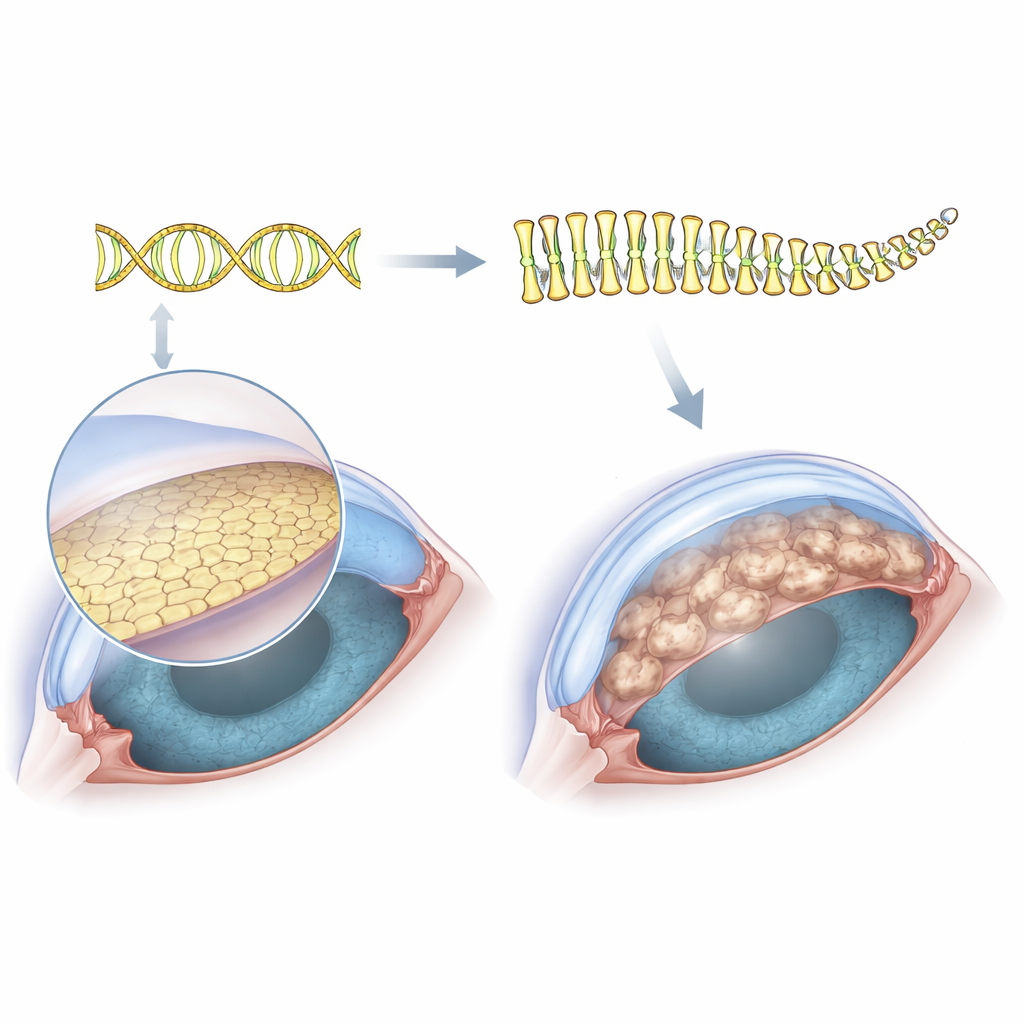
观察角膜隐秘的“劳动力”
角膜的透明性依靠其内表面的一层细胞——角膜内皮——来维持。这些细胞位于一层薄薄的支撑膜上,不断将组织内的液体泵出以保持透明。在费克斯营养不良中,这层内膜会布满类似疣状的突起(称为 guttae),细胞逐渐死亡,角膜随之肿胀并浑浊。由于这层细胞极薄,从患者处收集到足够用于全面研究其蛋白产物的材料在技术上非常困难。为了解决这一问题,研究者使用了一株来自一位携带扩增 TCF4 DNA 重复的费克斯患者的永生化细胞系,然后用 CRISPR 基因编辑精确切除该扩增片段,建立了一个几乎完美配对的“前后对照”细胞体系。
关闭重复并观察蛋白质的变化
在移除扩增的 DNA 重复后,编辑过的细胞在显微镜下看起来正常:它们保持典型的多边形形状并形成整齐的细胞层,表明单纯抹去该重复并不损害基本的细胞结构。真正的差异在研究团队用一种灵敏的质谱方法并行标记和比较样本来测量数千种蛋白质时显现出来。原始细胞与编辑细胞之间有 201 种蛋白在丰度上发生了统计学上显著的改变。有些蛋白变多,有些变少,但它们合在一起形成了一个独特的分子指纹,在对数据进行聚类和可视化时清楚地区分了“重复存在”与“重复删除”两种状态。
角膜支架和细胞“抓附”受扰乱
当研究人员按功能将这些变化蛋白分组时,两大主题突出。许多在删除重复后下降的蛋白参与构建和组织细胞外基质——位于细胞下方的网状支架——以及细胞如何附着于该支架和彼此之间。这些包括富含胶原的结构成分以及连接细胞表面与周围基质的蛋白。由于过多或异常的基质是费克斯病中 guttae 的标志性表现,这一模式表明 TCF4 的重复扩增在主动驱动角膜内表面过度构建和形态异常。删除该重复后相关基质与黏附蛋白减少的事实,支持了这一遗传改变与患者角膜上出现物理性小疙瘩之间的直接因果关系。
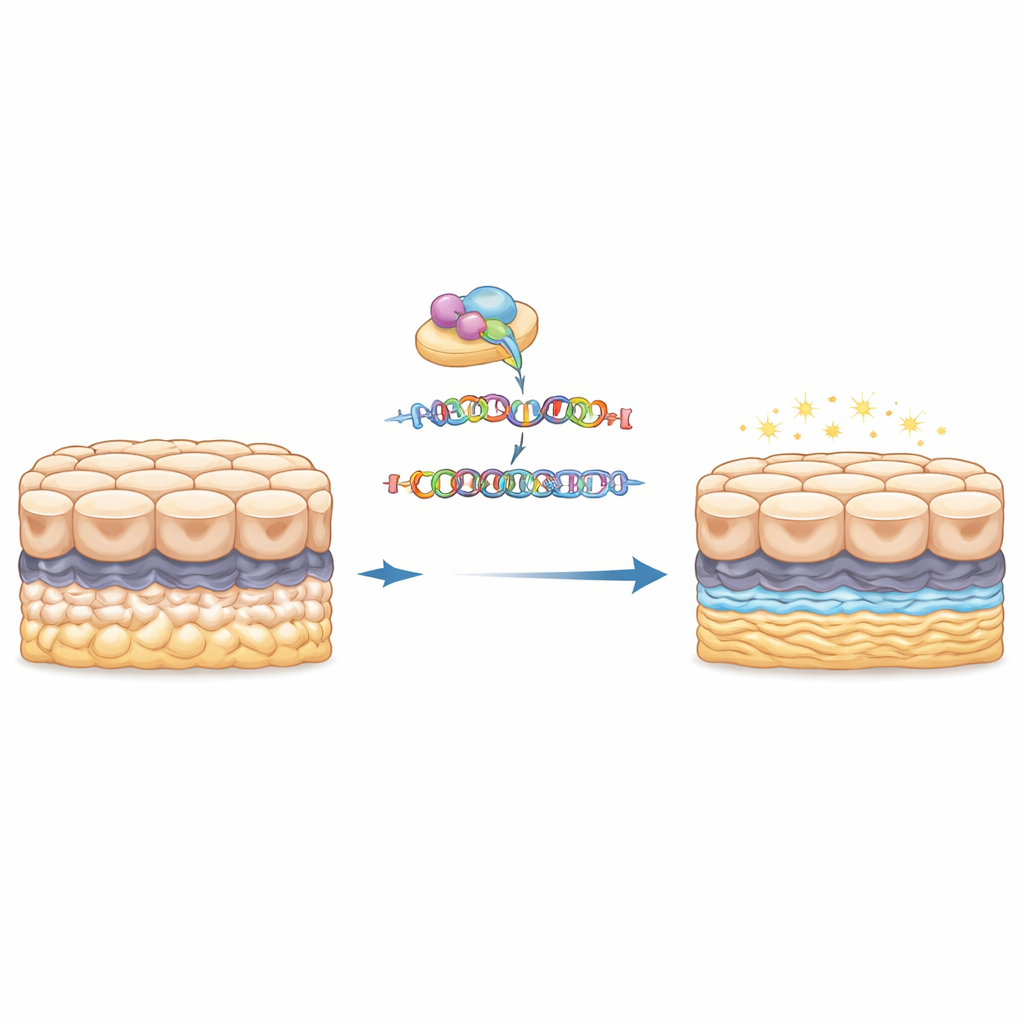
来自免疫警报系统的意外信号
令人意外的是,许多在删除重复后上升的蛋白与干扰素信号通路和抗原处理有关,这些通路通常与抗病毒防御和免疫监视相关。例如与血管生成和基质重塑相关的神经穿膜蛋白-1(neuropilin-1),以及有助于交联基质蛋白或调节细胞周期的酶,都在编辑细胞中上调。与此同时,一些保护性的应激缓冲蛋白,包括一种小型类热休克蛋白和参与细胞存活调控的信号连接蛋白则下降。总体来看,这些变化暗示重复扩增不仅改变角膜的物理支架,还抑制或重塑内皮细胞内的应激与类免疫反应,使细胞随着时间推移可能变得更脆弱。
从 DNA 重复到视力模糊
对于普通读者来说,关键信息是这项研究更清晰地将 TCF4 基因中的一个小异常与费克斯营养不良中角膜浑浊联系了起来。额外的 DNA 重复像一个隐藏的开关,重编程了角膜内皮细胞的蛋白质构成,促使它们沉积过多或错误类型的支撑材料,并改变它们与基底的黏附强度。在一个可控的细胞模型中删除该重复在很大程度上使这些与基质相关的蛋白恢复正常,并揭示了应激与免疫通路的变化,这强化了针对重复本身(例如反义寡核苷酸药物或精确的基因编辑工具)的治疗策略可能同时缓解结构性的 guttae 和角膜内皮功能衰退的观点。尽管仍需在患者组织中做进一步研究,这张蛋白组学图谱使研究者更接近于基于基因的、有理性的治疗方向,未来可能延缓或防止携带费克斯病患者发生需要角膜移植的情况。
引用: Yuasa, T., Nakagawa, T., Honda, T. et al. TCF4 trinucleotide repeat expansion drives distinct proteomic signatures in Fuchs endothelial corneal dystrophy. Sci Rep 16, 14446 (2026). https://doi.org/10.1038/s41598-026-43789-x
关键词: 费克斯角膜内皮营养不良, TCF4 重复扩增, 角膜内皮, 细胞外基质, 蛋白质组学