Clear Sky Science · ru
Расширение триплетного повтора TCF4 формирует отличительные протеомные сигнатуры при дистрофии роговичной эндотелия Фукса
Почему это заболевание глаза важно
С возрастом одной из самых частых причин пересадки роговицы является заболевание, называемое дистрофией роговичного эндотелия Фукса. При этой болезни внутренняя поверхность роговицы — обычно прозрачное, гладкое окошко — приобретает крошечные наросты и отёк, что приводит к помутнению зрения. Врачи давно знают, что участок повторяющегося ДНК-кода в гене TCF4 значительно повышает риск Фукса, но не понимали, как именно это дополнительное «заикание» в генетическом коде вредит клеткам, поддерживающим прозрачность роговицы. В этом исследовании авторы решают эту задачу, посмотрев напрямую на белки внутри поражённых клеток, с целью связать загадочное изменение в ДНК с повседневной работой глаза.
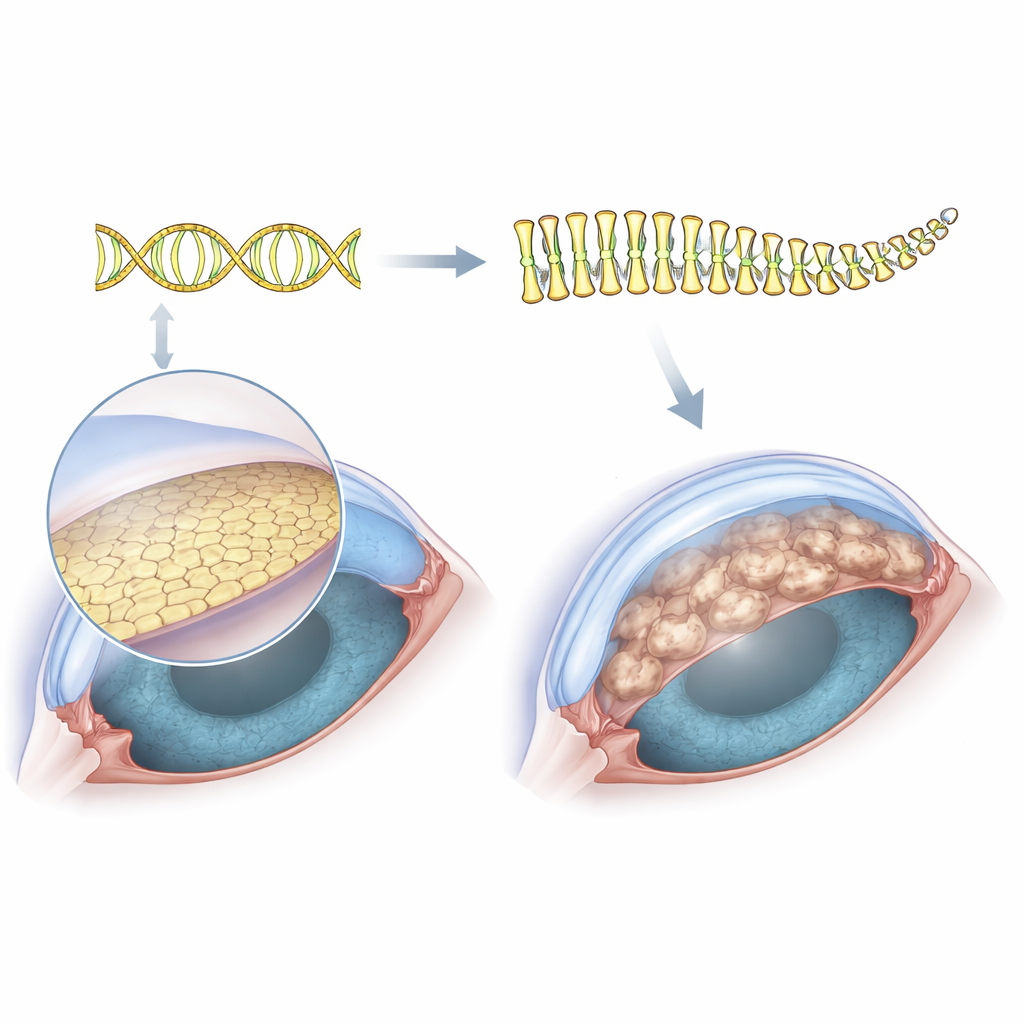
Смотрим на скрытую «рабочую силу» роговицы
Прозрачность роговицы зависит от единственного слоя клеток на её внутренней поверхности — роговичного эндотелия. Эти клетки располагаются на тонкой опорной мембране и постоянно откачивают жидкость из ткани, чтобы поддерживать прозрачность. При дистрофии Фукса эта внутренняя мембрана покрывается бородавчатоподобными выростами, называемыми гуттае, клетки постепенно погибают, и роговица отекает и мутнеет. Поскольку этот слой клеток очень тонкий, технически сложно собрать у пациентов достаточно материала, чтобы изучить все белки, которые они синтезируют. Чтобы обойти это ограничение, исследователи использовали иммортализованную клеточную линию от человека с Фуксом, которая естественно несёт расширенный TCF4-повтор, а затем с помощью редактирования генов CRISPR вырезали именно этот расширенный фрагмент, создав почти идеально сопоставимую систему «до и после».
Отключили повтор и наблюдали за изменением белков
После удаления расширенного повтора отредактированные клетки выглядели нормально в микроскоп: они сохраняли типичную многоугольную форму и образовывали аккуратные пласты, что говорит о том, что простое стирание повтора не разрушает базовую структуру клеток. Настоящие различия проявились при измерении тысяч белков с помощью чувствительного масс-спектрометрического метода, который маркирует и сравнивает образцы параллельно. Между исходными и отредактированными клетками 201 белок изменил свою концентрацию статистически значимым образом. Некоторые стали более выраженными, другие — менее, но вместе они сформировали отчётливый молекулярный отпечаток, чётко разделявший состояния «повтор включён» и «повтор выключен» при кластеризации и визуализации данных.
Нарушены «скелет» роговицы и клеточное прикрепление
Когда исследователи сгруппировали изменённые белки по функциям, выявились две основные темы. Многие белки, концентрация которых снизилась после удаления повтора, участвуют в создании и организации внеклеточного матрикса — сетчатого каркаса под клетками — а также в том, как клетки прикрепляются к этому каркасу и друг к другу. Сюда входят компоненты богатых коллагеном структур и белки, связывающие поверхность клетки с окружением. Поскольку избыток или аномальный матрикс являются характерной чертой гуттае при дистрофии Фукса, эта картина указывает на то, что расширение повтора TCF4 активно стимулирует чрезмерное создание и неправильное формирование внутренней поверхности роговицы. Тот факт, что удаление повтора снижает уровень этих матриксных и адгезионных белков, поддерживает прямую причинно-следственную связь между генетическим изменением и физическими наростами, наблюдаемыми в роговицах пациентов.
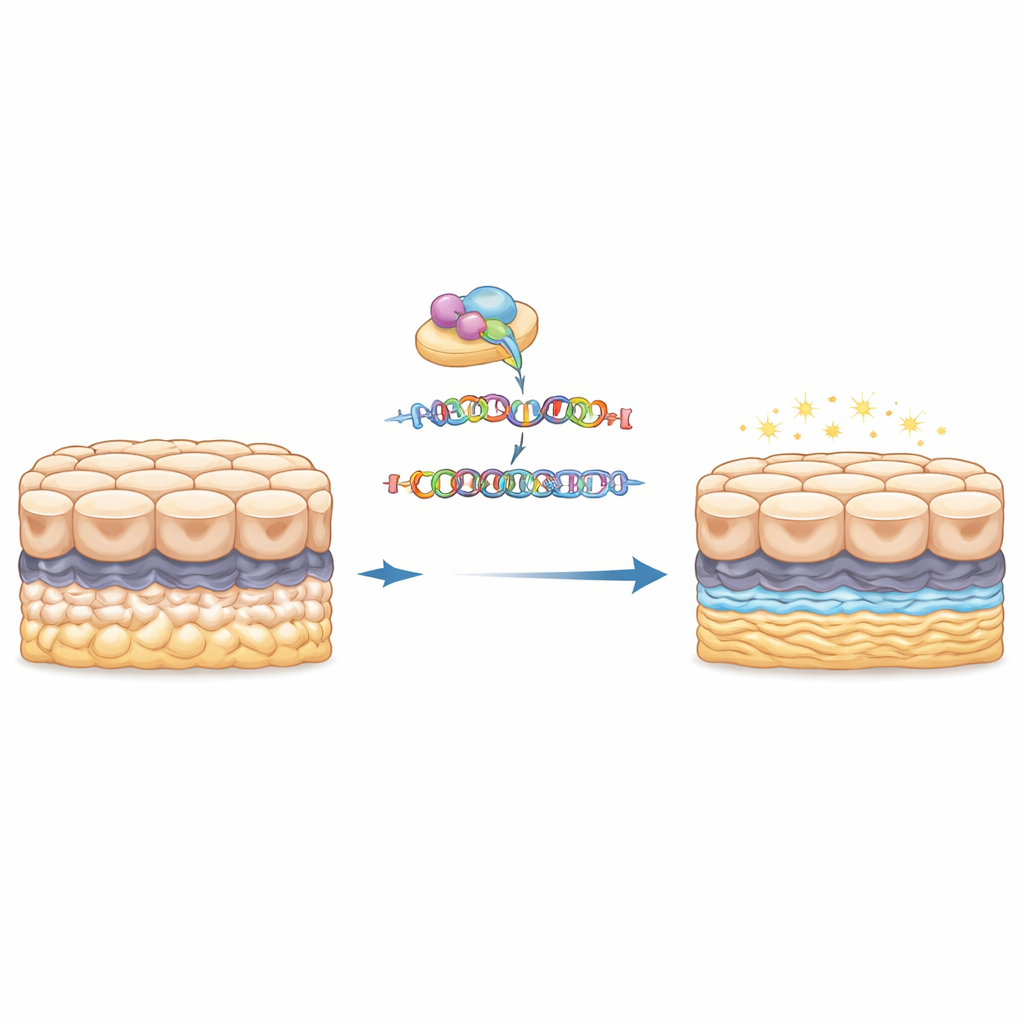
Неожиданные сигналы от иммунной «тревожной» системы
Удивительно, но многие белки, концентрация которых возросла после удаления повтора, были связаны с интерферонной сигнализацией и обработкой антигенов — путями, обычно ассоциированными с противовирусной защитой и иммунным надзором. Такие белки, как нейропилин‑1, молекула, связанная с ростом сосудов и ремоделированием матрикса, а также ферменты, помогающие перекрёстно связывать матриксные белки или регулировать клеточный цикл, все повысились в отредактированных клетках. В то же время несколько защитных белков, смягчающих стресс, включая небольшой белок, похожий на шоковый белок, и сигнальный адаптер, контролирующий выживание клеток, снизились. В совокупности эти сдвиги намекают, что расширение повтора не только меняет физический каркас роговицы, но и ослабляет или перестраивает стрессовые и иммуноподобные ответы внутри эндотелиальных клеток, что со временем может делать их более уязвимыми.
От ДНК‑повтора к мутному зрению
Для неспециалиста ключевое сообщение таково: это исследование проводит более чёткую линию от небольшой особенности в гене TCF4 до помутнения роговицы при дистрофии Фукса. Дополнительные повторы ДНК действуют как скрытый переключатель, перенастраивающий белковый ландшафт роговичных эндотелиальных клеток, побуждая их откладывать слишком много или не тот тип опорного материала и менять степень прикрепления к основе. Удаление этого повтора в контролируемой клеточной модели в значительной степени нормализует связанные с матриксом белки и выявляет изменения в путях стресса и иммунитета, что укрепляет идею о том, что терапия, нацеленная непосредственно на сам повтор — например, антисмысловые препараты или точные инструменты редактирования генов — может смягчить как структурные гуттае, так и функциональное снижение эндотелия роговицы. Хотя необходима дополнительная работа с тканью пациентов, эта протеомная карта приближает исследователей к рациональным генно‑направленным методам лечения, которые однажды могут отсрочить или предотвратить необходимость пересадки роговицы у людей с дистрофией Фукса.
Цитирование: Yuasa, T., Nakagawa, T., Honda, T. et al. TCF4 trinucleotide repeat expansion drives distinct proteomic signatures in Fuchs endothelial corneal dystrophy. Sci Rep 16, 14446 (2026). https://doi.org/10.1038/s41598-026-43789-x
Ключевые слова: Дистрофия роговичного эндотелия Фукса, Расширение повтора TCF4, эндотелий роговицы, внеклеточный матрикс, протеомика