Clear Sky Science · pl
Ekspansja trójnukleotydowego powtórzenia w TCF4 wywołuje odrębne podpisy proteomiczne w dystrofii śródbłonka rogówki Fuchsa
Dlaczego ta choroba oka ma znaczenie
Wraz z wiekiem jedną z najczęstszych przyczyn konieczności przeszczepu rogówki jest choroba zwana dystrofią śródbłonka rogówki Fuchsa. W tej chorobie wewnętrzna powierzchnia rogówki — normalnie przezroczyste, gładkie okno — rozwija drobne wybrzuszenia i obrzęk, które zamazują obraz. Lekarze od dawna wiedzą, że fragment powtarzającego się kodu DNA w genie o nazwie TCF4 wyraźnie zwiększa ryzyko Fuchsa, ale nie rozumieli, w jaki sposób to dodatkowe genetyczne „zacina się” faktycznie uszkadza komórki utrzymujące rogówkę w przejrzystości. To badanie podejmuje to pytanie, przyglądając się bezpośrednio białkom w dotkniętych komórkach, z zamiarem powiązania zagadkowej zmiany w DNA z codziennymi mechanizmami działania oka.
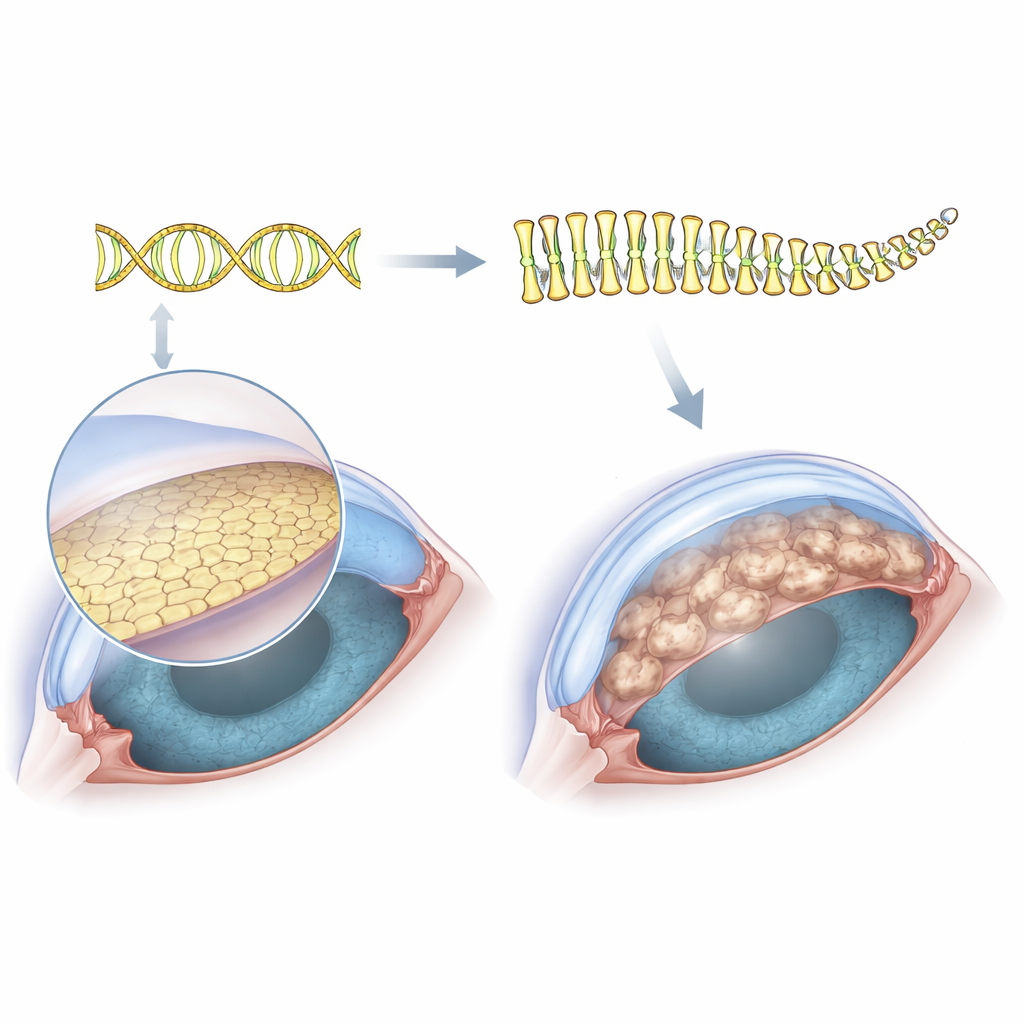
Przyglądając się ukrytej sile roboczej rogówki
Przejrzystość rogówki zależy od jednej warstwy komórek na jej wewnętrznej powierzchni, śródbłonka rogówki. Komórki te spoczywają na cienkiej warstwie podporowej i nieustannie wypompowują płyn z tkanki, aby utrzymać jej przejrzystość. W dystrofii Fuchsa ta wewnętrzna warstwa staje się pokryta brodawkowatymi wyroślami zwanymi guttae, komórki stopniowo obumierają, a rogówka puchnie i mętnieje. Ponieważ ta warstwa komórek jest tak cienka, technicznie trudno było zebrać wystarczającą ilość materiału od pacjentów, aby zbadać wszystkie wytwarzane przez nie białka. Aby to obejść, badacze użyli immortalizowanej linii komórkowej pochodzącej od osoby z Fuchsem, która naturalnie nosi rozszerzone powtórzenie TCF4, a następnie użyli edycji genów CRISPR, aby wyciąć właśnie ten rozszerzony fragment, tworząc niemal idealnie dopasowany system komórek „przed i po”.
Wyłączenie powtórzenia i obserwacja zmian w białkach
Po usunięciu rozszerzonego powtórzenia, komórki poddane edycji wyglądały normalnie pod mikroskopem: zachowały typowy wielokątny kształt i tworzyły uporządkowane warstwy, co sugeruje, że samo wykreślenie powtórzenia nie niszczy podstawowej struktury komórki. Rzeczywiste różnice ujawniły się, gdy zespół zmierzył tysiące białek przy użyciu czułej metody spektrometrii mas, która znakowała i porównywała próbki równolegle. Pomiędzy komórkami oryginalnymi a edytowanymi 201 białek zmieniło swoją obfitość w sposób statystycznie istotny. Niektóre stały się bardziej powszechne, inne mniej, ale razem utworzyły wyraźny odcisk molekularny, który jasno odróżniał stany „powtórzenie-włączone” i „powtórzenie-wyłączone” po zgrupowaniu i wizualizacji danych.
Szkielet rogówki i przyczep komórek są zaburzone
Gdy badacze pogrupowali zmienione białka według funkcji, wyłoniły się dwa główne motywy. Wiele białek, których poziomy spadły po usunięciu powtórzenia, uczestniczy w budowie i organizacji macierzy zewnątrzkomórkowej — sieciowej struktury pod komórkami — oraz w tym, jak komórki przyczepiają się do tej macierzy i do siebie nawzajem. Należą do nich składniki struktur bogatych w kolagen i białka łączące powierzchnię komórki z jej otoczeniem. Ponieważ nadmierna lub nieprawidłowa macierz jest cechą charakterystyczną guttae w dystrofii Fuchsa, ten wzorzec sugeruje, że ekspansja powtórzenia TCF4 aktywnie napędza nadmierne budowanie i deformację wewnętrznej powierzchni rogówki. Fakt, że usunięcie powtórzenia obniża poziomy tych białek macierzy i adhezji, wspiera bezpośredni związek przyczynowo-skutkowy między zmianą genetyczną a fizycznymi wybrzuszeniami obserwowanymi w rogówkach pacjentów.
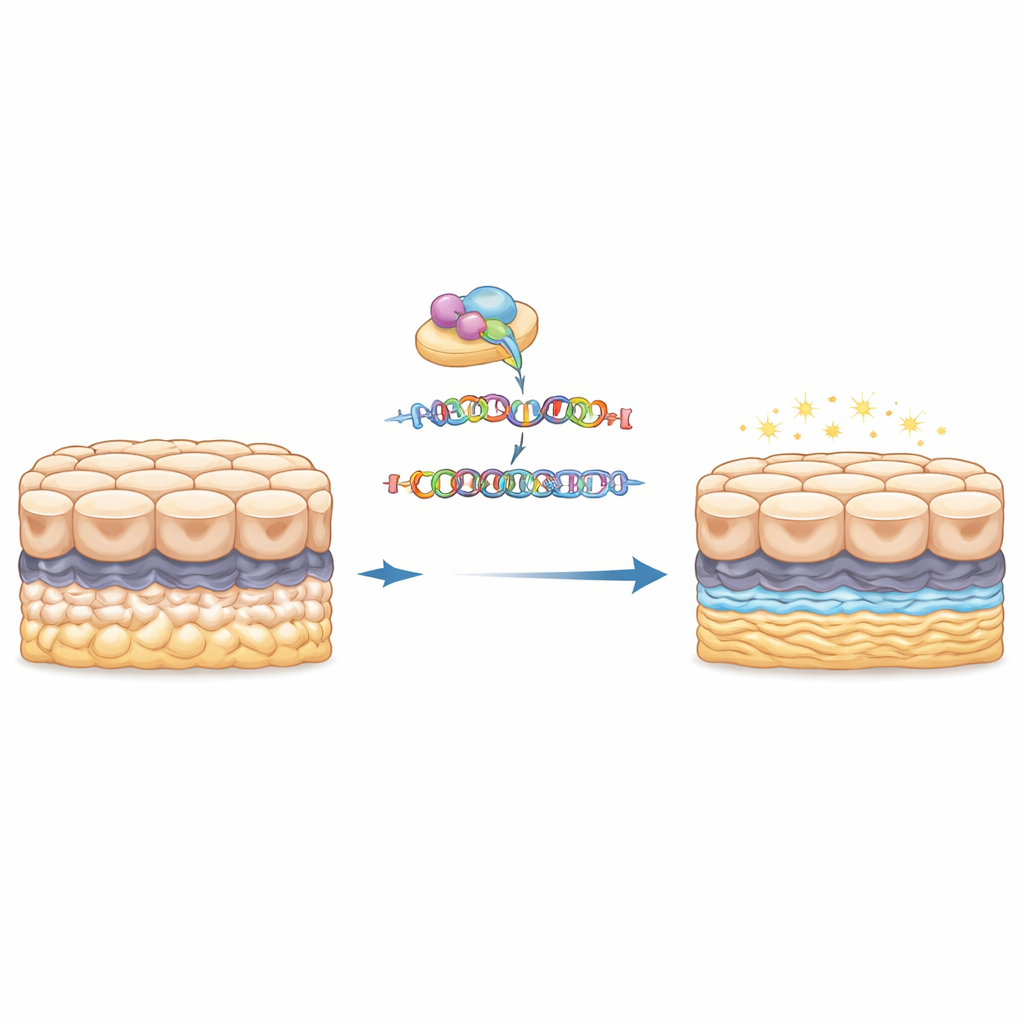
Niespodziewane sygnały z systemu alarmowego odporności
Zaskakująco, wiele białek, których poziomy wzrosły po usunięciu powtórzenia, było powiązanych z sygnalizacją interferonową i przetwarzaniem antygenów, szlakami zwykle kojarzonymi z obroną przeciwwirusową i nadzorem immunologicznym. Białka takie jak neuropilina-1, cząsteczka związana z angiogenezą i przebudową macierzy, oraz enzymy pomagające sieciować białka macierzy lub regulować cykl komórkowy, wzrosły w komórkach edytowanych. Jednocześnie kilka ochronnych białek buforujących stres, w tym małe białko podobne do heat-shock i adaptor sygnałowy pomagający kontrolować przeżywalność komórek, spadło. Razem te zmiany sugerują, że ekspansja powtórzenia nie tylko modyfikuje fizyczny szkielet rogówki, ale również tłumi lub przekształca odpowiedzi stresowe i immunopodobne w komórkach śródbłonka, potencjalnie czyniąc je bardziej podatnymi z czasem.
Od powtórzenia w DNA do zamglonego widzenia
Dla laika kluczowy przekaz jest taki, że to badanie bardziej klarownie łączy drobną anomalię w genie TCF4 z zmętnieniem rogówki obserwowanym w dystrofii Fuchsa. Dodatkowe powtórzenia DNA działają jak ukryty przełącznik, który przepisuje krajobraz białkowy komórek śródbłonka rogówki, skłaniając je do odkładania nadmiernej lub nieprawidłowej substancji podporowej i do zmiany sposobu mocnego przylegania do podłoża. Usunięcie tego powtórzenia w kontrolowanym modelu komórkowym w dużej mierze normalizuje te białka związane z macierzą i ujawnia przesunięcia w szlakach stresu i odporności, wzmacniając pomysł, że terapie ukierunkowane na samo powtórzenie — takie jak leki antysensowne lub precyzyjne narzędzia edycji genów — mogłyby złagodzić zarówno strukturalne guttae, jak i funkcjonalne pogorszenie śródbłonka rogówki. Choć potrzebne są dalsze badania na tkance pacjentów, ta mapa proteomiczna przybliża badaczy do racjonalnych, prowadzonych genetycznie terapii, które w przyszłości mogłyby opóźnić lub zapobiec konieczności przeszczepów rogówki u osób z dystrofią Fuchsa.
Cytowanie: Yuasa, T., Nakagawa, T., Honda, T. et al. TCF4 trinucleotide repeat expansion drives distinct proteomic signatures in Fuchs endothelial corneal dystrophy. Sci Rep 16, 14446 (2026). https://doi.org/10.1038/s41598-026-43789-x
Słowa kluczowe: Dystrofia śródbłonka rogówki Fuchsa, ekspansja powtórzenia TCF4, śródbłonek rogówki, macierz zewnątrzkomórkowa, proteomika