Clear Sky Science · de
TCF4-Trinukleotidwiederholungsexpansion treibt charakteristische proteomische Signaturen bei Fuchs-Endotheldystrophie der Hornhaut
Warum diese Augenkrankheit wichtig ist
Mit zunehmendem Alter ist eine der häufigsten Ursachen für eine Hornhauttransplantation eine Erkrankung namens Fuchs-Endotheldystrophie. Bei dieser Krankheit entwickelt die innere Oberfläche der Hornhaut – normalerweise ein klares, glattes Fenster – winzige Erhebungen und Schwellungen, die das Sehvermögen trüben. Ärztinnen und Ärzte wissen seit Langem, dass eine Strecke sich wiederholender DNA im Gen TCF4 das Risiko für Fuchs stark erhöht, aber wie dieses zusätzliche genetische "Stottern" die Zellen schädigt, die die Hornhaut klar halten, war unklar. Diese Studie geht dieser Frage nach, indem sie direkt die Proteine in betroffenen Zellen betrachtet, mit dem Ziel, eine mysteriöse DNA-Änderung mit den alltäglichen Funktionen des Auges zu verknüpfen.
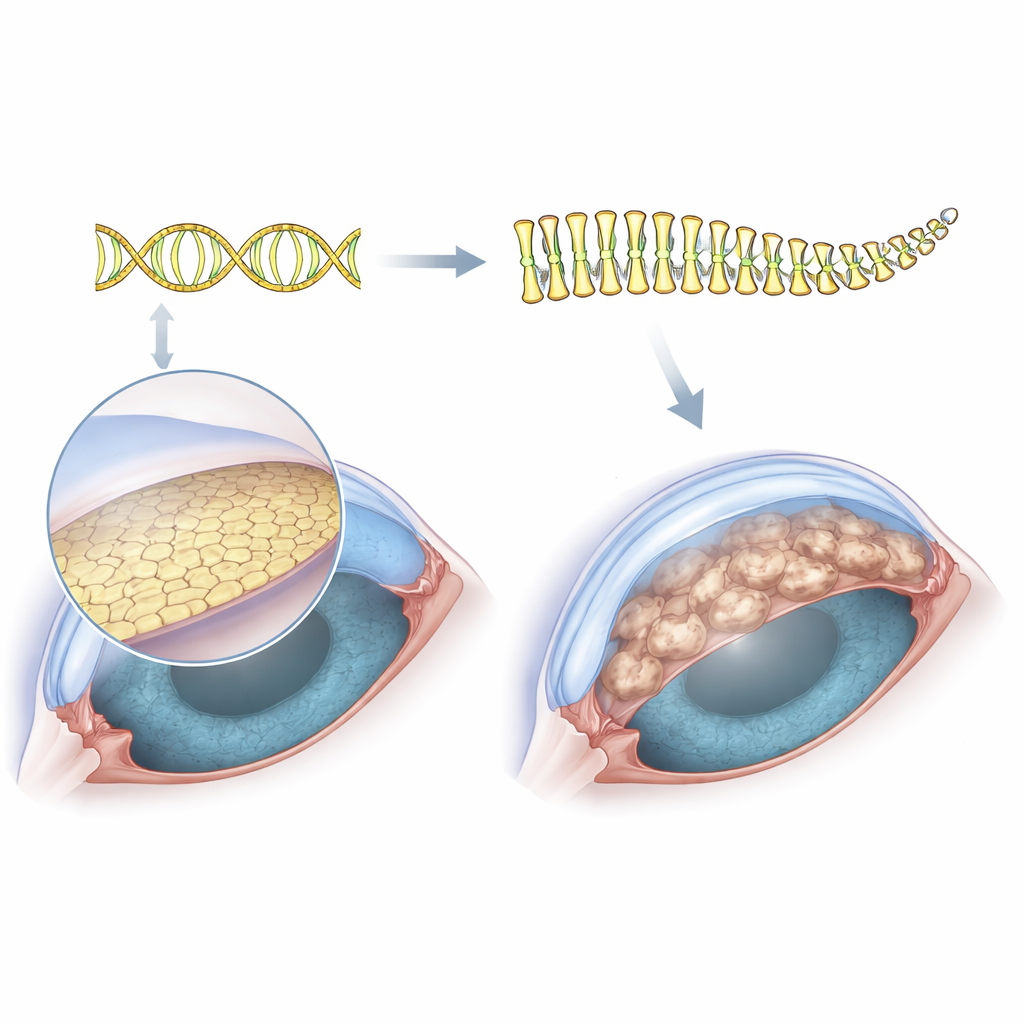
Blick auf die verborgene Arbeitskraft der Hornhaut
Die Klarheit der Hornhaut hängt von einer einzigen Zellschicht an ihrer Innenseite ab, dem Hornhautendothel. Diese Zellen sitzen auf einer dünnen Stützschicht und pumpen ständig Flüssigkeit aus dem Gewebe, um es transparent zu halten. Bei der Fuchs-Dystrophie wird diese innere Schicht von warzenähnlichen Auswüchsen, den sogenannten Guttae, übersät, die Zellen sterben allmählich ab und die Hornhaut schwillt an und trübt. Da diese Zellschicht so dünn ist, war es technisch schwierig, genügend Material von Patientinnen und Patienten zu gewinnen, um alle gebildeten Proteine zu untersuchen. Um dies zu umgehen, verwendeten die Forscher eine immortaliserte Zelllinie aus einer Person mit Fuchs, die natürlich die erweiterte TCF4-DNA-Wiederholung trägt, und setzten dann CRISPR-Geneditierung ein, um genau dieses erweiterte Segment zu entfernen und so ein nahezu perfekt passendes "Vorher-Nachher"-Zellsystem zu schaffen.
Die Wiederholung ausschalten und Proteine beobachten
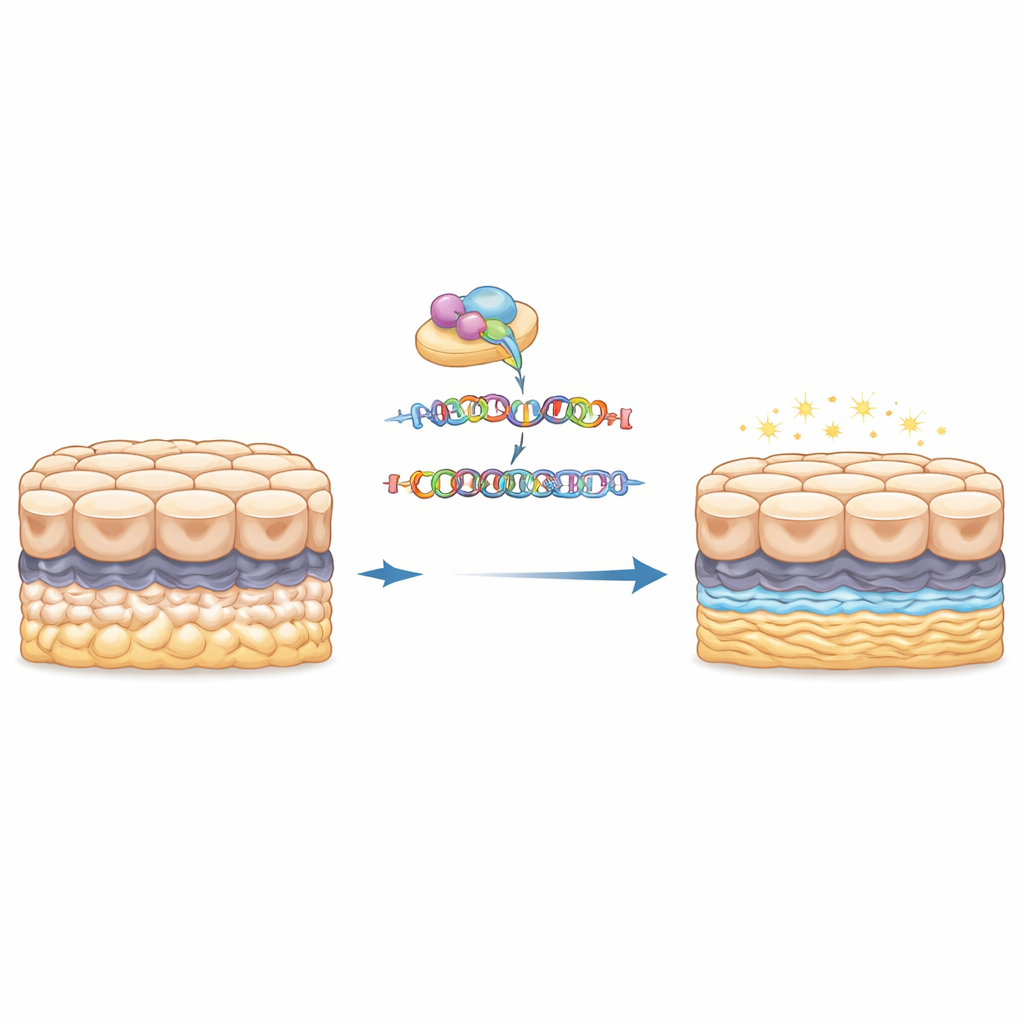
Nachdem die erweiterte DNA-Wiederholung entfernt war, wirkten die editierten Zellen unter dem Mikroskop normal: Sie behielten ihre typische polygonale Form und bildeten ordentliche Schichten, was darauf hindeutet, dass das bloße Löschen der Wiederholung die grundlegende Zellstruktur nicht schädigt. Die wirklichen Unterschiede zeigten sich, als das Team Tausende von Proteinen mit einer empfindlichen Massenspektrometriemethode maß, die Proben parallel markiert und vergleicht. Zwischen den Original- und den editierten Zellen änderten sich 201 Proteine in ihrer Häufigkeit auf statistisch bedeutsame Weise. Einige wurden häufiger, andere seltener, aber zusammen bildeten sie einen eindeutigen molekularen Fingerabdruck, der die "Wiederholung-an"- und "Wiederholung-aus"-Zustände klar trennte, als die Daten gruppiert und visualisiert wurden.
Das Gerüst der Hornhaut und der Zell"halt" sind gestört
Als die Forscher diese veränderten Proteine nach Funktion gruppierten, traten zwei Hauptthemen hervor. Viele der Proteine, die nach dem Entfernen der Wiederholung abnahmen, sind an Aufbau und Organisation der extrazellulären Matrix – dem netzartigen Gerüst unter den Zellen – sowie an der Art und Weise beteiligt, wie Zellen an diesem Gerüst und aneinander haften. Dazu gehören Bestandteile kollagenreicher Strukturen und Proteine, die Zelloberflächen mit ihrer Umgebung verbinden. Da überschüssige oder abnorme Matrix ein Kennzeichen der Guttae bei der Fuchs-Dystrophie ist, deutet dieses Muster darauf hin, dass die TCF4-Wiederholungsexpansion aktiv das Überbauen und die Deformierung der inneren Hornhautoberfläche antreibt. Dass das Löschen der Wiederholung diese Matrix- und Adhäsionsproteine abschwächt, stützt eine direkte Ursache-Wirkungs-Verbindung zwischen der genetischen Veränderung und den physischen Erhebungen, die bei Patientinnen und Patienten zu sehen sind.
Unerwartete Signale vom Immunalarm
Überraschenderweise waren viele der Proteine, die nach dem Entfernen der Wiederholung zunahmen, mit Interferon-Signalgebung und Antigenverarbeitung verknüpft – Wege, die normalerweise mit antiviraler Abwehr und immunologischer Überwachung assoziiert werden. Proteine wie Neuropilin-1, ein Molekül, das mit Gefäßwachstum und Matrixumbau in Verbindung steht, sowie Enzyme, die Matrixproteine quervernetzen oder den Zellzyklus regulieren, stiegen in den editierten Zellen an. Gleichzeitig fielen mehrere schützende Stresspufferproteine, darunter ein kleines hitze-schock–ähnliches Protein und ein Signaladapter, der die Zellüberlebenssteuerung unterstützt. Zusammengenommen deuten diese Verschiebungen darauf hin, dass die Wiederholungsexpansion nicht nur das physische Gerüst der Hornhaut verändert, sondern auch Stress- und immunähnliche Reaktionen innerhalb der Endothelzellen dämpft oder umgestaltet und sie so im Laufe der Zeit anfälliger machen könnte.
Von der DNA-Wiederholung zur trüben Sicht
Für Laien ist die Kernbotschaft, dass diese Studie eine klarere Verbindung von einer kleinen Eigenheit im TCF4-Gen zur getrübten Hornhaut bei der Fuchs-Dystrophie zieht. Die zusätzlichen DNA-Wiederholungen wirken wie ein versteckter Schalter, der die Proteom-Landschaft der Hornhautendothelzellen umverdrahtet, sie dazu bringt, zu viel oder die falsche Art von Stützmaterial abzusetzen und zu verändern, wie fest sie an ihrer Basis haften. Das Entfernen dieser Wiederholung in einem kontrollierten Zellmodell normalisiert weitgehend diese matrixbezogenen Proteine und legt Verschiebungen in Stress- und Immunwegen offen, was die Vorstellung stärkt, dass Therapien, die gezielt die Wiederholung ansprechen – etwa Antisense-Medikamente oder präzise Geneditierungstools – sowohl die strukturellen Guttae als auch den funktionellen Abbau des Hornhautendothels lindern könnten. Zwar sind weitere Arbeiten an Patientengewebe notwendig, doch diese proteomische Landkarte bringt Forschende dem Ziel näher, rationale, genbasierte Behandlungen zu entwickeln, die eines Tages die Notwendigkeit von Hornhauttransplantationen bei Menschen mit Fuchs-Dystrophie verzögern oder verhindern könnten.
Zitation: Yuasa, T., Nakagawa, T., Honda, T. et al. TCF4 trinucleotide repeat expansion drives distinct proteomic signatures in Fuchs endothelial corneal dystrophy. Sci Rep 16, 14446 (2026). https://doi.org/10.1038/s41598-026-43789-x
Schlüsselwörter: Fuchs-Endotheldystrophie der Hornhaut, TCF4-Wiederholungsexpansion, Hornhautendothel, extrazelluläre Matrix, Proteomik