Clear Sky Science · zh
芬戈莫德使与突触可塑性和记忆相关的代谢特征在APP/PS1模型中恢复正常:鞘氨醇‑1‑磷酸受体作为阿尔茨海默病的治疗靶点
这项研究对家庭和衰老大脑意味着什么
阿尔茨海默病夺走了数百万人的记忆,但现有药物只能提供有限的缓解,对大脑的根本变化帮助甚微。本研究考察了一个出人意料的盟友:已用于多发性硬化的药物芬戈莫德。通过研究该药物如何重塑大脑化学和在类阿尔茨海默小鼠模型中增强记忆,研究者提出了一种新的保护脑细胞的方法:恢复能量供应并抑制有害炎症。
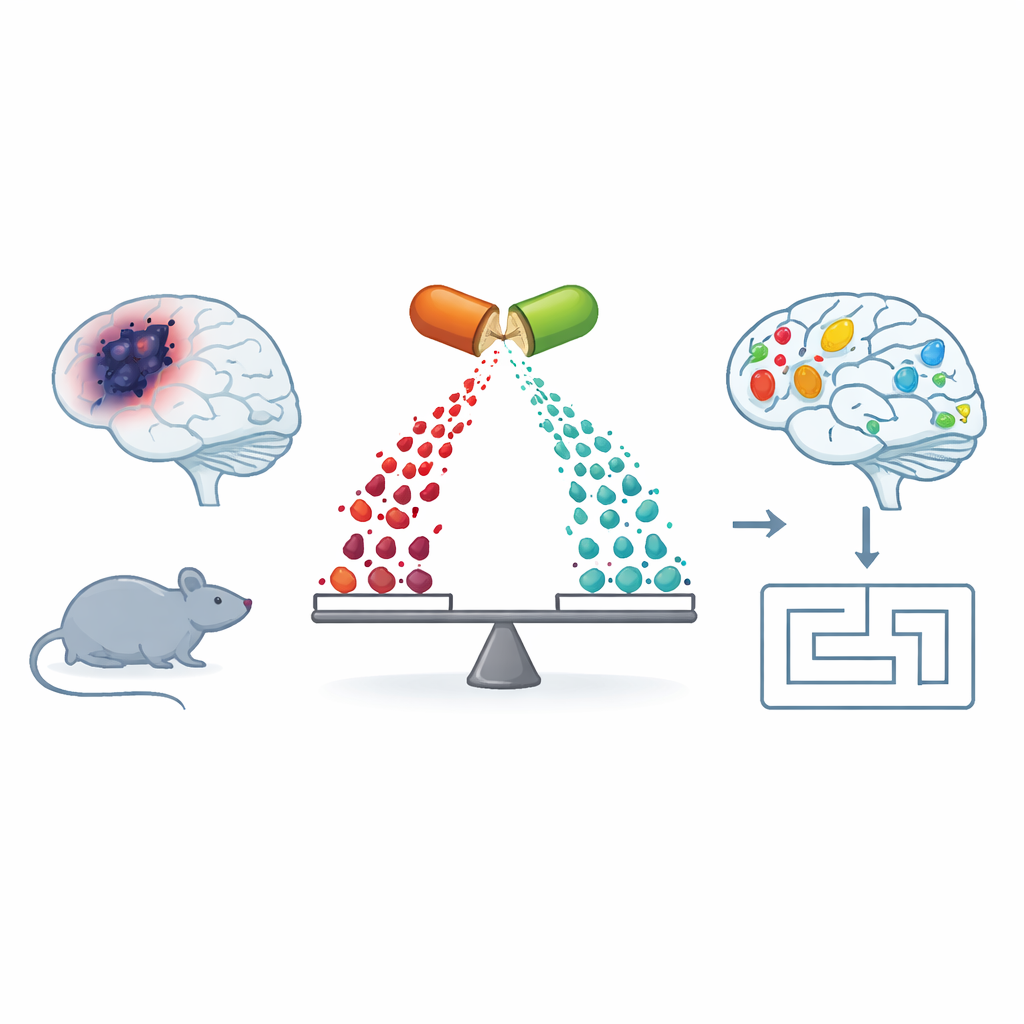
超越斑块与缠结,更细致地审视阿尔茨海默
大多数人都知道黏性的淀粉样斑块和扭曲的Tau缠结是阿尔茨海默病的标志。但在这些可见迹象背后,还存在大脑化学的更隐蔽扰动,尤其是构成细胞膜并在细胞间传递信号的脂类。研究团队研究了会出现类阿尔茨海默变化的老鼠(APP/PS1小鼠),并与健康小鼠进行了比较。他们在脑、血液和肝脏中测量了数百种小分子,发现类阿尔茨海默小鼠在若干分子类别中表现出广泛的不平衡,包括特化的脂类和被称为多胺的化合物——多胺有助于维持线粒体(细胞的动力工厂)的正常运作。
当大脑的脂类平衡失衡
研究的一个重点是称为鞘脂类的一组脂质,它们的平衡决定了细胞趋向存活还是死亡。在类阿尔茨海默小鼠中,这一“脂类平衡”偏向与细胞应激和炎症相关的分子,而保护性形式减少。与此同时,富含线粒体的细胞区域中构建膜的关键脂类发生了改变,支持线粒体能量产生的精胺及相关多胺的生成也减少。这些变化共同指向一个能量匮乏、易发炎的大脑环境,可能损害突触——学习和记忆编码的连接点。
将多发性硬化药物重新定位以重置大脑化学
研究人员随后用芬戈莫德处理了类阿尔茨海默小鼠,这种药物作用于一种脂质信使鞘氨醇‑1‑磷酸的受体。在早期工作中,同一团队已显示该处理能改善学习和突触可塑性(突触随经验增强的能力)。在这项新研究中,他们确认芬戈莫德恢复了小鼠在空间记忆任务(Barnes迷宫)中的表现,并在海马的一个主要通路中恢复了长期增强(LTP)——这一学习的关键电生理标志。在化学层面,芬戈莫德增加了保护性鞘脂信号,降低了有害鞘酰胺的标志,并在很大程度上逆转了大脑膜中许多异常的脂肪饱和度模式,尤其是在与记忆相关的颞皮层区域。
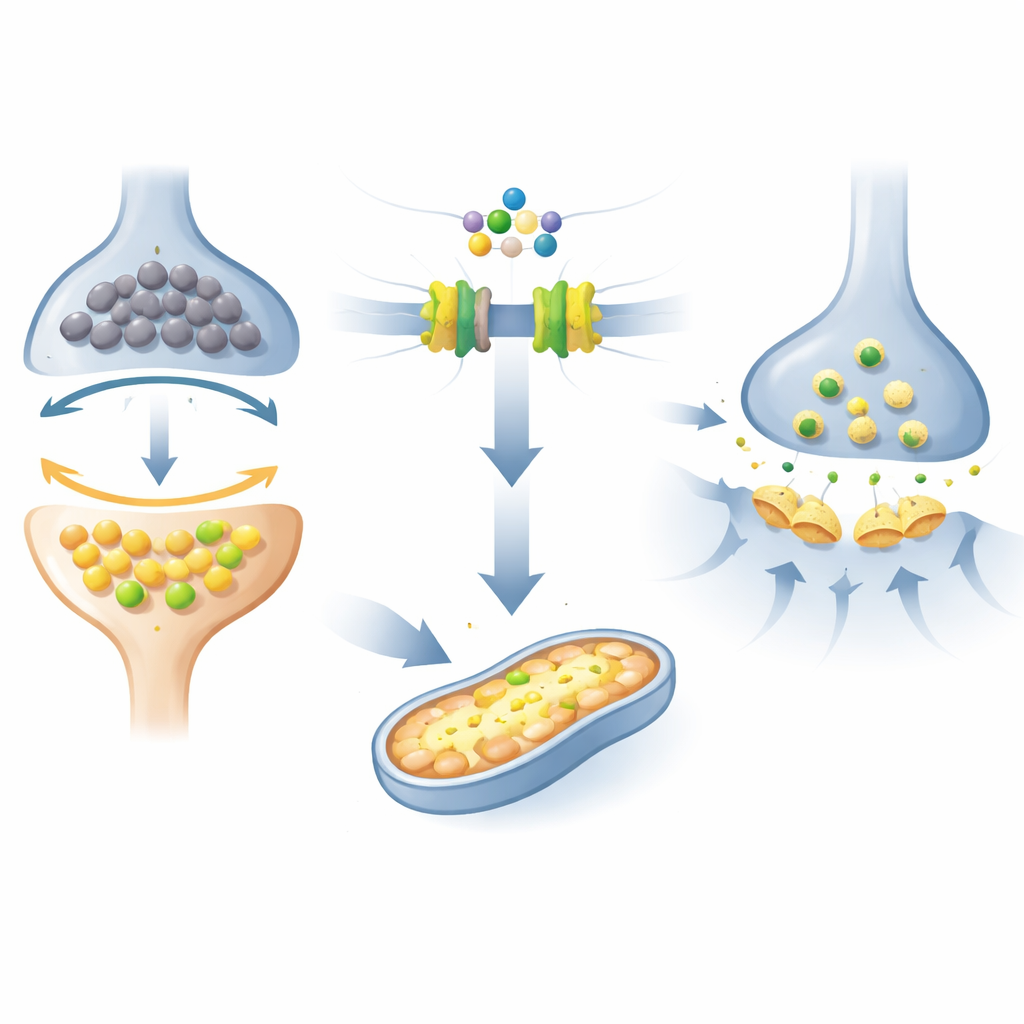
为线粒体补能并稳定记忆回路
除了这些脂类分子,芬戈莫德还提升了精胺合成的指标并增加了酰基肉碱——将脂肪运送到线粒体以用于能量产生的中间载体。这些改变与记忆表现和突触强度的改善紧密相关,表明该药物有助于挽救脑细胞的线粒体功能。该治疗还以符合该药已知细胞信号效应的方式改变了其他代谢通路:促进促存活通路、提高血清素、支持大脑内的抗炎免疫状态,并减少与氧化应激相关的副产物。简而言之,该药似乎将整个信号网络推向更健康、更有弹性的状态。
这对未来阿尔茨海默治疗可能意味着什么
通俗地说,这项工作表明,帮助脑细胞重建其内部化学平衡——特别是那些控制细胞存活的脂类和为线粒体供能的燃料——可能恢复部分因类阿尔茨海默变化而受损的记忆功能。芬戈莫德并非仅仅掩盖症状;在小鼠中,它纠正了与突触健康和学习相关的基础代谢紊乱。尽管小鼠毕竟不是人类,还需要更多机制和临床研究,但这些发现突出了一个有前景的新治疗方向:通过鞘氨醇‑1‑磷酸受体及相关通路靶向脂质与能量代谢,以在回路彻底失败前保护大脑网络。
引用: Kalecký, K., Buitrago, L., Alarcon, J.M. et al. Fingolimod normalizes metabolic signatures associated with synaptic plasticity and memory in APP/PS1 model: Sphingosine-1-phosphate receptor a therapeutic target for Alzheimer’s. Sci Rep 16, 12835 (2026). https://doi.org/10.1038/s41598-026-42518-8
关键词: 阿尔茨海默病, 大脑代谢, 芬戈莫德, 鞘脂类, 线粒体功能