Clear Sky Science · fr
Le fingolimod normalise les signatures métaboliques associées à la plasticité synaptique et à la mémoire dans le modèle APP/PS1 : le récepteur de la sphingosine‑1‑phosphate, une cible thérapeutique pour la maladie d’Alzheimer
Pourquoi cette recherche compte pour les familles et les cerveaux vieillissants
La maladie d’Alzheimer prive des millions de personnes de leurs souvenirs, alors que les médicaments actuels n’offrent qu’un soulagement modeste et peu d’effet sur les changements cérébraux sous‑jacents. Cette étude examine un allié inattendu : le fingolimod, un médicament déjà utilisé dans la sclérose en plaques. En analysant comment ce traitement remodèle la chimie cérébrale et améliore la mémoire dans un modèle murin d’allure Alzheimer, les chercheurs proposent une nouvelle manière de protéger les neurones en restaurant leur approvisionnement énergétique et en calmant l’inflammation dommageable.
Un regard plus précis sur Alzheimer au‑delà des plaques et des enchevêtrements
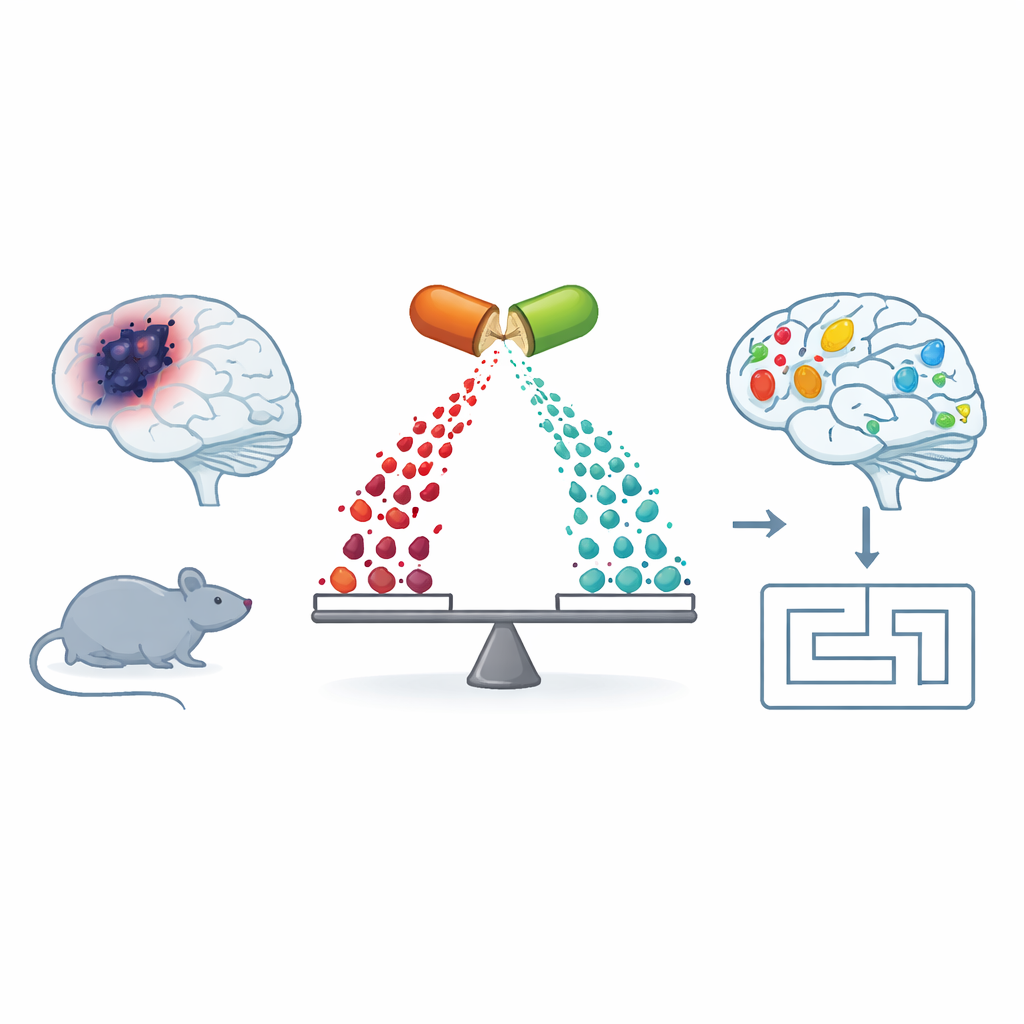
La plupart des gens savent que les plaques amyloïdes collantes et les enchevêtrements de protéine tau sont des signes emblématiques de la maladie d’Alzheimer. Mais derrière ces signes visibles se cache une perturbation plus discrète de la chimie cérébrale, en particulier des lipides qui composent les membranes cellulaires et véhiculent des signaux entre les cellules. L’équipe a étudié des souris développant des modifications proches d’Alzheimer (souris APP/PS1) et les a comparées à des souris saines. Ils ont mesuré des centaines de petites molécules dans le cerveau, le sang et le foie et ont constaté que les souris modèle présentaient de larges déséquilibres dans plusieurs familles de composés, y compris des lipides spécialisés et des polyamines, qui aident à maintenir les mitochondries — les centrales énergétiques des cellules — en bon fonctionnement.
Quand l’équilibre lipidique du cerveau bascule
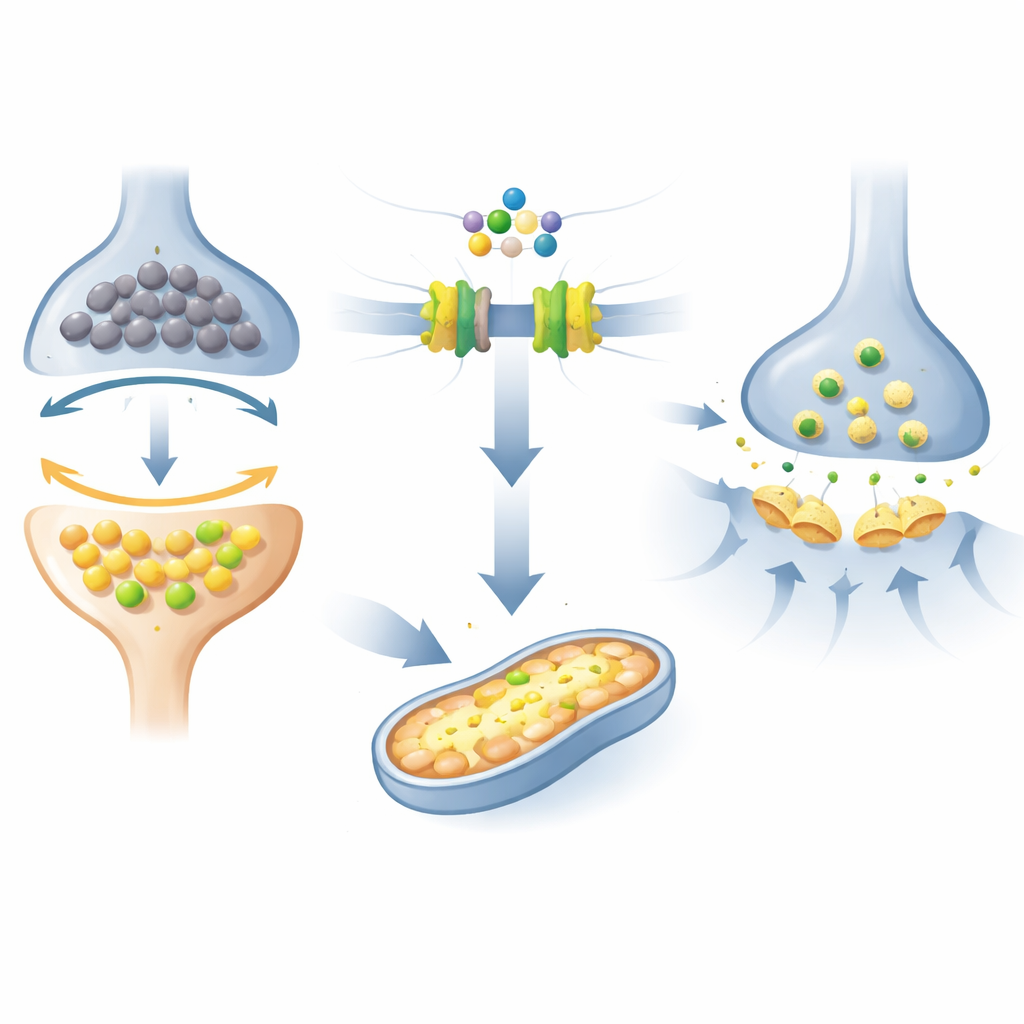
Un axe majeur d’étude porte sur une famille de lipides appelée sphingolipides, qui peuvent soit favoriser la survie cellulaire, soit conduire à la mort selon leur équilibre. Chez les souris APP/PS1, cet « équilibre lipidique » était décalé vers des molécules associées au stress cellulaire et à l’inflammation, tandis que les formes protectrices étaient réduites. Parallèlement, des lipides structurants des membranes dans les régions riches en mitochondries des neurones étaient altérés, et la production de spermidine et d’autres polyamines, qui soutiennent la production d’énergie mitochondriale, était diminuée. Ensemble, ces changements dessinent un environnement cérébral affamé en énergie et enclin à l’inflammation, susceptible de fragiliser les synapses — les jonctions où s’inscrivent apprentissage et mémoire.
Réaffecter un médicament de la sclérose en plaques pour réinitialiser la chimie cérébrale
Les chercheurs ont alors traité les souris APP/PS1 avec le fingolimod, un médicament qui cible les récepteurs d’un messager lipidique appelé sphingosine‑1‑phosphate. Dans des travaux antérieurs, le même groupe avait montré que ce traitement améliorait l’apprentissage et la plasticité synaptique (la capacité des synapses à se renforcer avec l’expérience). Dans la nouvelle étude, ils confirment que le fingolimod a rétabli les performances dans une tâche de mémoire spatiale (le labyrinthe de Barnes) et a ravivé la potentialisation à long terme, une signature électrique clé de l’apprentissage, dans une voie hippocampique majeure. Au niveau chimique, le fingolimod a augmenté les signaux sphingolipidiques protecteurs, réduit les marqueurs de céramides délétères et inversé pour une large part de nombreux profils anormaux de saturation lipidique dans les membranes cérébrales, en particulier dans les régions du cortex temporal liées à la mémoire.
Booster les mitochondries et stabiliser les circuits de la mémoire
Au‑delà de ces lipides, le fingolimod a renforcé les indicateurs de synthèse de la spermidine et augmenté les acylcarnitines, des transporteurs intermédiaires qui acheminent les lipides vers les mitochondries pour la production d’énergie. Ces changements étaient étroitement corrélés à des améliorations de la mémoire et de la force synaptique, suggérant que le médicament aide à restaurer la fonction mitochondriale dans les neurones. Le traitement a aussi modifié d’autres voies métaboliques d’une manière cohérente avec les effets de signalisation cellulaire connus du médicament : favoriser les voies pro‑survie, augmenter la sérotonine, soutenir des états immunitaires anti‑inflammatoires dans le cerveau et réduire les sous‑produits liés au stress oxydatif. En bref, le médicament semble orienter l’ensemble du réseau de signaux vers un état plus sain et plus résilient.
Ce que cela pourrait signifier pour les traitements futurs contre Alzheimer
Concrètement, ce travail suggère que rééquilibrer la chimie interne des cellules cérébrales — en particulier les lipides qui contrôlent la survie cellulaire et les carburants qui alimentent les mitochondries — pourrait restaurer une partie des fonctions mnésiques altérées par des changements de type Alzheimer. Le fingolimod n’a pas seulement masqué les symptômes ; chez la souris, il a corrigé des perturbations métaboliques sous‑jacentes liées à la santé synaptique et à l’apprentissage. Si les souris ne sont pas des humains et que des études mécanistiques et cliniques supplémentaires sont nécessaires, ces résultats mettent en lumière un angle thérapeutique prometteur : cibler le métabolisme des lipides et de l’énergie, via les récepteurs de la sphingosine‑1‑phosphate et les voies associées, pour protéger les circuits cérébraux bien avant leur effondrement.
Citation: Kalecký, K., Buitrago, L., Alarcon, J.M. et al. Fingolimod normalizes metabolic signatures associated with synaptic plasticity and memory in APP/PS1 model: Sphingosine-1-phosphate receptor a therapeutic target for Alzheimer’s. Sci Rep 16, 12835 (2026). https://doi.org/10.1038/s41598-026-42518-8
Mots-clés: Maladie d’Alzheimer, métabolisme cérébral, fingolimod, sphingolipides, fonction mitochondriale