Clear Sky Science · de
Fingolimod normalisiert mit synaptischer Plastizität und Gedächtnis assoziierte metabolische Signaturen im APP/PS1-Modell: Sphingosin-1-phosphat-Rezeptor als therapeutisches Ziel bei Alzheimer
Warum diese Forschung für Familien und alternde Gehirne wichtig ist
Die Alzheimer-Krankheit raubt Millionen Menschen ihre Erinnerungen; die heute verfügbaren Medikamente lindern jedoch nur wenig Symptome und greifen kaum die zugrunde liegenden Veränderungen im Gehirn an. Diese Studie richtet den Blick auf einen unerwarteten Verbündeten: Fingolimod, ein Arzneimittel, das bereits zur Behandlung von Multipler Sklerose eingesetzt wird. Indem die Forschenden untersuchten, wie dieses Medikament die Gehirnchemie umformt und das Gedächtnis in einem Alzheimer-ähnlichen Mausmodell verbessert, schlagen sie einen neuen Weg vor, Gehirnzellen zu schützen, indem man ihre Energieversorgung wiederherstellt und schädliche Entzündungsprozesse dämpft.
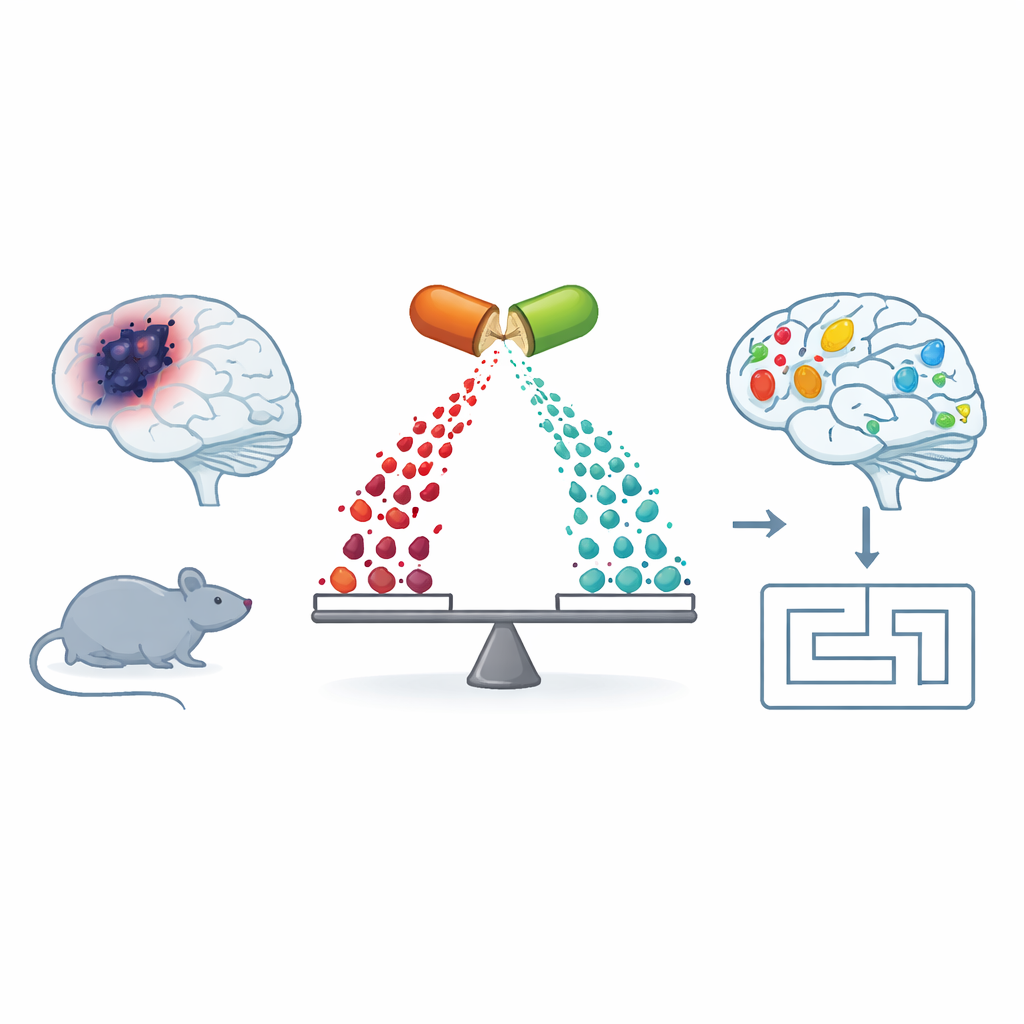
Ein genauerer Blick auf Alzheimer jenseits von Plaques und Tangles
Die meisten Menschen haben von den klebrigen Amyloid-Plaques und den verdrehten Tau-Tangles gehört, die typische Merkmale der Alzheimer-Krankheit sind. Hinter diesen sichtbaren Zeichen verbirgt sich jedoch eine leisere Störung der Gehirnchemie, insbesondere der Fette (Lipide), die Zellmembranen bilden und Signale zwischen Zellen übertragen. Das Team untersuchte Mäuse, die Alzheimer-ähnliche Veränderungen entwickeln (APP/PS1-Mäuse), und verglich sie mit gesunden Mäusen. Sie maßen Hunderte kleiner Moleküle im Gehirn, Blut und in der Leber und fanden heraus, dass die Alzheimer-ähnlichen Mäuse breite Ungleichgewichte in mehreren Molekülgruppen aufwiesen, darunter spezialisierte Fette und Verbindungen namens Polyamine, die dazu beitragen, die Mitochondrien—die Kraftwerke der Zellen—reibungslos am Laufen zu halten.
Wenn das Fettgleichgewicht im Gehirn aus dem Ruder läuft
Ein zentraler Schwerpunkt lag auf einer Gruppe von Fetten, den Sphingolipiden, die je nach ihrem Verhältnis Zellen entweder in Richtung Überleben oder Tod drängen können. Bei den Alzheimer-ähnlichen Mäusen war dieses „Fettgleichgewicht“ zugunsten von Molekülen verschoben, die mit Zellstress und Entzündung verbunden sind, während schützende Formen reduziert waren. Gleichzeitig waren wichtige membranbildende Lipide in mitochondrienreichen Bereichen von Gehirnzellen verändert, und die Produktion von Spermidin und verwandten Polyaminen, die die mitochondriale Energieproduktion unterstützen, war reduziert. Zusammen weisen diese Verschiebungen auf eine energiearme, entzündungsanfällige Gehirnumgebung hin, die Synapsen—die Schnittstellen, an denen Lernen und Gedächtnis verschaltet werden—untergraben kann.
Ein MS-Medikament neu einsetzen, um die Gehirnchemie zurückzusetzen
Die Forschenden behandelten die Alzheimer-ähnlichen Mäuse anschließend mit Fingolimod, einem Wirkstoff, der Rezeptoren für einen Lipidbotenstoff namens Sphingosin‑1‑phosphat anspricht. In früheren Arbeiten hatte dieselbe Gruppe gezeigt, dass diese Behandlung Lernen und synaptische Plastizität (die Fähigkeit von Synapsen, sich durch Erfahrung zu verstärken) verbesserte. In der neuen Studie bestätigten sie, dass Fingolimod die Leistung in einer räumlichen Gedächtnisaufgabe (dem Barnes-Maze) wiederherstellte und die Langzeitpotenzierung, ein wichtiges elektrisches Kennzeichen des Lernens, in einem zentralen Hippocampusweg belebte. Auf chemischer Ebene erhöhte Fingolimod schützende Sphingolipid-Signale, verringerte Marker schädlicher Ceramide und kehrte viele der abnormalen Muster der Lipidsättigung in Zellmembranen weitgehend um, insbesondere in temporalen Cortexregionen, die mit dem Gedächtnis verknüpft sind.
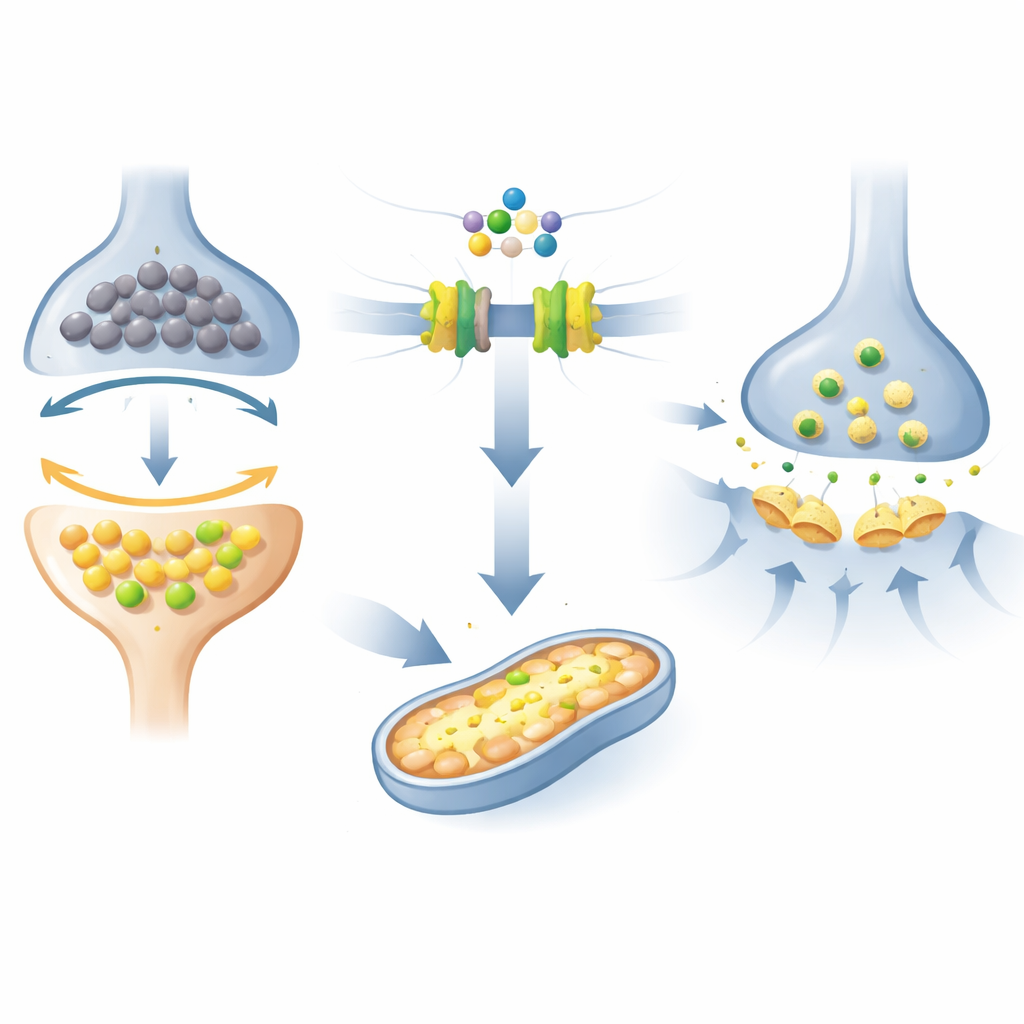
Mitochondrien auf Touren bringen und Gedächtnisschaltungen stabilisieren
Über diese Fettmoleküle hinaus förderte Fingolimod Hinweise auf die Spermidinsynthese und erhöhte Acylcarnitine, Zwischenüberträger, die Fette in die Mitochondrien transportieren, damit dort Energie erzeugt werden kann. Diese Veränderungen standen in engem Zusammenhang mit Verbesserungen sowohl der Gedächtnisleistung als auch der synaptischen Stärke, was darauf hindeutet, dass das Medikament dazu beiträgt, die mitochondriale Funktion in Gehirnzellen zu retten. Die Behandlung verschob auch andere Stoffwechselwege in einer Weise, die mit bekannten zellulären Signalwirkungen des Medikaments übereinstimmt: Förderung pro-überlebensfördernder Wege, Erhöhung von Serotonin, Unterstützung anti-entzündlicher Immunzustände im Gehirn und Verringerung von Nebenprodukten, die mit oxidativem Stress verbunden sind. Kurz gesagt: Das Medikament schien das gesamte Signalsystem in Richtung eines gesünderen, widerstandsfähigeren Zustands zu verschieben.
Was das für die zukünftige Alzheimer-Behandlung bedeuten könnte
Alltagsnah gesagt legt diese Arbeit nahe, dass das Wiederherstellen des inneren chemischen Gleichgewichts von Gehirnzellen—insbesondere der Lipide, die das Überleben der Zellen steuern, und der Brennstoffe, die die Mitochondrien speisen—einen Teil der durch Alzheimer-ähnliche Veränderungen geschädigten Gedächtnisfunktionen zurückgeben kann. Fingolimod überdeckte nicht einfach Symptome; in Mäusen korrigierte es zugrunde liegende metabolische Störungen, die mit synaptischer Gesundheit und Lernen verbunden sind. Zwar sind Mäuse keine Menschen und es sind weitere mechanistische und klinische Studien erforderlich, doch diese Ergebnisse heben einen vielversprechenden neuen therapeutischen Ansatz hervor: die Zielrichtung von Lipid- und Energiestoffwechsel über Sphingosin‑1‑phosphat-Rezeptoren und verwandte Wege, um neuronale Schaltkreise lange vor ihrem Versagen zu schützen.
Zitation: Kalecký, K., Buitrago, L., Alarcon, J.M. et al. Fingolimod normalizes metabolic signatures associated with synaptic plasticity and memory in APP/PS1 model: Sphingosine-1-phosphate receptor a therapeutic target for Alzheimer’s. Sci Rep 16, 12835 (2026). https://doi.org/10.1038/s41598-026-42518-8
Schlüsselwörter: Alzheimer-Krankheit, Gehirnstoffwechsel, Fingolimod, Sphingolipide, Mitochondrienfunktion