Clear Sky Science · it
Il fingolimod normalizza firme metaboliche associate alla plasticità sinaptica e alla memoria nel modello APP/PS1: il recettore della sfingosina-1-fosfato come bersaglio terapeutico per l’Alzheimer
Perché questa ricerca conta per le famiglie e i cervelli che invecchiano
La malattia di Alzheimer priva milioni di persone dei loro ricordi, eppure i farmaci disponibili oggi offrono solo un sollievo modesto e scarsa efficacia sui cambiamenti cerebrali di base. Questo studio esplora un alleato inaspettato: il fingolimod, un farmaco già impiegato nella sclerosi multipla. Analizzando come questo medicinale rimodelli la chimica cerebrale e migliori la memoria in un modello murino simile all’Alzheimer, i ricercatori propongono un nuovo approccio per proteggere le cellule cerebrali ripristinando la loro fornitura di energia e attenuando l’infiammazione dannosa.
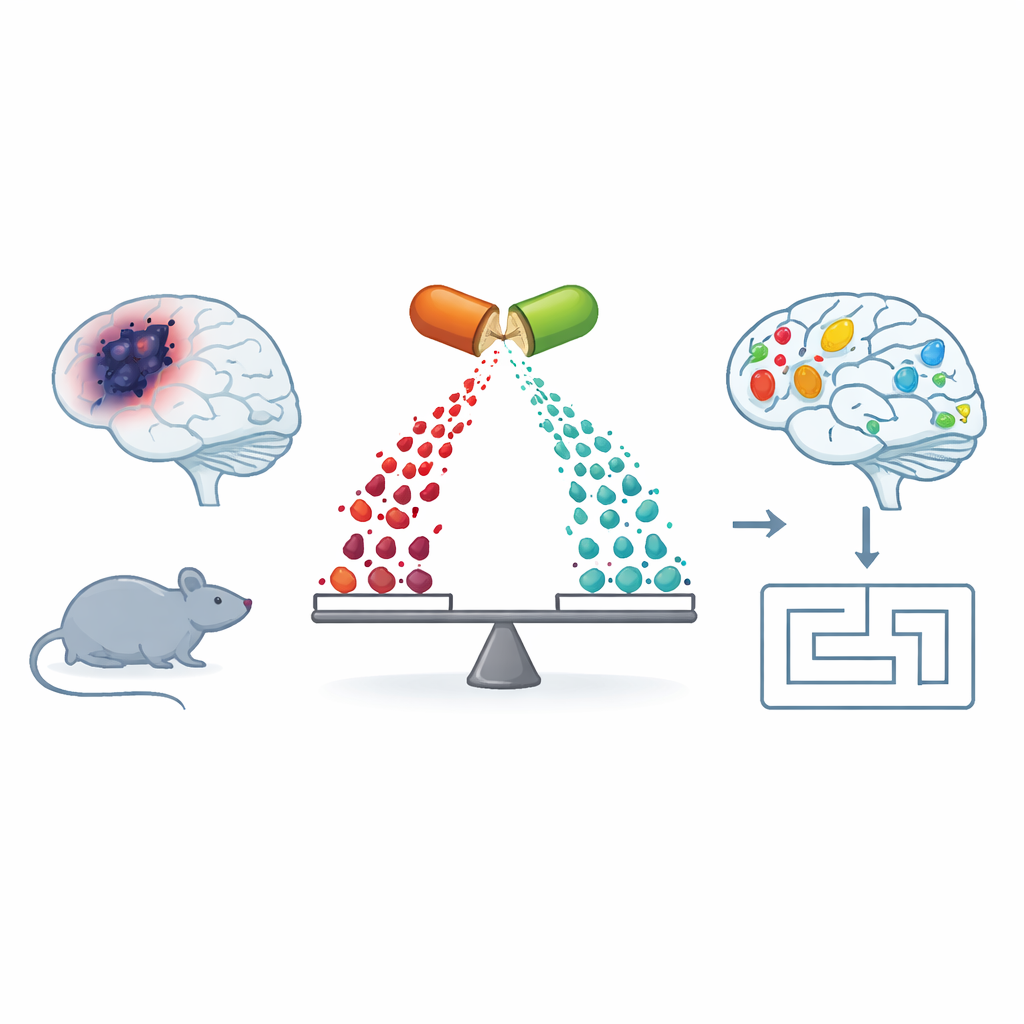
Uno sguardo più approfondito sull’Alzheimer oltre placche e grovigli
La maggior parte delle persone sa che le appiccicose placche di amiloide e i grovigli di tau sono segni distintivi dell’Alzheimer. Ma dietro questi segni visibili si cela un disturbo più silenzioso nella chimica cerebrale, in particolare nei grassi (lipidi) che costituiscono le membrane cellulari e trasmettono segnali fra le cellule. Il gruppo ha studiato topi che sviluppano cambiamenti simili all’Alzheimer (topi APP/PS1) e li ha confrontati con topi sani. Hanno misurato centinaia di piccole molecole nel cervello, nel sangue e nel fegato, trovando che i topi con caratteristiche Alzheimer mostravano ampi squilibri in diversi gruppi di molecole, inclusi lipidi specializzati e composti chiamati poliamine che aiutano a mantenere i mitocondri — le centrali energetiche delle cellule — funzionanti in modo regolare.
Quando l’equilibrio dei grassi cerebrali si sposta nella direzione sbagliata
Un focus importante era su un gruppo di lipidi chiamati sfingolipidi, che possono spingere le cellule verso la sopravvivenza o verso la morte a seconda del loro equilibrio. Nei topi simili all’Alzheimer questo “equilibrio lipidico” era sbilanciato verso molecole associate allo stress cellulare e all’infiammazione, mentre le forme protettive risultavano ridotte. Allo stesso tempo, i lipidi chiave per la costruzione delle membrane in regioni ricche di mitocondri delle cellule cerebrali erano alterati, e la produzione di spermidina e di poliamine correlate, che supportano la produzione di energia mitocondriale, era diminuita. Complessivamente questi cambiamenti indicano un ambiente cerebrale affamato di energia e incline all’infiammazione, che può compromettere le sinapsi — le giunzioni dove si codificano apprendimento e memoria.
Riprofilare un farmaco per la sclerosi multipla per resettare la chimica cerebrale
I ricercatori hanno quindi trattato i topi simili all’Alzheimer con fingolimod, un farmaco che agisce sui recettori di un messaggero lipidico chiamato sfingosina‑1‑fosfato. In lavori precedenti lo stesso gruppo aveva mostrato che questo trattamento migliorava l’apprendimento e la plasticità sinaptica (la capacità delle sinapsi di rafforzarsi con l’esperienza). Nel nuovo studio hanno confermato che il fingolimod ha ripristinato le prestazioni in un compito di memoria spaziale (il Barnes maze) e ha ravvivato la potenziamento a lungo termine, una firma elettrica chiave dell’apprendimento, in una importante via ippocampale. A livello chimico, il fingolimod ha aumentato i segnali sfingolipidici protettivi, ridotto i marcatori di ceramidi dannose e in larga misura ha invertito molti degli anomali schemi di saturazione lipidica nelle membrane cerebrali, in particolare nelle regioni della corteccia temporale legate alla memoria.
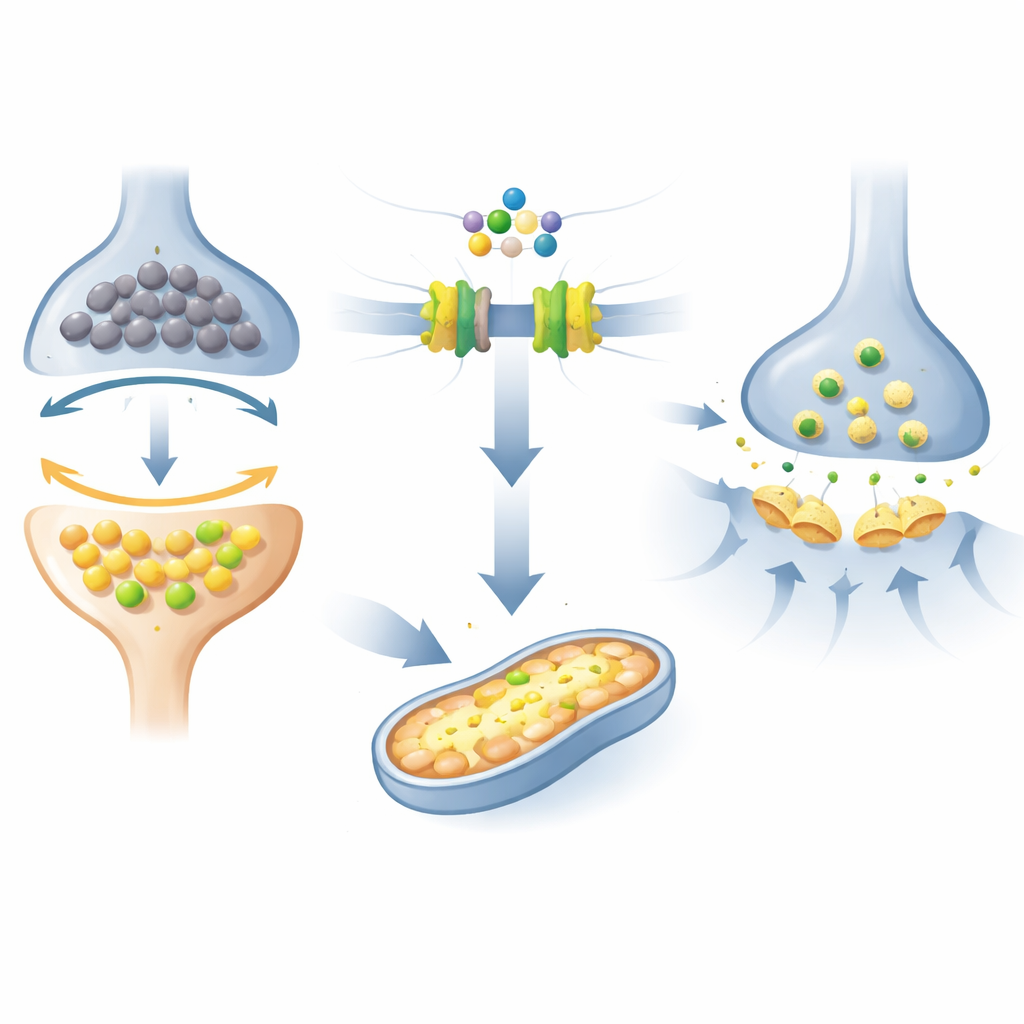
Ricaricare i mitocondri e stabilizzare i circuiti della memoria
Oltre a questi lipidi, il fingolimod ha aumentato gli indicatori della sintesi della spermidina e ha incrementato gli acilcarnitini, vettori intermedi che trasportano i grassi nei mitocondri per la produzione di energia. Questi cambiamenti erano strettamente correlati ai miglioramenti sia delle prestazioni mnemoniche sia della forza sinaptica, suggerendo che il farmaco aiuta a recuperare la funzione mitocondriale nelle cellule cerebrali. Il trattamento ha anche modificato altri percorsi metabolici in modi coerenti con gli effetti di segnalazione cellulare noti del farmaco: promuovendo vie pro‑sopravvivenza, aumentando la serotonina, favorendo stati immunitari antinfiammatori nel cervello e riducendo i sottoprodotti associati allo stress ossidativo. In breve, il farmaco sembrava spostare l’intera rete di segnali verso uno stato più sano e resiliente.
Cosa potrebbe significare per il trattamento futuro dell’Alzheimer
In termini pratici, questo lavoro suggerisce che aiutare le cellule cerebrali a riequilibrare la loro chimica interna — in particolare i lipidi che controllano la sopravvivenza cellulare e i combustibili che nutrono i mitocondri — può ripristinare alcune delle funzioni mnemoniche danneggiate da cambiamenti simili all’Alzheimer. Il fingolimod non ha semplicemente mascherato i sintomi; nei topi ha corretto disfunzioni metaboliche sottostanti legate alla salute sinaptica e all’apprendimento. Pur riconoscendo che i topi non sono esseri umani e che sono necessari ulteriori studi meccanicistici e clinici, questi risultati evidenziano un promettente nuovo angolo terapeutico: mirare al metabolismo dei lipidi e dell’energia, attraverso i recettori della sfingosina‑1‑fosfato e vie correlate, per proteggere i circuiti cerebrali molto prima che vengano compromessi.
Citazione: Kalecký, K., Buitrago, L., Alarcon, J.M. et al. Fingolimod normalizes metabolic signatures associated with synaptic plasticity and memory in APP/PS1 model: Sphingosine-1-phosphate receptor a therapeutic target for Alzheimer’s. Sci Rep 16, 12835 (2026). https://doi.org/10.1038/s41598-026-42518-8
Parole chiave: Malattia di Alzheimer, metabolismo cerebrale, fingolimod, sfingolipidi, funzione mitocondriale