Clear Sky Science · zh
基于MIEN1的六肽(LA3IK)通过破坏EGFR–ERBB2异二聚体抑制前列腺癌中的EGF驱动致癌信号
这对前列腺癌为何重要
晚期前列腺癌患者常常面临有效治疗选择枯竭的局面,尤其是当肿瘤对激素不再敏感时。本研究考察了一种实验室合成的小型分子——由六个氨基酸组成的肽LA3IK,旨在在不损伤健康组织的前提下关闭癌细胞常用的生长信号通路。弄清这种微型候选药物的作用机制,可能为侵袭性前列腺癌带来更安全、更具靶向性的治疗方向。
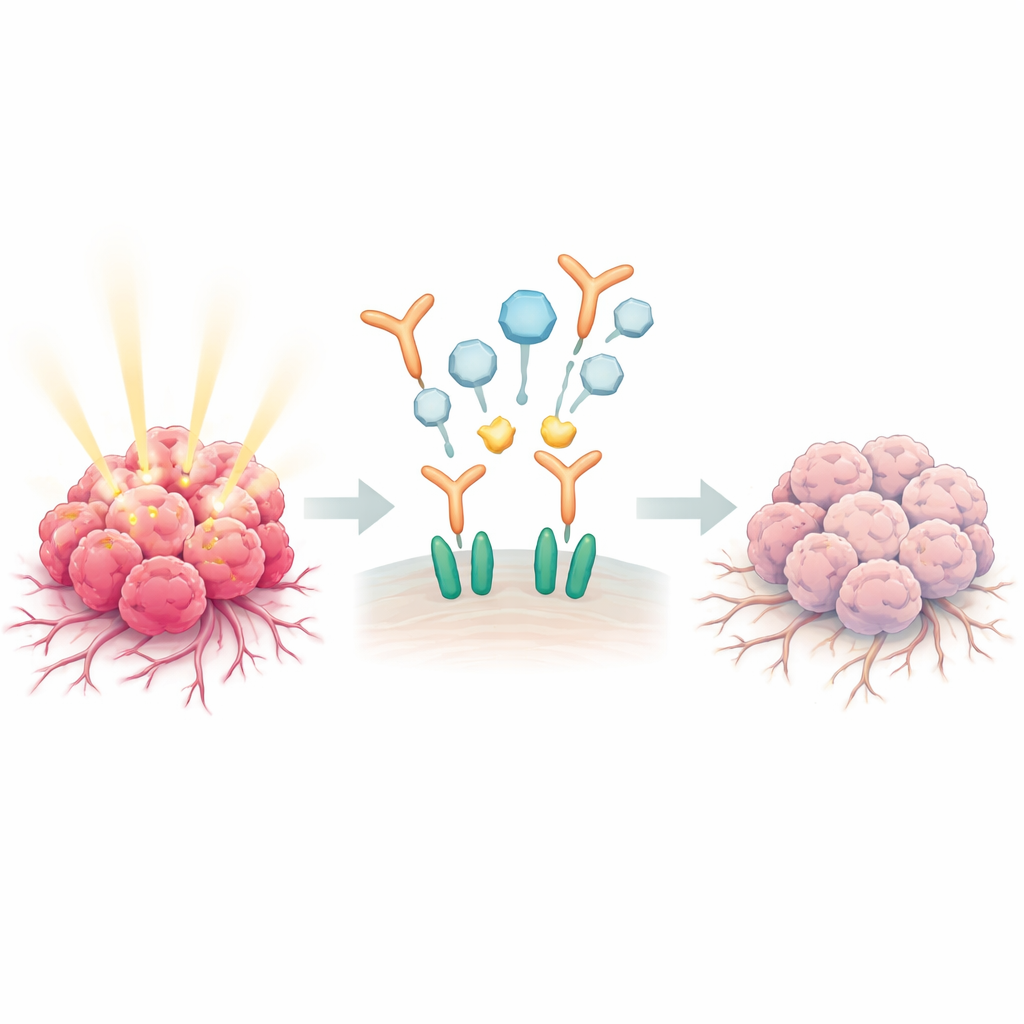
被癌细胞劫持的生长开关
许多前列腺肿瘤通过过度利用以表皮生长因子(EGF)及其受体EGFR为核心的细胞通讯系统变得高度侵袭性。当EGF与癌细胞表面的受体结合时,这些受体会与一个称为ERBB2的伙伴蛋白配对,形成强大的二聚体,进而发出促使细胞迁移、侵入邻近组织并吸引新血管的信号。在健康前列腺组织中,男性激素有助于抑制这一信号通路。但在晚期疾病中,这一制动失效,EGFR–ERBB2活性与复发、骨转移及治疗耐受性相关联。
具有精确靶点的小肽
研究人员基于一种与癌症相关的蛋白MIEN1设计了LA3IK,MIEN1已知可以促进细胞迁移与侵袭。早期研究表明LA3IK能削弱乳腺癌细胞中的有害信号,因此团队探究其是否也能抑制前列腺癌中由EGF驱动的通路。使用过表达EGFR并在体外表现出强侵袭性的PC3前列腺癌细胞,他们发现LA3IK并不是简单地直接杀死细胞,而更像一种定向的干扰者:它阻止EGFR–ERBB2二聚体的形成,并切断通常将EGFR及其下游伙伴置于“开启”状态的化学标记。
LA3IK如何破坏该信号
更深入的生化实验揭示了一个微妙但重要的特征:LA3IK能直接与EGF结合,并改变EGF中两处色氨酸残基周围的局部环境。这一微小的结构性推挤似乎削弱了EGF与EGFR–ERBB2配对有效结合的能力,尽管受体在细胞表面仍可形成更大的簇。结果是细胞内关键信使——如Src、STAT3、NF-κB和β-连环蛋白——的活化显著降低。在功能性测试中,这转化为癌细胞在人工屏障上的运动和侵袭明显减少,但存活细胞数量未见下降。LA3IK还下调了驱动血管生成的基因与分泌因子,包括ANGPTL4和VEGF家族成员,表明它可抑制肿瘤扩散并削弱肿瘤自我供养的能力。
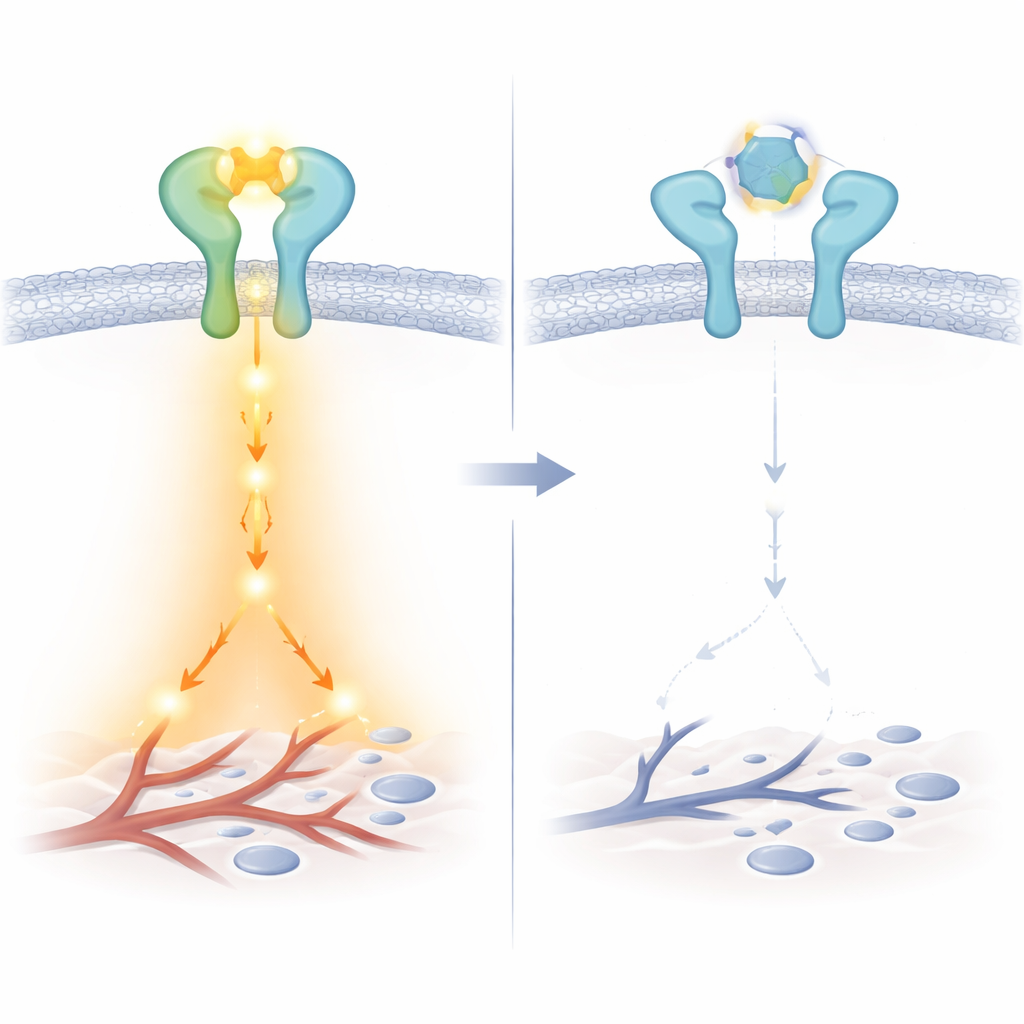
对肿瘤强效,对健康组织温和
针对EGFR的任何药物都存在一个重要担忧:连带损伤——该受体也在正常组织中发挥保护作用,尤其是肝脏。在接受EGF注射的小鼠中,LA3IK并未扰乱肝组织中保护性的EGFR信号,也未改变循环血液中EGFR水平。在细胞实验中,该肽对前列腺癌细胞的选择性高于一种标准EGFR抑制剂厄洛替尼(erlotinib),尤其是在一些常用癌细胞系中。这一表现提示LA3IK可能在癌症环境中更具特异性,原因可能在于其设计源自MIEN1——一种在肿瘤中丰度高而在正常细胞中稀少的蛋白。
这些发现对未来的意义
综合来看,结果将LA3IK呈现为一种异常短小的肽,能够在早期测试中在很大程度上保护健康组织的同时,削弱晚期前列腺癌中一个重要的生长与转移通路。LA3IK并非粗暴地破坏受体机械,而是通过微妙地重塑供能的生长因子并阻止最具侵袭性的受体配对形成来发挥作用。对患者而言,这一策略指向未来可减缓侵袭和血管生成且副作用较少的药物开发路径,为那些已失去激素治疗效应的肿瘤提供一种更精确的解除武装方式。
引用: Tripathi, A.K., Ahamad, N., Tyagi, A. et al. An MIEN1-based hexamer peptide (LA3IK) inhibits EGF-driven oncogenic signaling in prostate cancer by disrupting EGFR–ERBB2 heterodimerization. Sci Rep 16, 12295 (2026). https://doi.org/10.1038/s41598-026-41933-1
关键词: 前列腺癌, 生长因子信号, 肽类疗法, 肿瘤侵袭, 血管生成