Clear Sky Science · it
Un esamer peptidico basato su MIEN1 (LA3IK) inibisce la segnalazione oncogenica indotta da EGF nel carcinoma prostatico interrompendo l’etero-dimerizzazione EGFR–ERBB2
Perché è importante per il carcinoma prostatico
Negli uomini con carcinoma prostatico avanzato le opzioni terapeutiche efficaci spesso si esauriscono, soprattutto quando i tumori non rispondono più agli ormoni. Questo studio esplora una piccola molecola sintetica, un peptide di sei amminoacidi chiamato LA3IK, che mira a spegnere uno dei segnali di crescita preferiti dal cancro senza danneggiare i tessuti sani. Comprendere il meccanismo d’azione di questo candidato farmaco in miniatura potrebbe aprire la strada a terapie più sicure e altamente mirate per i carcinomi prostatici aggressivi.
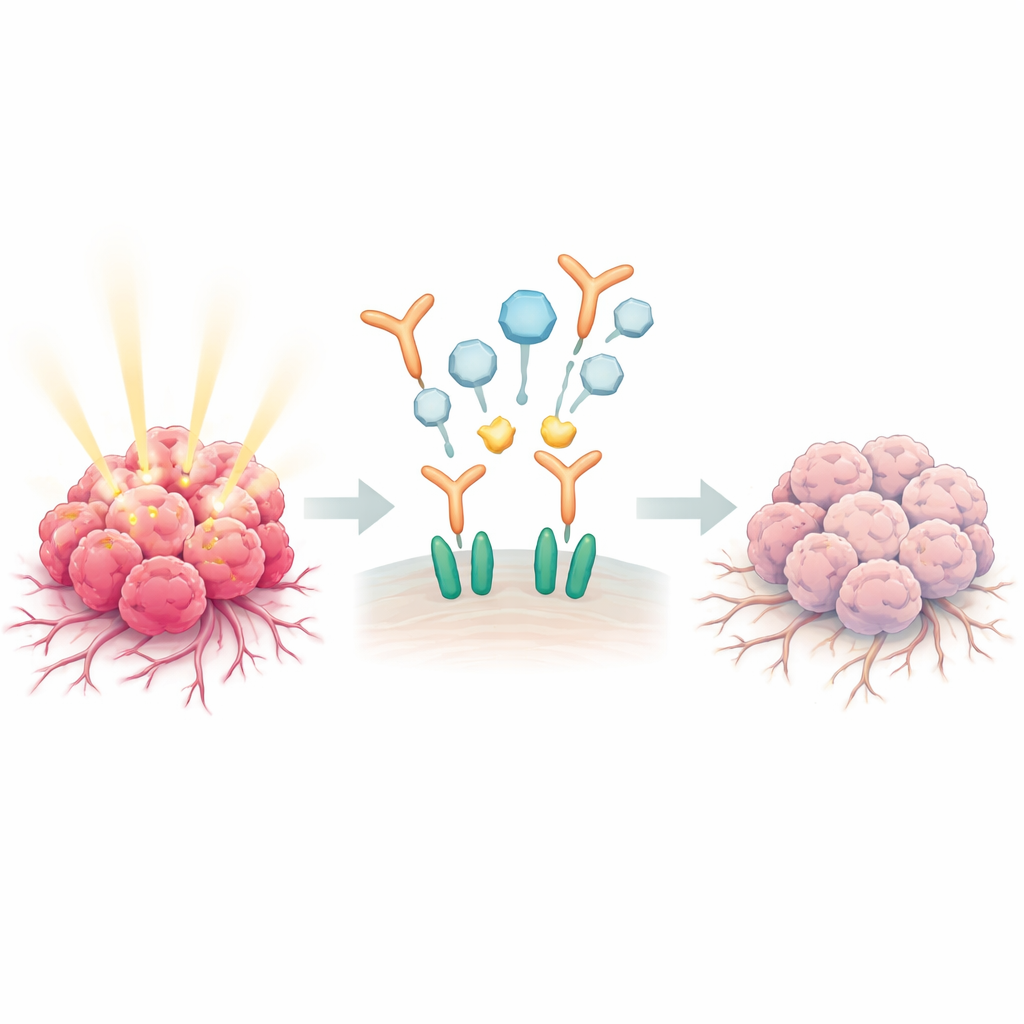
Un interruttore di crescita sfruttato dal cancro
Molti tumori prostatici diventano pericolosamente aggressivi sovrautilizzando un sistema di comunicazione naturale basato sul fattore di crescita epidermico (EGF) e sul suo recettore, EGFR. Quando l’EGF si lega ai recettori sulla superficie delle cellule tumorali, questi recettori si associano con una proteina partner chiamata ERBB2, formando coppie potenti che inviano comandi per la migrazione cellulare, l’invasione dei tessuti vicini e l’attrazione di nuovi vasi sanguigni. Nel tessuto prostatico sano, gli ormoni maschili contribuiscono a tenere sotto controllo questa segnalazione. Ma nella malattia avanzata questo freno viene meno e l’attività EGFR–ERBB2 è associata a recidiva, diffusione alle ossa e resistenza alle terapie.
Un peptide minuscolo con un bersaglio preciso
I ricercatori hanno costruito LA3IK a partire da una proteina associata al cancro chiamata MIEN1, nota per potenziare migrazione e invasione cellulare. Lavori precedenti avevano mostrato che LA3IK poteva attenuare segnali dannosi nelle cellule del carcinoma mammario, perciò il gruppo si è chiesto se potesse anche domare le vie indotte da EGF nel carcinoma prostatico. Utilizzando cellule di carcinoma prostatico PC3, che sovraesprimono EGFR e mostrano un comportamento aggressivo in laboratorio, hanno scoperto che LA3IK non uccide semplicemente le cellule. Piuttosto, agisce come un disruptor mirato: blocca la formazione delle coppie EGFR–ERBB2 e interrompe le modifiche chimiche che normalmente attivano EGFR e i suoi effettori a valle.
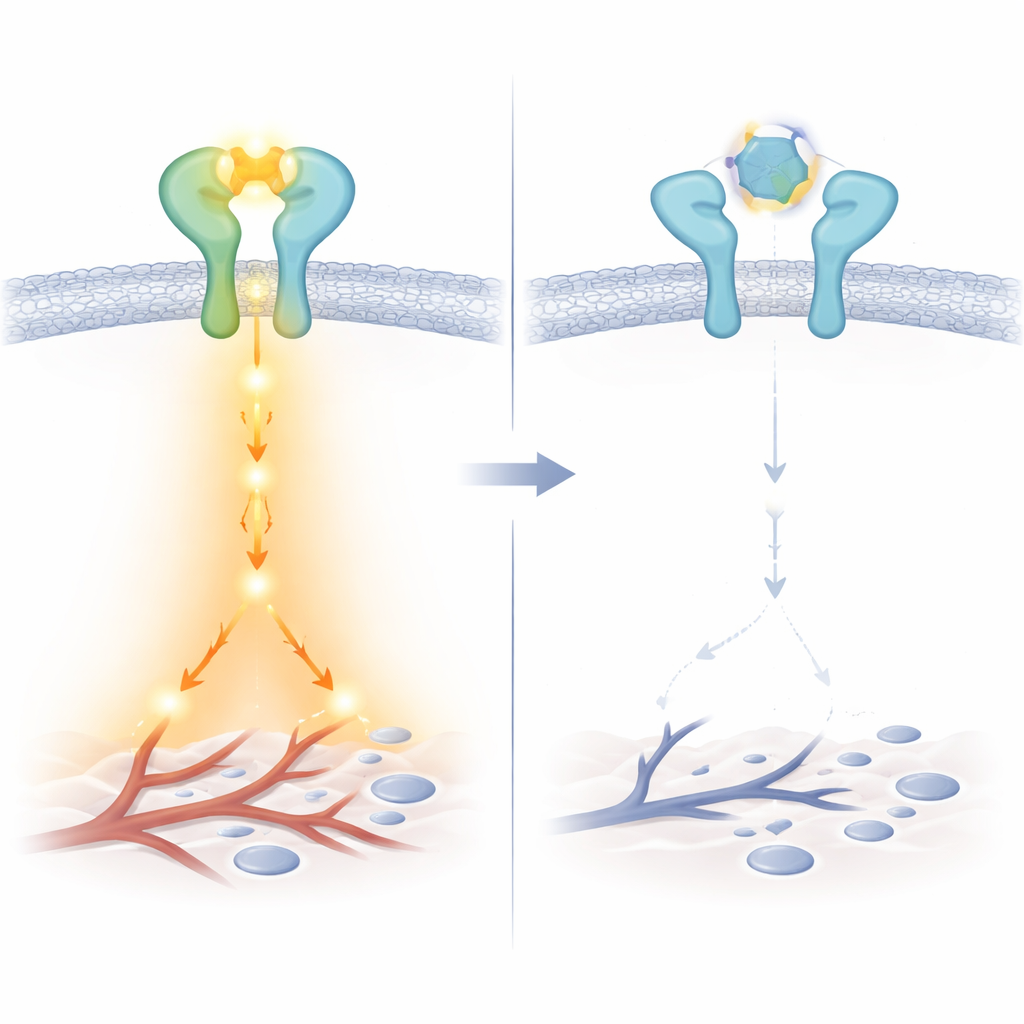
Come LA3IK interrompe la segnalazione
Esperimenti biochimici più dettagliati hanno rivelato una sfumatura importante: LA3IK si lega direttamente allo stesso EGF e altera l’ambiente locale intorno a due residui di triptofano di EGF. Questo piccolo spostamento strutturale sembra indebolire la capacità dell’EGF di coinvolgere efficacemente la coppia EGFR–ERBB2, anche se i recettori possono ancora aggregarsi in cluster più ampi sulla superficie cellulare. Di conseguenza, messaggeri chiave all’interno della cellula — come Src, STAT3, NF-κB e beta-catenina — risultano molto meno attivati. Nei test funzionali, ciò si è tradotto in una marcata riduzione della motilità e dell’invasione delle cellule tumorali attraverso barriere artificiali, senza diminuire il numero di cellule vive. LA3IK ha inoltre ridotto l’espressione di geni e fattori secretori che promuovono la crescita vascolare, inclusi ANGPTL4 e membri della famiglia VEGF, suggerendo la capacità di attenuare sia la diffusione che la capacità del tumore di nutrirsi.
Azione marcata sui tumori, impatto lieve sui tessuti sani
Una preoccupazione importante con qualsiasi farmaco che prende di mira EGFR è il danno collaterale: questo recettore protegge anche i tessuti normali, in particolare il fegato. In topi sottoposti a iniezioni di EGF, LA3IK non ha alterato i segnali protettivi mediati da EGFR nel tessuto epatico, né ha modificato i livelli di EGFR circolante nel sangue. Nei test in vitro, il peptide è risultato più selettivo per le cellule del carcinoma prostatico rispetto a una pillola standard che blocca EGFR, erlotinib, soprattutto in alcune linee tumorali ampiamente utilizzate. Questo profilo suggerisce che LA3IK agisca preferenzialmente nel contesto tumorale, probabilmente perché è stato progettato a partire da MIEN1, una proteina abbondante nei tumori ma scarsa nelle cellule normali.
Cosa significano i risultati per il futuro
Nel complesso, i risultati presentano LA3IK come un peptide insolitamente corto in grado di attenuare una via chiave di crescita e diffusione nel carcinoma prostatico avanzato, risparmiando in gran parte i tessuti sani, almeno nei test iniziali. Piuttosto che demolire il macchinario recettoriale, LA3IK rimodella sottilmente il fattore di crescita che lo alimenta e impedisce la formazione delle associazioni recettoriali più aggressive. Per i pazienti, questa strategia indica la possibilità di farmaci futuri che rallentino invasione e angiogenesi con effetti collaterali minori, offrendo un modo più preciso per disarmare tumori che hanno superato i trattamenti ormonali standard.
Citazione: Tripathi, A.K., Ahamad, N., Tyagi, A. et al. An MIEN1-based hexamer peptide (LA3IK) inhibits EGF-driven oncogenic signaling in prostate cancer by disrupting EGFR–ERBB2 heterodimerization. Sci Rep 16, 12295 (2026). https://doi.org/10.1038/s41598-026-41933-1
Parole chiave: carcinoma prostatico, segnalazione dei fattori di crescita, terapia con peptidi, invasione tumorale, angiogenesi