Clear Sky Science · de
Ein auf MIEN1 basierendes Hexamer-Peptid (LA3IK) hemmt EGF‑vermittelte onkogene Signalwege beim Prostatakrebs durch Störung der EGFR–ERBB2‑Heterodimerisierung
Warum das für Prostatakrebs wichtig ist
Männer mit fortgeschrittenem Prostatakrebs haben oft nur noch wenige wirksame Behandlungsoptionen, besonders wenn Tumoren nicht mehr auf Hormontherapien ansprechen. Diese Studie untersucht ein winziges, im Labor synthetisiertes Molekül, ein sechs Aminosäuren langes Peptid namens LA3IK, das darauf abzielt, eines der bevorzugten Wachstumssignale des Krebses abzuschalten, ohne gesunde Gewebe zu schädigen. Zu verstehen, wie dieser miniaturisierte Wirkstoffkandidat funktioniert, könnte den Weg zu sichereren, hochspezifischen Therapien für aggressiven Prostatakrebs ebnen.
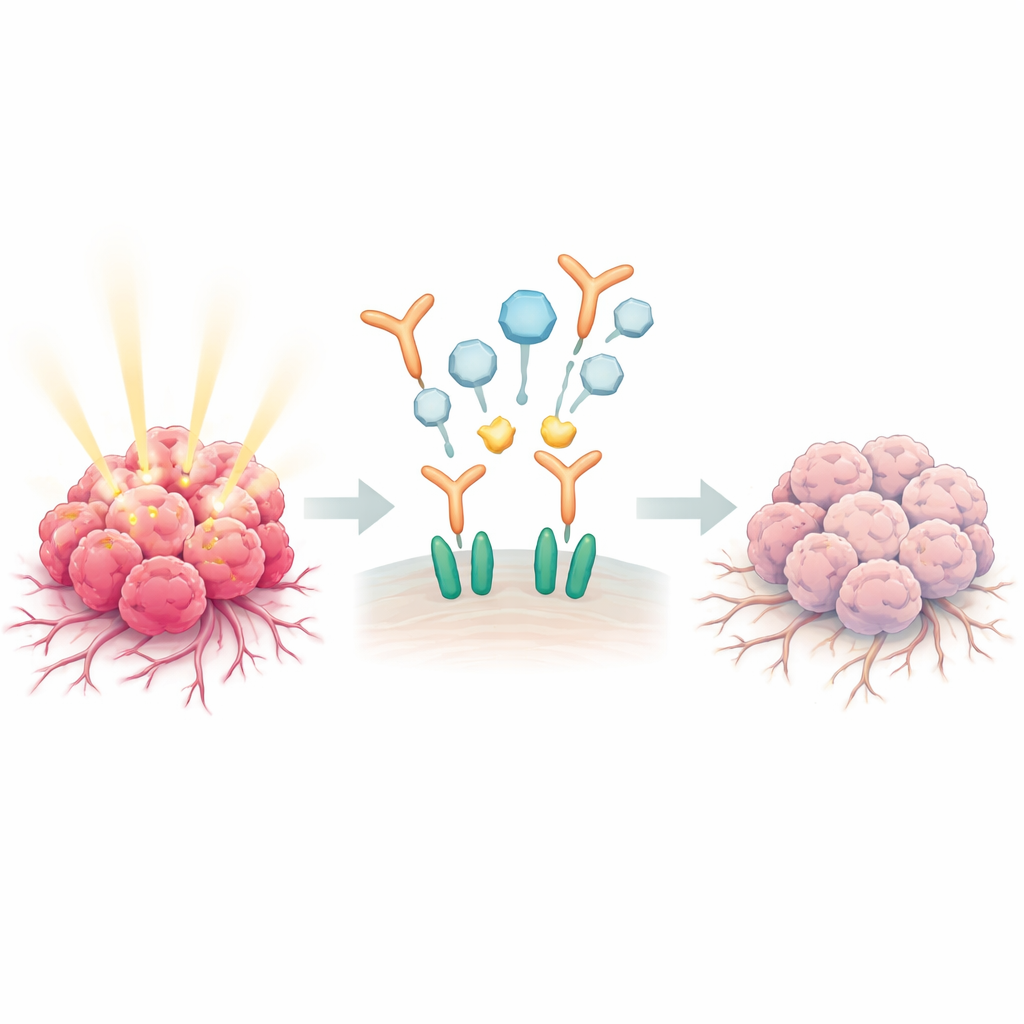
Ein Wachstumsschalter, den Krebs kapert
Viele Prostatatumoren werden gefährlich aggressiv, indem sie ein natürliches Kommunikationssystem um den epidermalen Wachstumsfaktor (EGF) und seinen Rezeptor EGFR übernutzen. Wenn EGF an Rezeptoren auf der Oberfläche von Krebszellen bindet, koppeln sich diese Rezeptoren mit einem Partnerprotein namens ERBB2 und bilden mächtige Paare, die Signale zum Bewegen, Infiltrieren benachbarter Gewebe und Anlocken neuer Blutgefäße aussenden. Im gesunden Prostatagewebe halten männliche Hormone diese Signalgebung in Schach. Bei fortgeschrittener Erkrankung versagt diese Bremsfunktion jedoch, und eine erhöhte EGFR–ERBB2‑Aktivität wird mit Rückfall, Knochenmetastasen und Therapie‑Resistenz in Verbindung gebracht.
Ein winziges Peptid mit präzisem Ziel
Die Forschenden leiteten LA3IK von einem krebsassoziierten Protein namens MIEN1 ab, das dafür bekannt ist, Zellmigration und Invasion zu fördern. Frühere Arbeiten zeigten, dass LA3IK schädliche Signale in Brustkrebszellen dämpfen kann, weshalb das Team untersuchte, ob es auch EGF‑getriebene Wege beim Prostatakrebs bändigen könnte. An PC3‑Prostatakrebszellen, die EGFR überproduzieren und im Labor aggressiv auftreten, zeigte sich, dass LA3IK die Zellen nicht einfach abtötet. Stattdessen wirkt es wie ein gezielter Störer: Es blockiert die Bildung von EGFR–ERBB2‑Paaren und unterbindet die chemischen Markierungen, die normalerweise EGFR und seine nachgeschalteten Partner in den „ein“-Zustand versetzen.
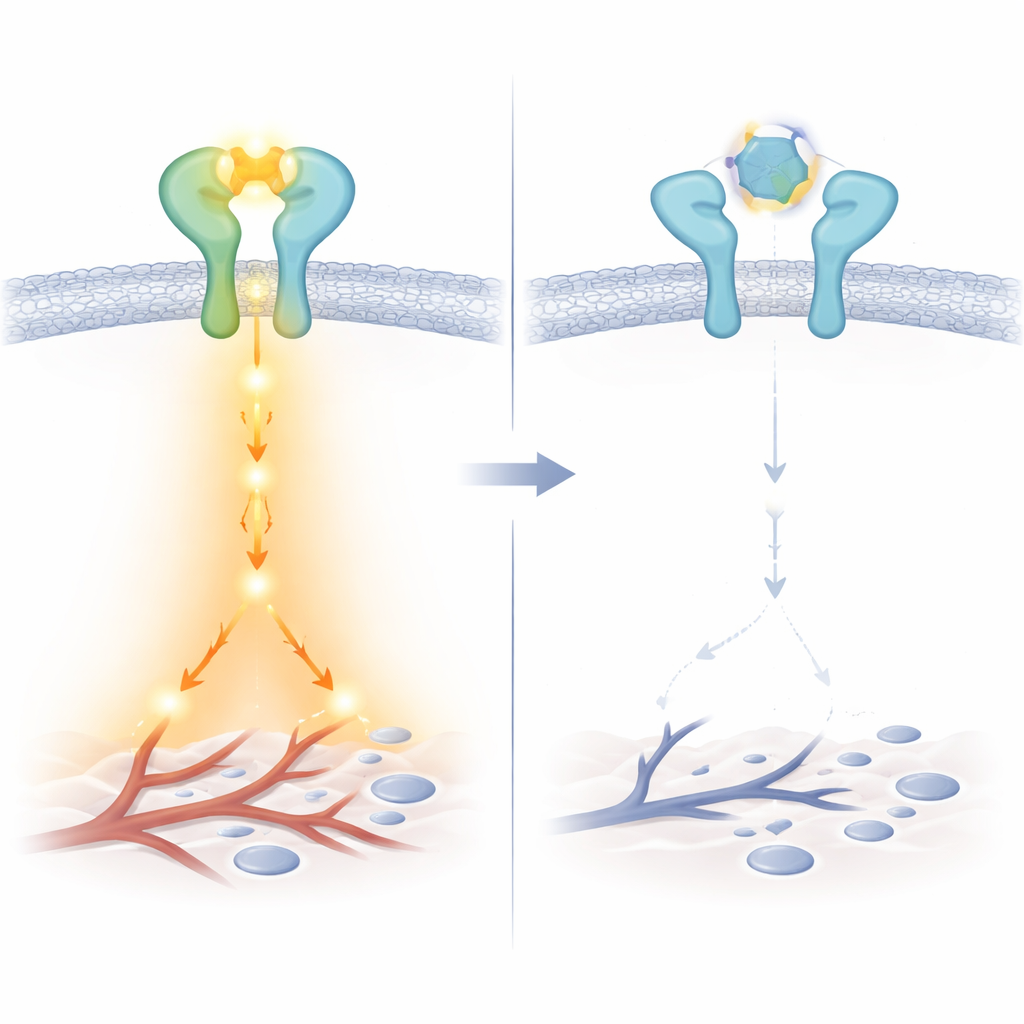
Wie LA3IK das Signal stört
Nähere biochemische Untersuchungen zeigten eine subtile, aber wichtige Wendung: LA3IK bindet direkt an EGF selbst und verändert die lokale Umgebung um zwei Tryptophan‑Bausteine von EGF. Dieser kleine strukturelle Impuls scheint die Fähigkeit von EGF zu schwächen, wirksam mit dem EGFR–ERBB2‑Paar zu interagieren, obwohl die Rezeptoren weiterhin größere Cluster auf der Zelloberfläche bilden können. Infolgedessen sind zentrale Botenstoffe in der Zelle — etwa Src, STAT3, NF‑κB und Beta‑Catenin — deutlich weniger aktiviert. In funktionellen Tests führte dies zu stark reduziertem Zellbewegungs‑ und Invasionsverhalten durch künstliche Barrieren, ohne die Anzahl lebender Zellen zu verringern. LA3IK senkte außerdem die Expression von Genen und sezernierten Faktoren, die das Gefäßwachstum fördern, einschließlich ANGPTL4 und Mitgliedern der VEGF‑Familie, was darauf hindeutet, dass es sowohl die Ausbreitung als auch die Nahrungsversorgung des Tumors abschwächen kann.
Starke Wirkung auf Tumoren, schonender Umgang mit gesundem Gewebe
Eine wichtige Sorge bei jedem Wirkstoff, der EGFR anvisiert, ist Kollateralschaden: Dieser Rezeptor schützt auch normales Gewebe, insbesondere die Leber. Bei Mäusen, die EGF‑Injektionen erhielten, störte LA3IK die schützenden EGFR‑Signale im Lebergewebe nicht und veränderte auch nicht die zirkulierenden EGFR‑Spiegel im Blut. In zellbasierten Tests war das Peptid selektiver für Prostatakrebszellen als ein Standard‑EGFR‑Blocker, Erlotinib, insbesondere in einigen weit verbreiteten Zelllinien. Dieses Muster legt nahe, dass LA3IK bevorzugt im Tumorumfeld wirkt, vermutlich weil es von MIEN1 abgeleitet wurde — einem Protein, das in Tumoren reichlich vorhanden, in normalen Zellen jedoch selten ist.
Was die Ergebnisse für die Zukunft bedeuten
Insgesamt stellen die Befunde LA3IK als ein ungewöhnlich kurzes Peptid vor, das einen wichtigen Weg für Wachstum und Ausbreitung bei fortgeschrittenem Prostatakrebs abschwächen kann, während es gesundes Gewebe weitgehend verschont — zumindest in frühen Versuchen. Anstatt die Rezeptormaschinerie vollständig zu zerstören, formt LA3IK den Wachstumsfaktor, der sie speist, leicht um und verhindert so die Bildung der aggressivsten Rezeptorpaarungen. Für Patientinnen und Patienten weist diese Strategie auf künftige Medikamente hin, die Invasion und Angiogenese verlangsamen könnten, bei gleichzeitig geringeren Nebenwirkungen, und bietet einen präziseren Ansatz, um Tumore zu entwaffnen, die hormonsystemische Therapien überholt haben.
Zitation: Tripathi, A.K., Ahamad, N., Tyagi, A. et al. An MIEN1-based hexamer peptide (LA3IK) inhibits EGF-driven oncogenic signaling in prostate cancer by disrupting EGFR–ERBB2 heterodimerization. Sci Rep 16, 12295 (2026). https://doi.org/10.1038/s41598-026-41933-1
Schlüsselwörter: Prostatakrebs, Wachstumsfaktorsignalgebung, Peptidtherapie, Tumorinvasion, Angiogenese