Clear Sky Science · pl
Heksamerowy peptyd oparty na MIEN1 (LA3IK) hamuje onkogeniczne sygnalizowanie napędzane przez EGF w raku prostaty przez zakłócanie heterodimeryzacji EGFR–ERBB2
Dlaczego to ma znaczenie dla raka prostaty
Mężczyźni z zaawansowanym rakiem prostaty często kończą leczenie skutecznymi opcjami, zwłaszcza gdy guzy przestają reagować na terapie hormonalne. W badaniu tym analizowano niewielką, syntetyczną cząsteczkę — sześciokw asowy peptyd nazwany LA3IK — mającą na celu wyłączyć jeden z ulubionych sygnałów wzrostu nowotworu, nie szkodząc tkankom zdrowym. Zrozumienie mechanizmu działania tego miniaturowego kandydata na lek może otworzyć drogę do bezpieczniejszych, wysoce ukierunkowanych terapii agresywnego raka prostaty.
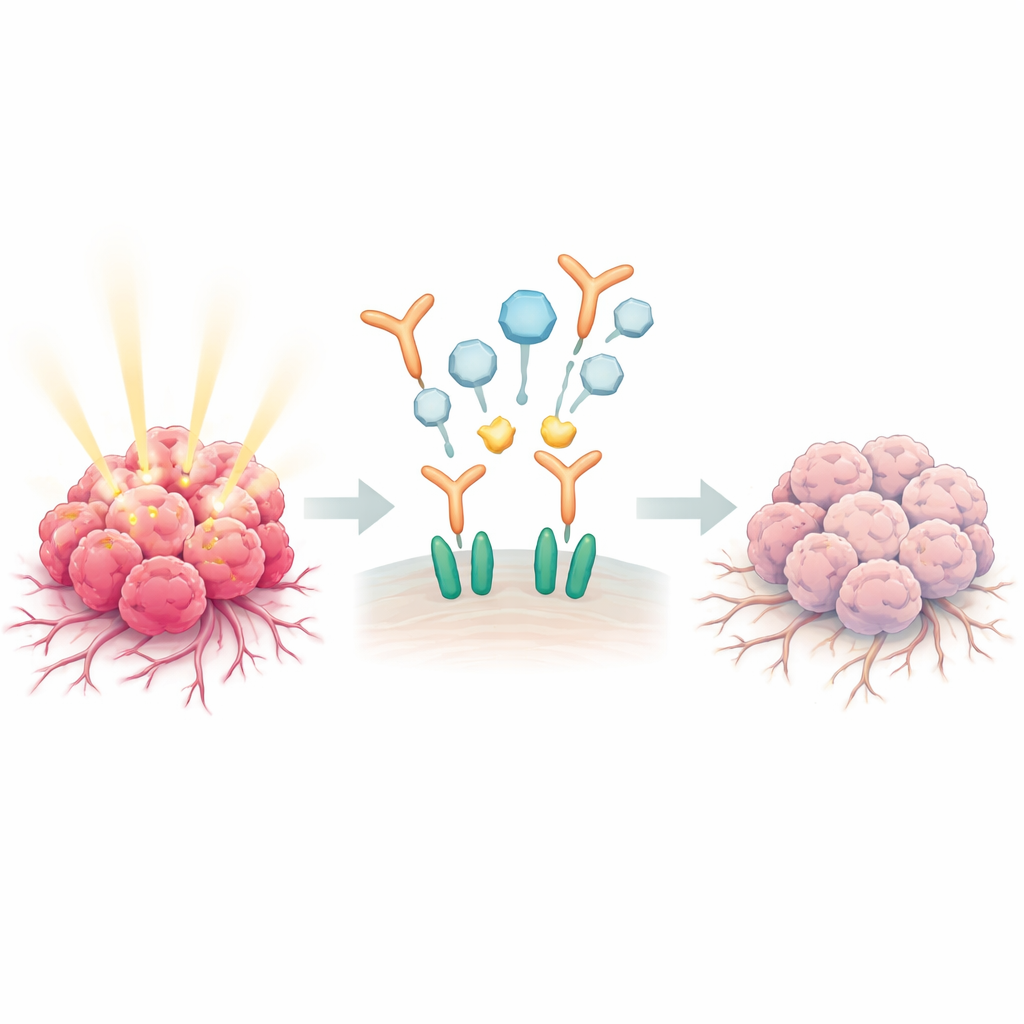
Włącznik wzrostu przejmowany przez nowotwór
Wiele nowotworów prostaty staje się niebezpiecznie agresywnych przez nadużywanie naturalnego systemu komunikacji opartego na naskórkowym czynniku wzrostu (EGF) i jego receptorze EGFR. Gdy EGF łączy się z receptorami na powierzchni komórek nowotworowych, receptory te tworzą pary z białkiem towarzyszącym ERBB2, tworząc potężne zespoły wysyłające polecenia do komórek, by się przemieszczały, naciekały sąsiednie tkanki i przyciągały nowe naczynia krwionośne. W zdrowej tkance prostaty hormony męskie pomagają powstrzymywać tę sygnalizację. Jednak w chorobie zaawansowanej mechanizm hamujący zawodzi, a aktywność EGFR–ERBB2 wiąże się z nawrotem, przerzutami do kości i opornością na leczenie.
Malutki peptyd o precyzyjnym celu
Naukowcy zbudowali LA3IK w oparciu o białko związane z rakiem o nazwie MIEN1, które jest znane z nasilania migracji i inwazji komórek. Wcześniejsze badania wykazały, że LA3IK potrafi stłumić szkodliwe sygnały w komórkach raka piersi, więc zespół sprawdził, czy może też okiełznać szlaki napędzane przez EGF w raku prostaty. Używając komórek PC3, które nadprodukują EGFR i wykazują agresywne zachowanie in vitro, odkryli, że LA3IK nie zabija komórek bezpośrednio. Działa raczej jak ukierunkowany disruptor: blokuje tworzenie par EGFR–ERBB2 i przerywa dodawanie chemicznych znaczników, które normalnie włączają EGFR i jego partnerów w dół szlaku.
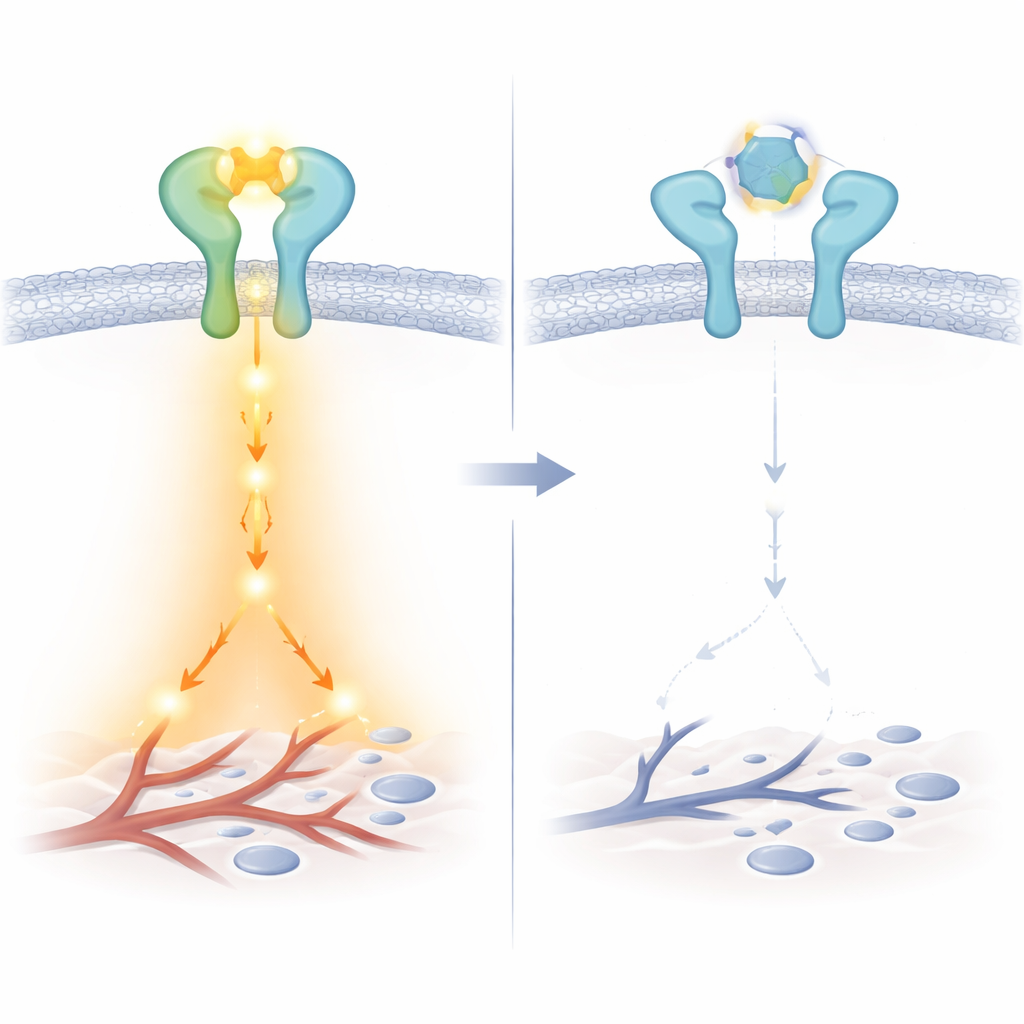
Jak LA3IK zakłóca sygnał
Bardziej szczegółowe badania biochemiczne ujawniły subtelny, lecz istotny zwrot: LA3IK wiąże się bezpośrednio z samym EGF i zmienia lokalne otoczenie wokół dwóch tryptofanów tego czynnika. Ten drobny strukturalny impuls wydaje się osłabiać skuteczność, z jaką EGF angażuje parę EGFR–ERBB2, mimo że receptory wciąż mogą tworzyć większe skupiska na powierzchni komórki. W efekcie kluczowe przekaźniki wewnątrzkomórkowe — takie jak Src, STAT3, NF-κB i beta-katenina — są znacznie mniej aktywowane. W testach funkcjonalnych przekładało się to na wyraźnie zmniejszoną migrację i inwazję komórek nowotworowych przez sztuczne bariery, bez redukcji liczby żywych komórek. LA3IK obniżał też ekspresję genów i wydzielanych czynników napędzających wzrost naczyń, w tym ANGPTL4 i członków rodziny VEGF, co sugeruje, że może tłumić zarówno rozprzestrzenianie się, jak i zdolność guza do odżywiania się.
Mocny efekt na guzy, łagodny wpływ na tkanki zdrowe
Istotnym problemem przy każdym leku ukierunkowanym na EGFR jest uszkodzenie tkanek zdrowych: ten receptor chroni też normalne narządy, zwłaszcza wątrobę. U myszy otrzymujących wstrzyknięcia EGF, LA3IK nie zakłócał ochronnych sygnałów EGFR w tkance wątroby ani nie zmieniał poziomów EGFR krążącego we krwi. W testach na liniach komórkowych peptyd był bardziej selektywny wobec komórek raka prostaty niż standardowy doustny inhibitor EGFR, erlotynib, szczególnie w niektórych powszechnie stosowanych liniach nowotworowych. Ten wzorzec sugeruje, że LA3IK działa preferencyjnie w kontekście nowotworu, prawdopodobnie dlatego, że został zaprojektowany na bazie MIEN1 — białka obficie występującego w guzach, ale rzadkiego w komórkach normalnych.
Co znaczą te wyniki na przyszłość
Podsumowując, wyniki przedstawiają LA3IK jako wyjątkowo krótki peptyd zdolny stłumić ważny szlak wzrostu i rozprzestrzeniania się w zaawansowanym raku prostaty, jednocześnie w dużej mierze oszczędzając tkanki zdrowe, przynajmniej w wczesnych testach. Zamiast całkowicie niszczyć aparaturę receptorową, LA3IK subtelnie przekształca czynnik wzrostu, który ją napędza, i zapobiega tworzeniu się najbardziej agresywnych par receptorowych. Dla pacjentów ta strategia wskazuje kierunek rozwoju leków spowalniających inwazję i angiogenezę przy mniejszych skutkach ubocznych, oferując bardziej precyzyjny sposób unieszkodliwiania guzów, które wymknęły się spod kontroli standardowych terapii hormonalnych.
Cytowanie: Tripathi, A.K., Ahamad, N., Tyagi, A. et al. An MIEN1-based hexamer peptide (LA3IK) inhibits EGF-driven oncogenic signaling in prostate cancer by disrupting EGFR–ERBB2 heterodimerization. Sci Rep 16, 12295 (2026). https://doi.org/10.1038/s41598-026-41933-1
Słowa kluczowe: rak prostaty, sygnalizacja czynników wzrostu, terapia peptydowa, inwazja guza, angiogeneza