Clear Sky Science · zh
羟考酮自我给药与遗传背景对肠道微生物群的群落特异性影响
为什么你的肠道可能在意止痛药
处方止痛药如羟考酮被广泛使用,但其影响不仅限于缓解疼痛或增加成瘾风险——它们还深入作用于肠道。本研究提出了一个看似简单却意义重大的问题:我们的基因和阿片类药物使用如何共同重塑肠内数万亿微生物?通过测验两种不同的大鼠品系在自我给药羟考酮的情况下,研究者表明遗传构成和药物使用都会在肠道微生物群上留下清晰但具有群落特异性的指纹。 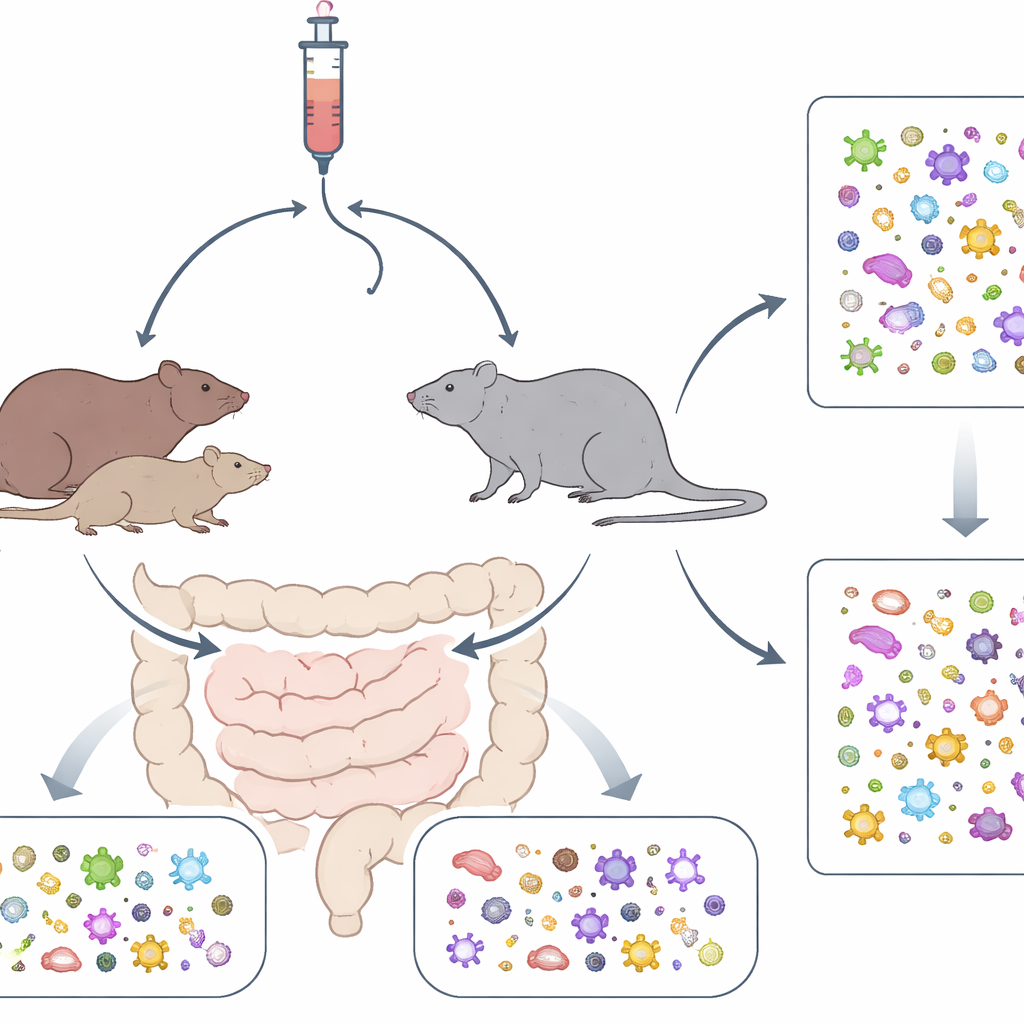
两类大鼠,一种强效药物
研究团队使用了两种遗传差异显著的近交大鼠品系。雄性与雌性大鼠都被训练按杆以静脉注射羟考酮或无害的生理盐水,模拟人类的自愿用药行为。数周内,动物先进行短时接触,然后延长到更长的给药时段,使其摄入量得以上升。其中一品系称为 M520/N,持续摄入的羟考酮量高于 ACI/EurMcwi 品系,凸显出遗传背景可以强烈影响个体选择摄入药物的多少。即便杠杆只发放生理盐水,品系和性别仍然起作用:M520/N 雌鼠按杆的次数超过其他任何组,表明天生特质不仅能影响寻药行为,也会塑造对刺激的普遍偏好。
过程中的体重与肠道健康追踪
研究者在这一高强度实验期间监测体重,作为整体健康状况的简单指标。在长时接触阶段,自我给药羟考酮的大鼠相比接受生理盐水的同伴倾向于体重下降,且雄性下降幅度大于雌性。因为饮食和体重变化已知会改变肠道细菌,这些变化很可能与羟考酮对肠道的直接作用相互作用,增加了药物如何重塑微生物群的复杂性。在最后一次给药后,团队采集了两个关键肠道区域的样本——粪便(反映结肠)和盲肠(微生物尤其密集的囊袋)——以观察每个群落如何改变。
遗传与性别塑造微生物多样性
为了解微生物群落的丰富性与多样性,科学家测量了每个样本内的不同多样性指标。在粪便和盲肠群落中,遗传背景和性别都产生了显著影响。总体上,ACI/EurMcwi 大鼠与雌性倾向于拥有比 M520/N 大鼠与雄性更丰富多样的细菌群落。有趣的是,单纯服用羟考酮并未降低样本内的这种多样性,意味着微生物的总数和进化广度在总体上保持相似。然而,当研究者比较不同动物间哪些细菌存在以及它们的丰度时,按品系以及是否接受羟考酮或生理盐水出现了明显分离。这表明尽管肠道总体上仍然“繁忙”,但具体的参与者及其相对平衡强烈受到遗传和药物暴露的影响。 
群落特异性的肠道细菌变化
更深入分析中,团队识别出随羟考酮使用变化或在品系间不同的特定细菌类群。总体而言,有15个细菌类群将服用羟考酮的大鼠与生理盐水对照组区分开来,51个类群在两种品系间存在差异。一些模式在肠道区域间共享——例如某些属如 Blautia、Prevotella 和 Rodentibacter 在粪便和盲肠样本中在羟考酮使用者中都变得更常见。其他变化则高度群落特异:一个名为 Patescibacteria 的细菌门在盲肠中随羟考酮减少,但在粪便中并未见下降,且许多类群在两个区域的变化方向相反。细菌的共存倾向以及形成相互作用网络的方式也随品系和药物而改变,表明羟考酮和遗传因素不仅改变了哪些微生物存在,还改变了它们之间的关系。
这对人类与镇痛药意味着什么
总体而言,该研究表明我们的遗传构成和阿片类药物暴露可以共同以微妙但广泛的方式重塑肠道生态系统,这些影响在肠道不同区域间存在差异。遗传背景影响大鼠选择摄入羟考酮的多少,也强烈决定了哪些微生物在其肠道中繁盛。羟考酮使用随后在微生物组成和微生物网络上叠加了额外的、群落特异性的变化,即便总体多样性并未大幅下降。对于人来说,这意味着两位服用相同止痛药的个体,可能因其基因和既有微生物群的不同而经历截然不同的肠道乃至大脑后果。理解这些基因—微生物—药物相互作用,或可帮助解释为何部分患者更易发生阿片类药物使用障碍或出现胃肠副作用,并可能最终指导更个性化的治疗策略,以保护或甚至利用肠道微生物群。
引用: Duffy, E.P., Sterrett, J.D., Hale, L.H. et al. Oxycodone self-administration and genetic background exert community-specific effects in the gut microbiome. Sci Rep 16, 13276 (2026). https://doi.org/10.1038/s41598-026-41666-1
关键词: 阿片类药物使用障碍, 肠道微生物群, 羟考酮, 遗传背景, 大鼠自我给药