Clear Sky Science · ru
Самоадминистрирование оксикодона и генетический фон оказывают специфичные для сообществ эффекты на микробиом кишечника
Почему вашему кишечнику может быть не все равно на обезболивающие
Рецептурные обезболивающие, такие как оксикодон, широко применяются, но их действие выходит за рамки снятия боли или риска зависимости — они также глубоко влияют на кишечник. В этом исследовании задается на первый взгляд простой, но важный вопрос: как наши гены и употребление опиоидов вместе перестраивают триллионы микробов, живущих в кишечнике? На двух разных штаммах крыс, которые самоадминистрировали оксикодон, исследователи показали, что и генетический состав, и прием препарата оставляют четкие, но специфичные для сообществ отпечатки на микробиоме кишечника. 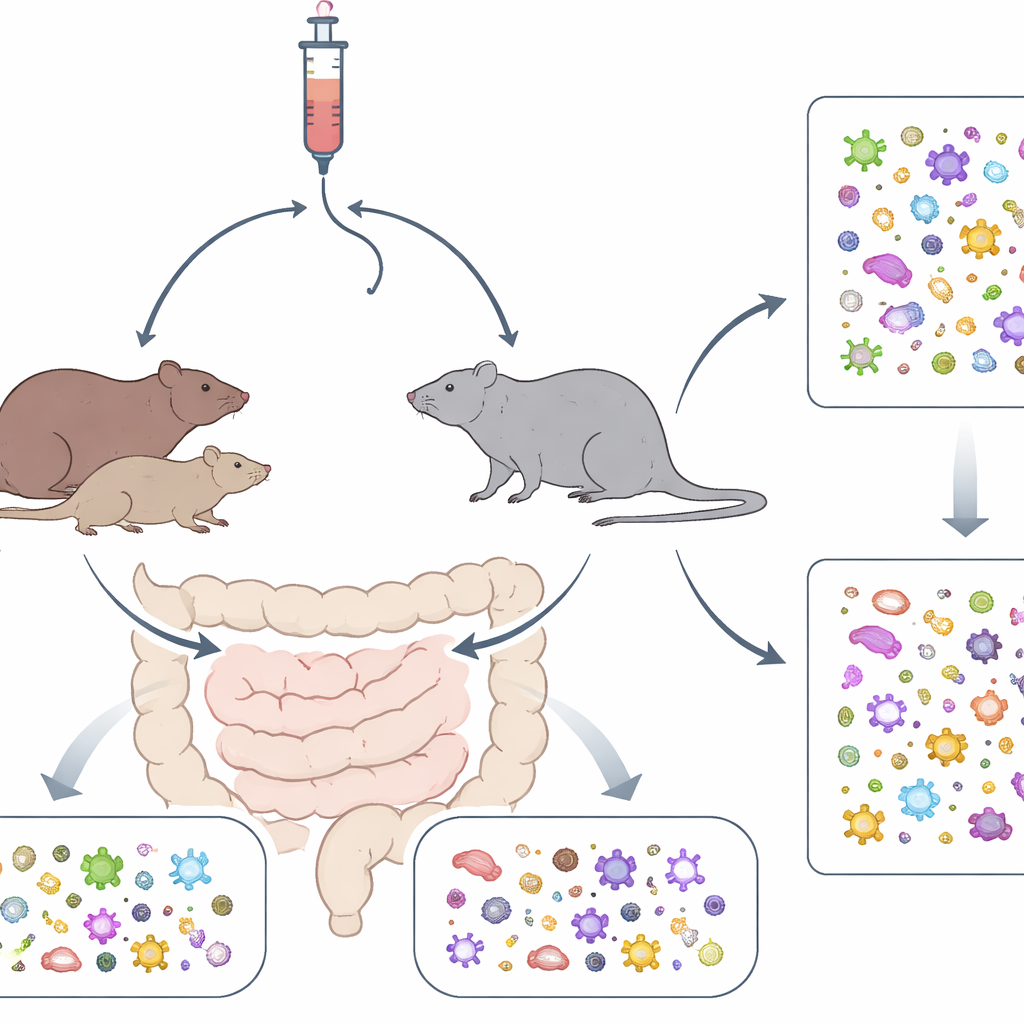
Два типа крыс, один мощный препарат
Команда работала с двумя инбредными штаммами крыс, которые генетически существенно различаются. Самцов и самок обучали нажимать рычаг, чтобы ввести себе внутривенно оксикодон или нейтральный физиологический раствор, моделируя добровольное потребление наркотика у людей. На протяжении недель у животных сначала был короткий доступ, а затем значительно более длительные сессии, что позволило их приему возрасти. Один штамм, называемый M520/N, постоянно потреблял больше оксикодона, чем штамм ACI/EurMcwi, что подчеркивает, что генетический фон может сильно влиять на количество вещества, которое индивидуум выбирает принять. Даже когда рычаг выдавал только физиологический раствор, имелись различия по штамму и полу: самки M520/N нажимали рычаг чаще, чем другие группы, что говорит о том, что врожденные черты могут формировать не только поиск наркотика, но и общую склонность к стимуляции.
Отслеживание массы тела и здоровья кишечника по ходу эксперимента
Исследователи контролировали массу тела как простой показатель общего состояния здоровья в течение этой требовательной схемы. В фазе длительного доступа крысы, самоадминистрировавшие оксикодон, как правило, теряли вес по сравнению с контрольными, получавшими физиологический раствор, и самцы теряли больше, чем самки. Поскольку диета и изменения веса известны как факторы, изменяющие состав кишечной микробиоты, эти сдвиги, вероятно, взаимодействуют с прямыми эффектами оксикодона на кишечник, добавляя еще один уровень сложности в том, как препарат перестраивает микробиом. После финальных сессий команда собрала пробы из двух ключевых зон кишечника — фекалий (отражающих состояние толстой кишки) и слепой кишки (цекума), мешка, где микроорганизмов особенно много — чтобы увидеть, как изменились сообщества в каждой области.
Гены и пол формируют микробную разнообразность
Чтобы понять, насколько богаты и разнообразны микробные сообщества, ученые измеряли различные формы разнообразия в каждой пробе. В фекальных и цекальных сообществах генетический фон и пол оказывали сильное влияние. В целом у крыс ACI/EurMcwi и у самок наблюдалась более высокая внутренняя разнообразность бактериальных сообществ, чем у M520/N и самцов. Интересно, что сам по себе прием оксикодона не снижал это внутриобразцовое разнообразие, то есть общее число и эволюционная широта микробов оставались примерно схожими. Однако при сравнении того, какие бактерии присутствовали и в каких количествах у разных животных, наблюдалось четкое разделение по штамму и по тому, получали ли крысы оксикодон или физиологический раствор. Это показывает, что хотя кишечник в целом может оставаться «загруженным», конкретные участники сообщества и их соотношения сильно формируются и генетикой, и воздействием препарата. 
Специфичные для сообществ сдвиги в составе бактерий кишечника
Углубившись, команда выявила конкретные группы бактерий, которые менялись при приеме оксикодона или различались между штаммами. В целом 15 бактериальных групп отличали крыс, принимающих оксикодон, от контролей с физиологическим раствором, а 51 группа отличалась между двумя штаммами. Некоторые закономерности были общими для областей кишечника — например, роды Blautia, Prevotella и Rodentibacter становились более распространенными у принимающих оксикодон и в фекальных, и в цекальных образцах. Другие изменения оказались строго специфичными для сообщества: фило Patescibacteria снижалось в цекуме после оксикодона, но не в фекалиях, и многие таксоны смещались в противоположных направлениях в двух регионах. То, как бактерии склонны сосуществовать и формировать сети взаимодействий, также менялось в зависимости от штамма и препарата, что указывает на то, что оксикодон и генетика изменяют не только присутствие микробов, но и их взаимосвязи.
Что это значит для людей и болеутоляющих
В сумме исследование показывает, что наш генетический фон и воздействие опиоидов совместно могут перестраивать кишечную экосистему тонкими, но распространенными способами, при этом эти эффекты различаются между регионами кишечника. Генетика влияла на то, сколько оксикодона крысы выбирали принять, и также существенно определяла, какие микробы преобладали в их кишечнике. Прием оксикодона накладывал дополнительные, специфичные для сообщества сдвиги в составе микробов и в сетях их взаимодействий, даже без крупных падений общей разнообразности. Для людей это означает, что два пациента, получающие одно и то же обезболивающее, могут испытать очень разные кишечные и, возможно, мозговые последствия в зависимости от их генов и исходного микробиома. Понимание этих взаимодействий «гены–микробы–препарат» может помочь объяснить, почему некоторые пациенты более уязвимы к расстройствам, связанным с употреблением опиоидов, или к желудочно‑кишечным побочным эффектам, и в перспективе способствовать более персонализированным подходам лечения, защищающим или даже использующим микробиоту кишечника.
Цитирование: Duffy, E.P., Sterrett, J.D., Hale, L.H. et al. Oxycodone self-administration and genetic background exert community-specific effects in the gut microbiome. Sci Rep 16, 13276 (2026). https://doi.org/10.1038/s41598-026-41666-1
Ключевые слова: расстройство, связанное с употреблением опиоидов, микробиом кишечника, оксикодон, генетический фон, самоадминистрирование у крыс