Clear Sky Science · ar
الإدارة الذاتية للأوكسيكودون والخلفية الجينية تؤثران بآثار مميزة على مجتمع الميكروبيوم المعوي
لماذا قد يهتم جهازك الهضمي بأقراص المسكنات
تُستخدم مسكنات الألم الموصوفة مثل الأوكسيكودون على نطاق واسع، لكن آثارها لا تقتصر على تخفيف الألم أو خطر الإدمان—بل تصل أيضاً إلى عمق الأمعاء. تطرح هذه الدراسة سؤالاً بسيطاً في الظاهر لكن له تبعات كبيرة: كيف تعيد جيناتنا واستخدام الأفيونات معاً تشكيل التريليونات من الميكروبات التي تعيش في أمعائنا؟ من خلال اختبار سلالتين مختلفتين من الفئران اللواتي قدمن لأنفسهن جرعات من الأوكسيكودون، يُظهر الباحثون أن كلّاً من التركيب الجيني وتعاطي الدواء يتركان آثاراً واضحة، وإن كانت خاصة بكل مجتمع ميكروبي معيّن، على ميكروبيوم الأمعاء. 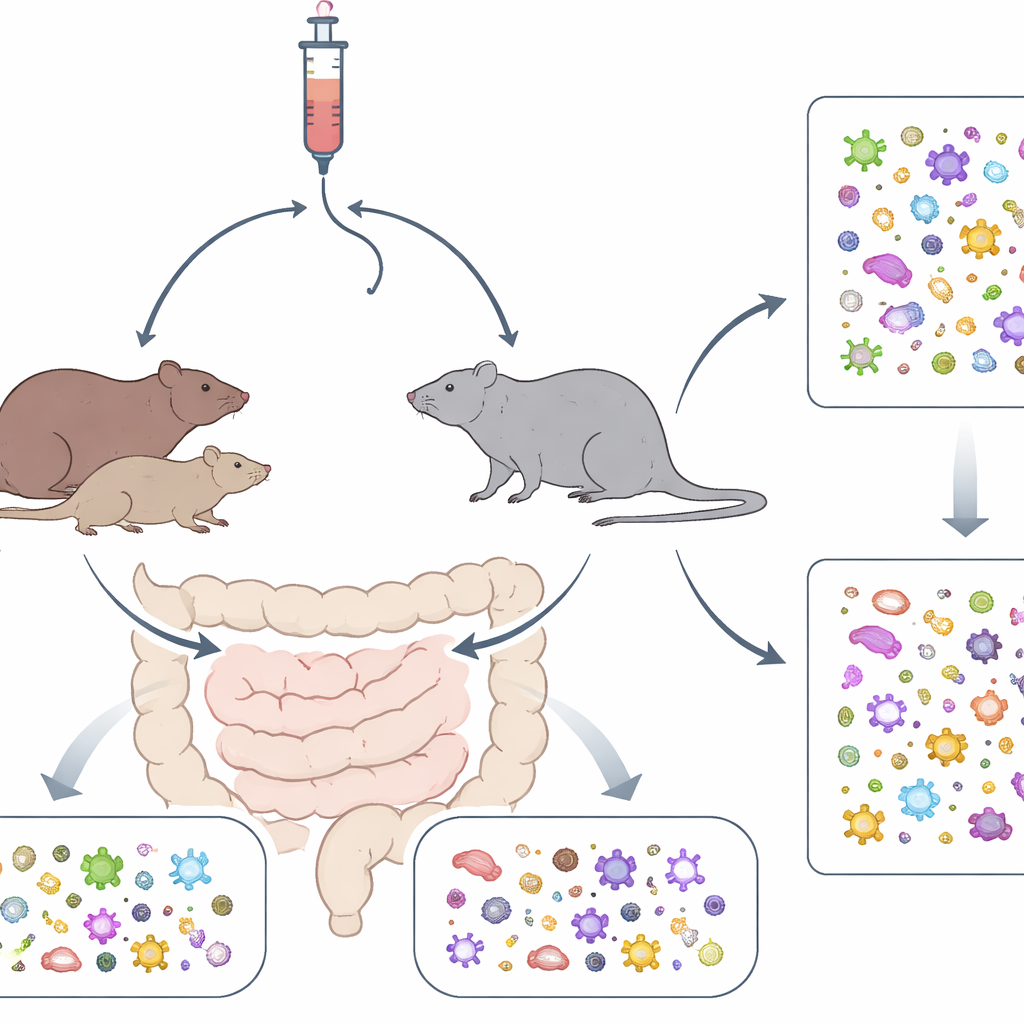
فئران من نوعين ودواء قوي واحد
عمل الفريق مع سلالتين متنخلتين من الفئران تختلفان وراثياً إلى حد بعيد. تم تدريب كل من الفئران والإناث ليركضن على ذراع ليفعلن بأنفسهن حقنًا وريدية من الأوكسيكودون أو محلول ملحي غير مؤذٍ، مقلدين التعاطي الإرادي لدى البشر. على مدى أسابيع، خضعت الحيوانات أولاً لجلسات ذات وصول قصير ثم لجلسات أطول بكثير، مما أتاح لتناول الدواء أن يتصاعد. سلالة واحدة، تسمى M520/N، استهلكت باستمرار كمية أكبر من الأوكسيكودون مقارنة بسلالة ACI/EurMcwi، مما يبرز أن الخلفية الجينية يمكن أن تؤثر بقوة على مقدار الدواء الذي يختار الفرد تناوله. وحتى عندما كان الذراع لا يمد سوى بالمحلول الملحي، بقيت السلالة والجنس مؤثرين: ضغطت الإناث من سلالة M520/N على الذراع أكثر من أي مجموعة أخرى، مما يشير إلى أن الصفات الفطرية يمكن أن تشكل ليس فقط السعي وراء المخدرات وإنما أيضاً الميل العام نحو التحفيز.
تتبُّع الوزن وصحة الأمعاء على طول التجربة
راقب الباحثون وزن الجسم كمؤشر بسيط على الصحة العامة خلال هذا النظام المرهق. خلال مرحلة الوصول الطويل، فقدت الفئران التي تناولت الأوكسيكودون وزناً مقارنةً بنظيراتها التي تلقت المحلول الملحي، وفقد الذكور مزناً أكثر من الإناث. وبما أن النظام الغذائي وتقلبات الوزن معروف أنها تغير بكتيريا الأمعاء، فمن المرجح أن هذه التغيرات تتداخل مع التأثيرات المباشرة للأوكسيكودون على الأمعاء، مضيفةً طبقة أخرى من التعقيد للطريقة التي يعيد بها الدواء تشكيل الميكروبيوم. بعد الجلسات الأخيرة من التعاطي، جمع الفريق عينات من منطقتين أساسيتين في الأمعاء—البراز (الذي يعكس القولون) والردب المعوي (cecum)، وهو جيب تكون فيه الميكروبات مكثفة بشكل خاص—ليروا كيف تغيّرت كل مجموعة ميكروبية.
الجينات والجنس يشكلان تنوّع الميكروبات
لفهم مدى غنى وتنوّع المجتمعات الميكروبية، قاس العلماء أشكالاً مختلفة من التنوع داخل كل عينة. في كل من مجتمعات البراز والردب، كان للخلفية الجينية والجنس تأثيرات قوية. عموماً، استضافت فئران ACI/EurMcwi والإناث مجتمعات بكتيرية أكثر تنوعاً مقارنةً بفئران M520/N والذكور. ومن المثير للاهتمام أن مجرد تناول الأوكسيكودون لم يخفض هذا التنوع داخل العينة، ما يعني أن العدد الإجمالي ونطاق الانتواع التطوري للميكروبات بقيا متشابهين إلى حدٍ كبير. ومع ذلك، عندما قارن الباحثون أي البكتيريا كانت موجودة وإلى أي مدى كانت وفيرة عبر الحيوانات، لاحظوا انفصالاً واضحاً بحسب السلالة وبحسب ما إذا كانت الفئران قد تلقت الأوكسيكودون أم المحلول الملحي. وهذا يدل على أنه بينما تبقى الأمعاء عموماً «مزدحمة»، فإن الفاعلين المحددين وتوازنهم يتشكلان بشدة بواسطة كلٍ من الجينات والتعرض للدواء. 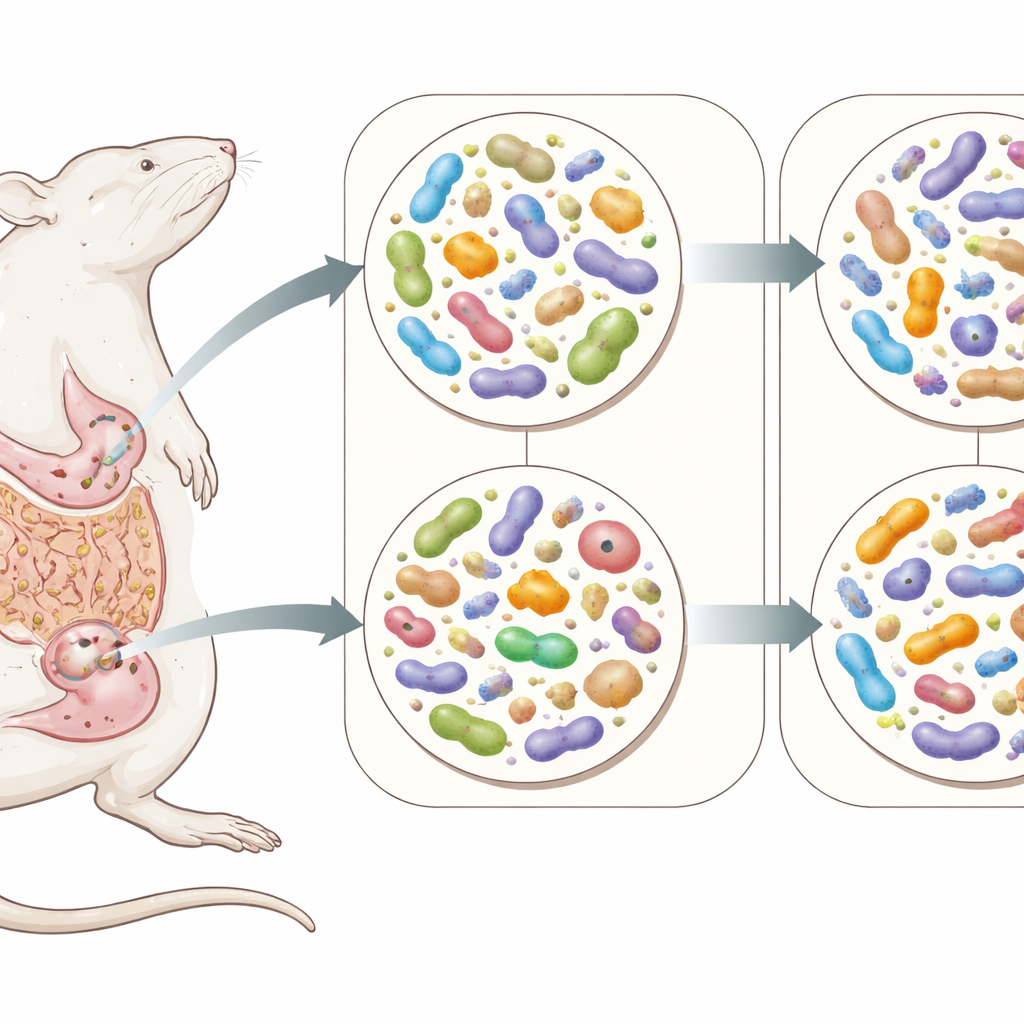
تحولات خاصة بكل مجتمع في بكتيريا الأمعاء
بالتعمق أكثر، حدّد الفريق مجموعات بكتيرية معينة تغيرت مع الأوكسيكودون أو اختلفت بين السلالات. عموماً، فرّقت 15 مجموعة بكتيرية بين الفئران المتعاطية للأوكسيكودون والضوابط المتلقية للمحلول الملحي، ووجدت 51 مجموعة اختلفت بين السلالتين. كانت بعض الأنماط مشتركة عبر مناطق الأمعاء—على سبيل المثال ازداد تكرار أجناس معينة مثل Blautia وPrevotella وRodentibacter في مستخدمي الأوكسيكودون في كلٍ من عينات البراز والردب. تغييرات أخرى كانت خاصة جداً بكل مجتمع: انخفض فرع بكتيري يسمى Patescibacteria في الردب بعد الأوكسيكودون، لكنه لم ينخفض في البراز، وتحركت العديد من الأصناف في اتجاهات معاكسة في المنطقتين. كما تغيرت طريقة تعايش البكتيريا وتشكيلها لشبكات تفاعلية مع بعضهم البعض بحسب كلٍ من السلالة والدواء، مما يشير إلى أن الأوكسيكودون والجينات لا يغيران فقط أي الميكروبات موجودة، بل أيضاً كيف ترتبط هذه الميكروبات ببعضها البعض.
ماذا يعني هذا للناس وطب الألم
بشكلٍ مجمل، تُظهر الدراسة أن تركيبتنا الجينية والتعرض للأفيونات يمكن أن يعيدا تشكيل النظام البيئي المعوي بطرق دقيقة لكن واسعة النطاق، وأن هذه التأثيرات تختلف بين مناطق الأمعاء. أثرت الخلفية الجينية على مقدار الأوكسيكودون الذي اختارت الفئران تناوله، وشكلت أيضاً بقوة أي الميكروبات ازدهرت في أحشائها. ثم طرأ على ذلك استخدام الأوكسيكودون تغيرات إضافية خاصة بكل مجتمع في تركيب الميكروبات وشبكاتها، حتى دون انخفاضات كبيرة في التنوع العام. بالنسبة للبشر، يوحي هذا بأن شخصين موصوف لهما نفس دواء الألم قد يختبران عواقب معوية وربما دماغية مختلفة جداً اعتماداً على جيناتهما والميكروبيوم السابق لهما. قد يساعد فهم هذه التفاعلات بين الجين–الميكروب–الدواء في تفسير سبب تعرض بعض المرضى بشكل أكبر لاضطراب استخدام الأفيونات أو للآثار الجانبية المعوية، وقد يوجه مستقبلاً علاجات أكثر تخصيصاً تحمي أو تستفيد من ميكروبيوم الأمعاء.
الاستشهاد: Duffy, E.P., Sterrett, J.D., Hale, L.H. et al. Oxycodone self-administration and genetic background exert community-specific effects in the gut microbiome. Sci Rep 16, 13276 (2026). https://doi.org/10.1038/s41598-026-41666-1
الكلمات المفتاحية: اضطراب استخدام المواد الأفيونية, ميكروبيوم الأمعاء, أوكسيكودون, الخلفية الجينية, التناوُل الذاتي لدى الفئران