Clear Sky Science · it
Autoconsumo di ossicodone e background genetico esercitano effetti specifici per comunità sul microbioma intestinale
Perché il tuo intestino potrebbe interessarsi alle pillole per il dolore
Gli analgesici da prescrizione come l'ossicodone sono ampiamente usati, ma i loro effetti non si limitano ad alleviare il dolore o a creare rischio di dipendenza: raggiungono anche l'intestino in profondità. Questo studio pone una domanda apparentemente semplice ma di grande portata: come rimodellano insieme i nostri geni e l'uso di oppioidi i trilioni di microbi che vivono nel nostro intestino? Testando due ceppi distinti di ratti che si autoconsumevano ossicodone, i ricercatori dimostrano che sia il patrimonio genetico sia l'uso del farmaco lasciano chiari, seppur specifici per comunità, segni distintivi sul microbioma intestinale. 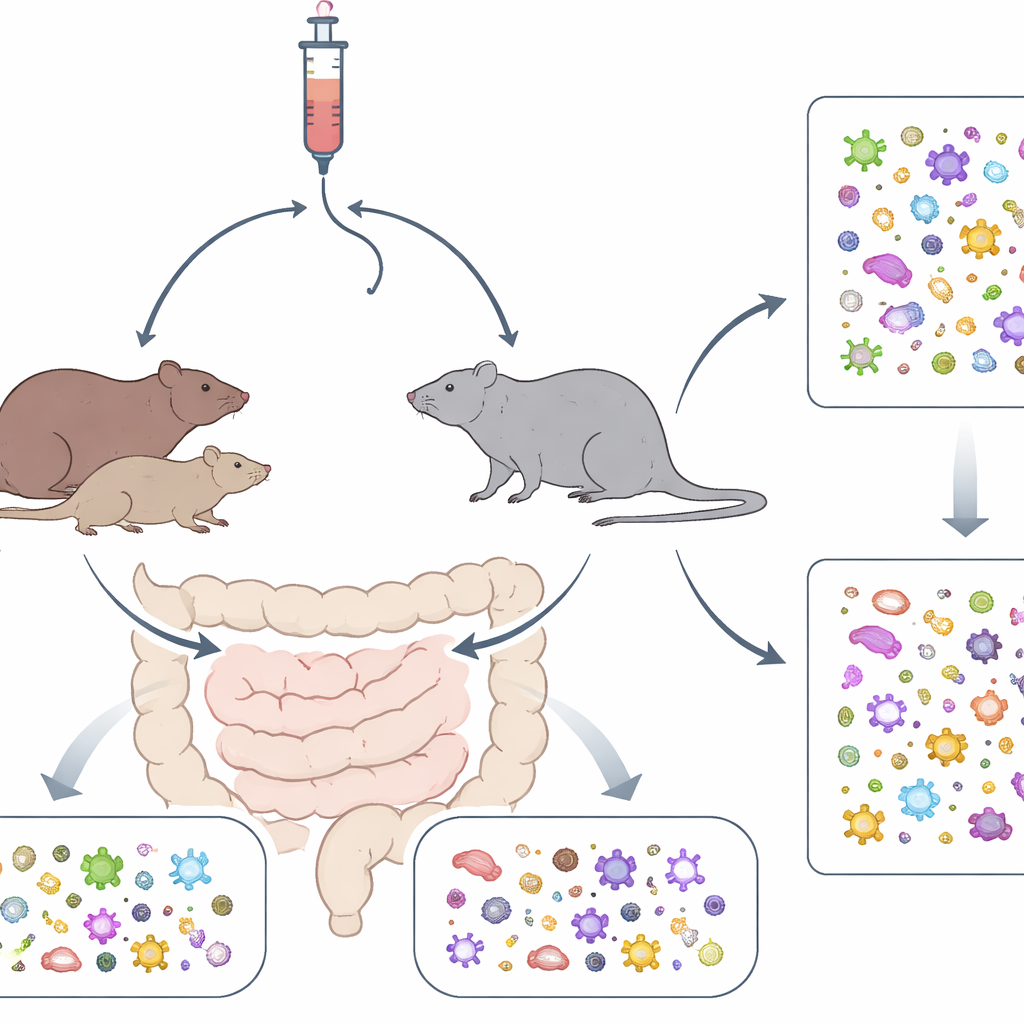
Due tipi di ratti, un farmaco potente
Il team ha lavorato con due ceppi di ratti endogami che sono geneticamente molto diversi. Ratti maschi e femmine sono stati addestrati a premere una leva per aut somministrarsi ossicodone per via endovenosa o una soluzione salina innocua, imitando l'assunzione volontaria di droga negli esseri umani. Nel corso di settimane, gli animali hanno avuto prima accessi di breve durata e poi sessioni molto più lunghe, permettendo all'assunzione di aumentare. Un ceppo, chiamato M520/N, ha assunto in modo costante più ossicodone rispetto al ceppo ACI/EurMcwi, sottolineando che il background genetico può influenzare fortemente la quantità di farmaco che un individuo sceglie di consumare. Anche quando la leva erogava solo soluzione salina, ceppo e sesso hanno continuato a influire: le femmine M520/N hanno premuto la leva più di ogni altro gruppo, suggerendo che tratti innati possono plasmare non solo la ricerca di droghe ma anche l'attrazione generale verso la stimolazione.
Monitorare peso e salute intestinale lungo il percorso
I ricercatori hanno monitorato il peso corporeo come semplice indicatore della salute generale durante questo regime impegnativo. Durante la fase ad accesso prolungato, i ratti che si autoconsumevano ossicodone tendevano a perdere peso rispetto ai corrispondenti trattati con soluzione salina, e i maschi hanno perso più delle femmine. Poiché dieta e variazioni di peso sono note per alterare i batteri intestinali, questi cambiamenti probabilmente interagiscono con gli effetti diretti dell'ossicodone sull'intestino, aggiungendo un ulteriore livello di complessità a come il farmaco rimodelli il microbioma. Dopo le sessioni finali, il team ha raccolto campioni da due regioni intestinali chiave—feci (che riflettono il colon) e il cieco, una sacca dove i microbi sono particolarmente densi—per vedere come ogni comunità fosse cambiata.
Geni e sesso modellano la diversità microbica
Per capire quanto fossero ricche e variegate le comunità microbiche, gli scienziati hanno misurato diverse forme di diversità all'interno di ciascun campione. Sia nelle comunità fecali sia in quelle del cieco, il background genetico e il sesso hanno avuto effetti marcati. In generale, i ratti ACI/EurMcwi e le femmine tendevano ad ospitare comunità batteriche più diversificate rispetto ai ratti M520/N e ai maschi. È interessante che il semplice consumo di ossicodone non abbia ridotto questa diversità all'interno dei campioni, il che significa che il numero totale e l'ampiezza evolutiva dei microbi sono rimasti in larga misura simili. Tuttavia, quando i ricercatori hanno confrontato quali batteri erano presenti e quanto erano abbondanti tra gli animali, hanno osservato una chiara separazione per ceppo e per trattamento (ossicodone o salina). Questo mostra che, mentre l'intestino può rimanere in senso ampio “attivo”, i giocatori specifici e il loro equilibrio sono fortemente plasmati sia dai geni sia dall'esposizione al farmaco. 
Spostamenti specifici per comunità nei batteri intestinali
Approfondendo, il team ha identificato gruppi particolari di batteri che cambiavano con l'ossicodone o differivano tra i ceppi. Complessivamente, 15 gruppi batterici distinguevano i ratti consumatori di ossicodone dai controlli con salina, e 51 differivano tra i due ceppi. Alcuni schemi erano condivisi tra le regioni intestinali—per esempio, certi generi come Blautia, Prevotella e Rodentibacter divennero più comuni nei consumatori di ossicodone sia nei campioni fecali sia in quelli del cieco. Altri cambiamenti invece erano altamente specifici per comunità: un phylum batterico chiamato Patescibacteria è diminuito nel cieco dopo l'ossicodone, ma non nelle feci, e molti taxa si sono spostati in direzioni opposte nelle due regioni. Anche il modo in cui i batteri tendevano a coesistere e a formare reti di interazione è cambiato in funzione sia del ceppo sia del farmaco, suggerendo che ossicodone e genetica non alterano solo quali microbi sono presenti, ma anche come interagiscono tra loro.
Che cosa significa per le persone e la medicina del dolore
Nel complesso, lo studio mostra che il nostro patrimonio genetico e l'esposizione agli oppioidi possono congiuntamente rimodellare l'ecosistema intestinale in modi sottili ma diffusi, e che questi effetti variano tra le regioni dell'intestino. Il background genetico ha influenzato quanto ossicodone i ratti hanno scelto di assumere, e ha anche plasmato fortemente quali microbi prosperavano nel loro intestino. L'uso di ossicodone ha poi aggiunto spostamenti specifici per comunità nella composizione microbica e nelle reti microbiche, anche senza grandi cali nella diversità complessiva. Per le persone, questo suggerisce che due individui a cui viene prescritto lo stesso analgesico potrebbero sperimentare conseguenze molto diverse a livello intestinale e forse cerebrale a seconda dei loro geni e del microbioma preesistente. Comprendere queste interazioni gene–microbioma–farmaco potrebbe aiutare a spiegare perché alcuni pazienti sono più vulnerabili al disturbo da uso di oppioidi o agli effetti gastrointestinali, e potrebbe infine guidare trattamenti più personalizzati che proteggano o persino sfruttino il microbioma intestinale.
Citazione: Duffy, E.P., Sterrett, J.D., Hale, L.H. et al. Oxycodone self-administration and genetic background exert community-specific effects in the gut microbiome. Sci Rep 16, 13276 (2026). https://doi.org/10.1038/s41598-026-41666-1
Parole chiave: disturbo da uso di oppioidi, microbioma intestinale, ossicodone, background genetico, autoconsumo nei ratti