Clear Sky Science · zh
M2 型巨噬细胞来源的细胞外囊泡通过上调 FAM83A 在结直肠癌细胞中诱导类 EMT 转录重编程
为何我们的防御有时会无意中助长癌症
癌症并非孤立生长;它在一个由免疫细胞和支持细胞组成的繁忙“社区”中发展,这些细胞可以抑制肿瘤,也可能在不自觉中帮助肿瘤。本研究探讨了一类免疫细胞如何发送微小的生物“包裹”,推动结肠癌细胞朝向更具移动性和侵袭性的状态——这种状态与癌症转移(肿瘤在体内扩散)有关。
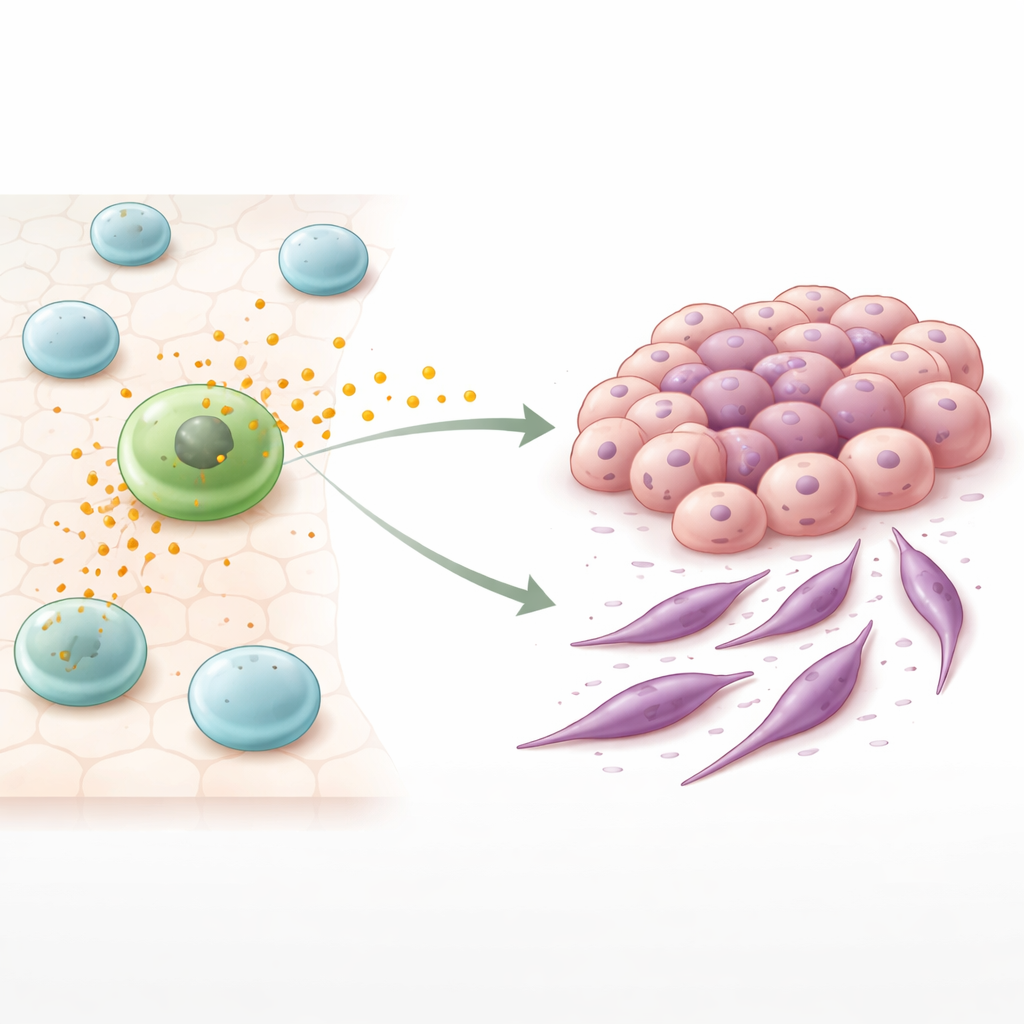
免疫细胞发送的隐藏信息
在聚集于肿瘤周围的免疫细胞中,巨噬细胞是关键角色。有些巨噬细胞呈现战士般的模式可以攻击肿瘤,而另一些被称为 M2 型样巨噬细胞,则更多承担滋养和伤口修复的角色。在许多癌症中,这类 M2 型样细胞积聚并与肿瘤生长及不良预后相关。作者着眼于这些细胞释放的微小膜泡,称为细胞外囊泡或外泌体。这些囊泡内含蛋白质和遗传物质,能在细胞间传递并重编程受体细胞的行为。
将定居的肿瘤细胞变成游走者
为测试这些囊泡对结肠癌的影响,研究者将人类结直肠癌细胞与 M2 型样巨噬细胞共同培养,或仅使癌细胞暴露于纯化的巨噬细胞囊泡中。在这两种情况下,癌细胞开始丧失紧密连接、有序组织细胞的特征,获得更具柔性、纺锤形并更易移动的特征。此变化类似于上皮-间质转化(EMT),在此过程中原本稳定的细胞松开连接变得更具迁移性。显著的是,当癌细胞接受分离的囊泡处理时,所发生的变化甚至比与巨噬细胞共培养更强烈,提示这些囊泡是驱动该效应的主要因素。
揭示癌细胞内的关键开关
为了解癌细胞内发生了什么,团队比较了囊泡暴露后成千上万基因的活性变化。他们发现基因活性被广泛重编程,其中一个名为 FAM83A 的基因显著上调,此基因此前与多种癌症的侵袭性行为有关。当 FAM83A 水平升高时,结肠癌细胞明显减少帮助细胞相互粘附的分子,同时增加与运动和组织分解相关的分子与酶。研究者采用小干扰 RNA(siRNA)这一精确的分子工具降低 FAM83A 水平后,囊泡驱动的向更具迁移性状态的转变在很大程度上被阻断。这将 FAM83A 锁定为连接巨噬细胞囊泡信号与癌细胞内部重编程的关键开关。
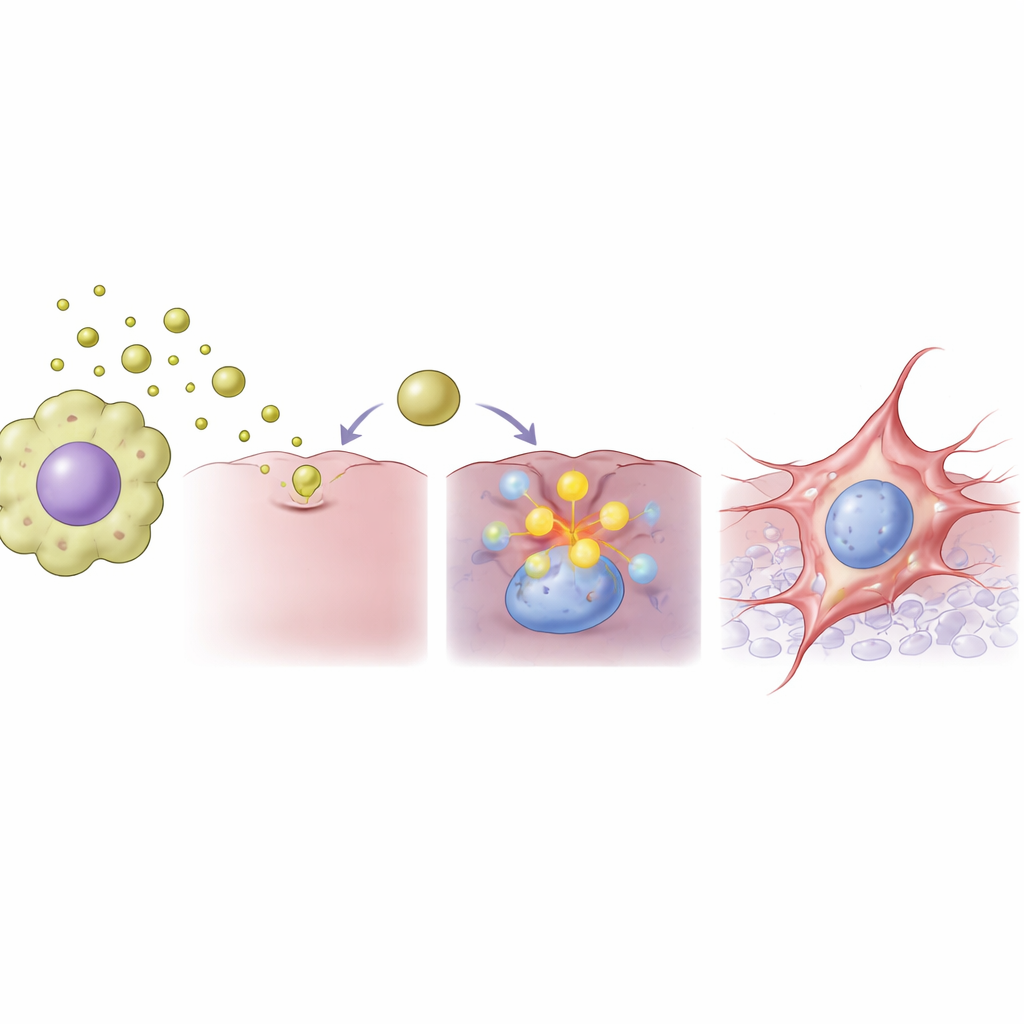
这些发现如何影响未来的癌症治疗
由于这些囊泡在推动癌细胞走向侵袭性方面比巨噬细胞本身更为强效,它们成为有前景的新靶点。研究表明,阻断肿瘤相关巨噬细胞释放囊泡,或直接下调肿瘤细胞中的 FAM83A,可能有助于阻止转移的早期步骤。作者还发现该囊泡—FAM83A 通路在其他癌种中可能也具有意义,但其作用在不同肿瘤类型间有所差异,强调在设计治疗前需要更多研究。
这对面对癌症的人意味着什么
简而言之,这项工作表明某些免疫细胞可以发送微小包裹,“指导”结肠癌细胞变得更具移动性和潜在危险性,而癌细胞内的单一基因在这一信息传递中起到关键中继作用。通过描绘从巨噬细胞囊泡到 FAM83A 激活再到更具侵袭性的细胞状态这一链条,研究提供了肿瘤微环境如何助长病情进展的更清晰图景。从长远看,破坏这些信号的治疗可能补充现有疗法,不仅旨在缩小肿瘤,也旨在防止其扩散。
引用: Isik, M., Akkulak, M. & Derkus, B. M2 macrophage–derived extracellular vesicles induce EMT-like transcriptional reprogramming in colorectal cancer cells via upregulation of FAM83A. Sci Rep 16, 9829 (2026). https://doi.org/10.1038/s41598-026-39262-4
关键词: 结直肠癌, 肿瘤微环境, 巨噬细胞外泌体, 上皮-间质转化, FAM83A