Clear Sky Science · pl
Egzosomy pochodzące od makrofagów M2 wywołują reprogramowanie transkrypcyjne przypominające EMT w komórkach raka jelita grubego poprzez nasilanie ekspresji FAM83A
Dlaczego nasze własne mechanizmy obronne czasem sprzyjają rakowi
Nowotwór nie rozwija się w izolacji; powstaje w tętniącej życiem okolicy komórek odpornościowych i podporowych, które mogą go zahamować lub – nieświadomie – mu pomagać. W badaniu tym przyjrzano się, jak określony typ komórek odpornościowych wysyła maleńkie biologiczne „paczki”, które skłaniają komórki raka jelita do przyjęcia bardziej ruchomego, inwazyjnego stanu związanego z przerzutami, czyli rozprzestrzenianiem się choroby w organizmie.
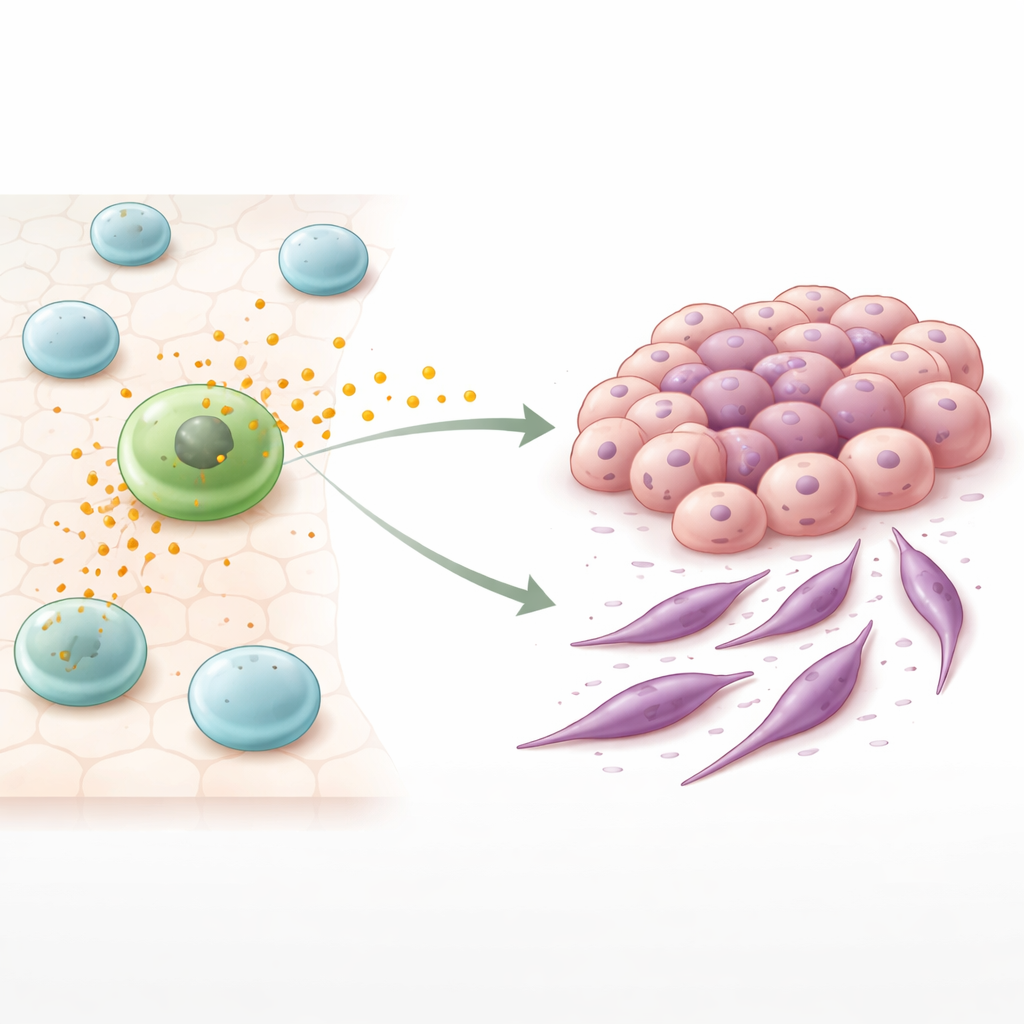
Ukryte komunikaty wysyłane przez komórki odpornościowe
Wśród komórek odpornościowych gromadzących się wokół guzów kluczową rolę odgrywają makrofagi. Niektóre przyjmują tryb „wojownika” i atakują guzy, inne zaś, określane jako makrofagi podobne do M2, pełnią bardziej opiekuńczą, gojącą funkcję. W wielu nowotworach komórki te gromadzą się i wiążą z nasilonym wzrostem guza oraz gorszym rokowaniem. Autorzy skupili się na maleńkich pęcherzykach błonowych uwalnianych przez te komórki, znanych jako pęcherzyki zewnątrzkomórkowe lub egzosomy. Wypełnione białkami i materiałem genetycznym, pęcherzyki te przemieszczają się między komórkami i potrafią przebudować zachowanie swoich odbiorców.
Przekształcanie osiadłych komórek nowotworowych w wędrowców
Aby sprawdzić, jak te pęcherzyki wpływają na raka jelita, badacze hodowali ludzkie komórki raka jelita grubego razem z makrofagami M2-podobnymi lub wystawiali komórki nowotworowe jedynie na oczyszczone pęcherzyki makrofagów. W obu przypadkach komórki nowotworowe zaczęły tracić cechy ściśle połączonych, uporządkowanych komórek tkankowych i nabierać cech bardziej elastycznych, wrzecionowatych komórek zdolnych do łatwiejszego przemieszczania się. Ta zmiana przypomina proces zwany przejściem nabłonkowo–mezenchymalnym (EMT), w którym wcześniej stabilne komórki rozluźniają połączenia i stają się bardziej migracyjne. Co znamienne, zmiany były jeszcze silniejsze, gdy komórki nowotworowe traktowano izolowanymi pęcherzykami niż gdy współhodowano je z makrofagami, co sugeruje, że to pęcherzyki są głównym motorem tego efektu.
Odkrycie kluczowego przełącznika wewnątrz komórek nowotworowych
Aby zrozumieć, co zachodzi wewnątrz komórek nowotworowych, zespół porównał aktywność tysięcy genów po ekspozycji na pęcherzyki. Stwierdzono szerokie przestawienie aktywności genów, w tym wyraźny wzrost ekspresji genu FAM83A, wcześniej powiązanego z agresywnym przebiegiem w kilku nowotworach. Wraz ze wzrostem poziomu FAM83A komórki raka jelita grubego silnie zmniejszały ilość cząsteczek pomagających im przylegać do sąsiadów oraz zwiększały stężenie białek i enzymów związanych z ruchem i rozkładem tkanki. Gdy badacze użyli małego interferującego RNA, precyzyjnego narzędzia molekularnego, aby obniżyć poziom FAM83A, napędzana przez pęcherzyki zmiana w kierunku bardziej ruchomego stanu została w dużej mierze zablokowana. Wskazało to FAM83A jako kluczowy przełącznik łączący sygnał z pęcherzyków makrofagów z wewnętrzną reprogramacją komórek nowotworowych.
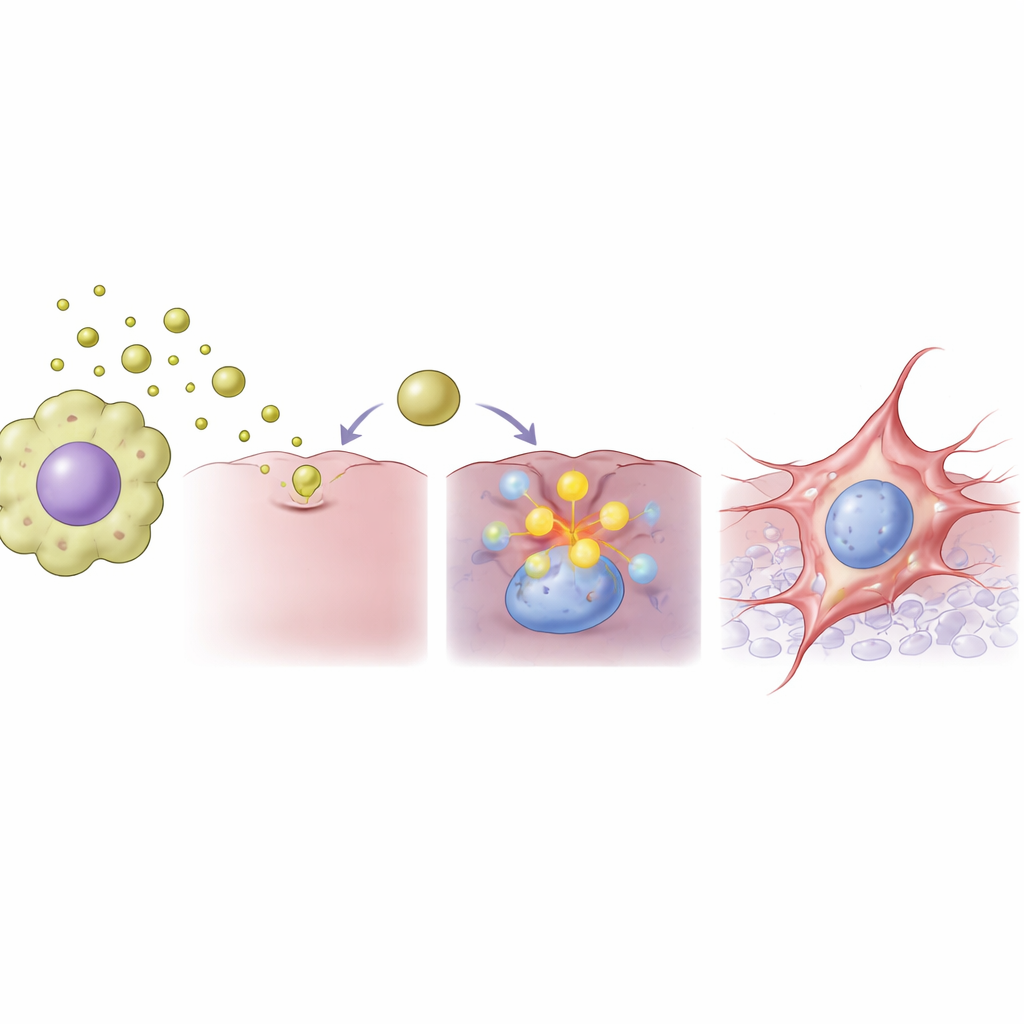
Jak te odkrycia mogą wpłynąć na przyszłe terapie przeciwnowotworowe
Ponieważ pęcherzyki okazały się silniejsze niż same makrofagi w nakłanianiu komórek nowotworowych do zachowań inwazyjnych, stają się obiecującym nowym celem. Badanie sugeruje, że blokowanie uwalniania pęcherzyków z makrofagów związanych z guzem lub bezpośrednie obniżenie poziomu FAM83A w komórkach guza może pomóc zapobiegać wczesnym etapom przerzutowania. Autorzy zauważyli również wskazówki, że szlak pęcherzyk–FAM83A może mieć znaczenie w innych nowotworach, choć jego rola wydaje się różnić w zależności od typu guza, co podkreśla potrzebę dalszych badań przed opracowaniem terapii.
Co to oznacza dla osób dotkniętych rakiem
Mówiąc prosto, to badanie pokazuje, że określone komórki odpornościowe mogą wysyłać mikroskopijne paczki, które „szkolą” komórki raka jelita, by stały się bardziej ruchome i potencjalnie bardziej niebezpieczne, oraz że pojedynczy gen w komórkach nowotworowych działa jako kluczowy przekaźnik tego sygnału. Mapując tę ścieżkę — od pęcherzyków makrofagów przez aktywację FAM83A po bardziej inwazyjny stan komórkowy — badanie daje jaśniejszy obraz tego, jak mikrośrodowisko guza może napędzać progresję. W dłuższej perspektywie terapie zakłócające te sygnały mogłyby uzupełniać istniejące leczenie, dążąc nie tylko do zmniejszenia guzów, lecz także do powstrzymania ich rozprzestrzeniania się.
Cytowanie: Isik, M., Akkulak, M. & Derkus, B. M2 macrophage–derived extracellular vesicles induce EMT-like transcriptional reprogramming in colorectal cancer cells via upregulation of FAM83A. Sci Rep 16, 9829 (2026). https://doi.org/10.1038/s41598-026-39262-4
Słowa kluczowe: rak jelita grubego, mikrośrodowisko guza, egzosomy makrofagów, przejście nabłonkowo-mezenchymalne, FAM83A