Clear Sky Science · he
ואזיקולות חוץ-תאיות שמקורן במקרופאגי M2 מעוררות תכנות מחדש טרנסקריפציוני בדומה ל-EMT בתאי סרטן המעי הגס באמצעות העלאת ביטוי FAM83A
מדוע ההגנות שלנו לעיתים מסייעות בסתר לסרטן
סרטן אינו צומח בבידוד; הוא מתפתח בתוך שכונה תוססת של תאים חיסוניים ותמיכה שיכולים או להצר את צמיחת הגידול או — מבלי כוונה — לעזור לו. מחקר זה חוקר כיצד קבוצת תאים חיסוניים מסוימת שולחת "חבילות" ביולוגיות זעירות שדוחפות תאי סרטן המעי הגס למצב יותר נייד ואגרסיבי, הקשור למטסטזות, פיזור הסרטן ברחבי הגוף.
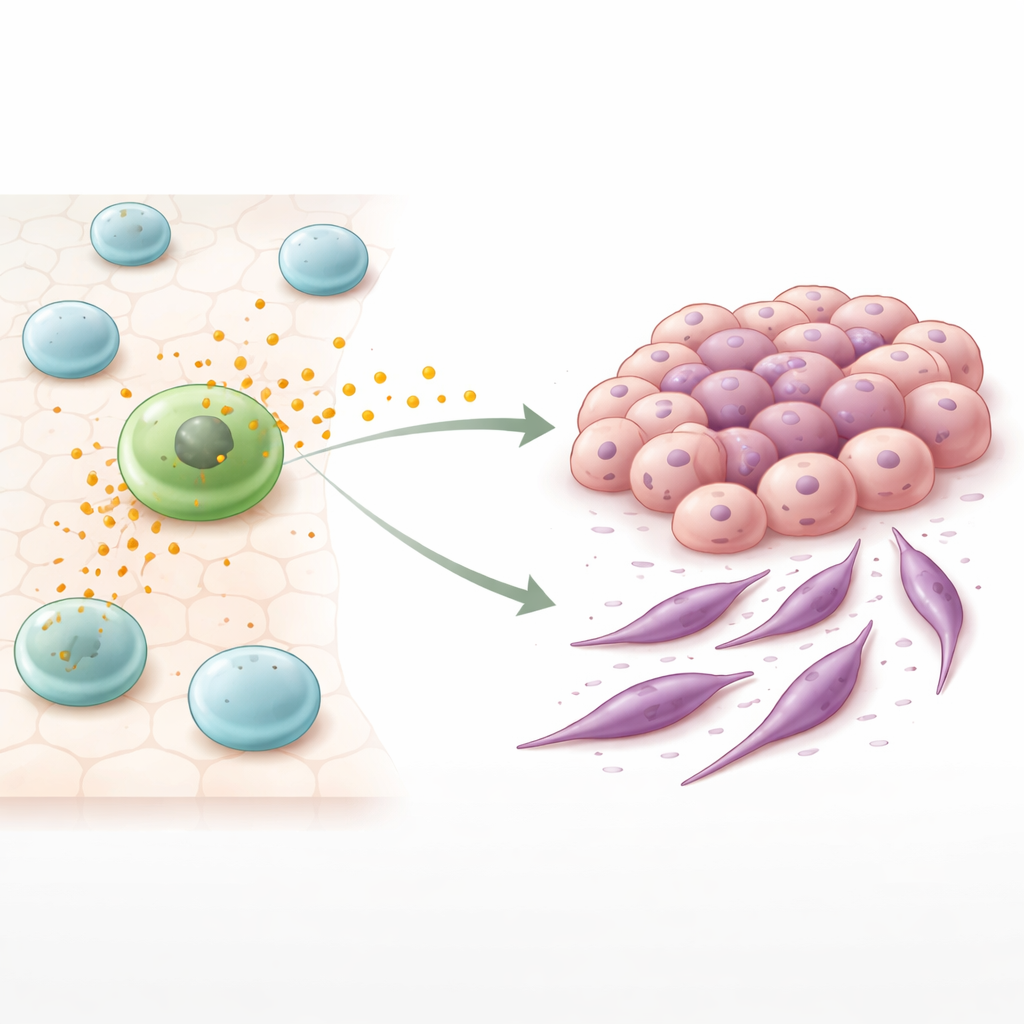
המסרים המוסתרים שנשלחים על ידי תאים חיסוניים
בין התאים החיסוניים המתמקדים סביב הגידול, מקרופאגים הם שחקנים מרכזיים. חלק מהמקרופאגים מקבלים אופי לוחמני שיכול לתקוף גידולים, בעוד אחרים, המכונים מקרופאגים בדמות M2, נוטים לתפקד באופן מטפח ומלווה בריפוי פצע. ברבים מהמקרים, תאים בדמות M2 מצטברים ומתקשרים עם גדילה גרועה יותר של הגידול ותוצאה קלינית פחות טובה. החוקרים התמקדו בשלפוחיות ממברנליות זעירות שמשתחררות מהם, הידועות כוזיקולות חוץ-תאיות או אקסוזומים. עטופות בחלבונים וחומר גנטי, הוזיקולות הללו נעות בין תאים ויכולות לתכנת מחדש את התנהגות היעד שלהן.
להפוך תאים יציבים של הגידול לנודדים
כדי לבדוק כיצד הוזיקולות האלה משפיעות על סרטן המעי הגס, החוקרים גידלו תאי סרטן קולורקטליים אנושיים יחד עם מקרופאגים בדמות M2 או חשפו את תאי הסרטן רק לוזיקולות מפרוקות של המקרופאגים. בשתי המצבויים, תאי הסרטן החלו לאבד מאפיינים של תאים מסודרים ומחוברים באופן הדוק, ורכשו תכונות של תאים גמישים יותר ובעלי צורה ספינדלית שיכולים לנוע ביתר קלות. המעבר הזה דומה לתהליך הקרוי מעבר אפיתליאליקומזנכימלי (EMT), שבו תאים יציבים מרפים את קישרותיהם והופכים לניידים יותר. באופן בולט, השינויים היו חזקים אף יותר כאשר תאי הסרטן טופלו בוזיקולות מבודדות מאשר כאשר חולקו בתרבית עם מקרופאגים, מה שמרמז שהוזיקולות הן מניע משמעותי של האפקט.
גילוי מתג מרכזי בתוך תאי הסרטן
כדי להבין מה קורה בתוך תאי הסרטן, הקבוצה השוותה פעילות של אלפי גנים לאחר חשיפה לוזיקולות. הם מצאו רה-תכנות רחב היקף של פעילות גנטית, כולל עלייה חזקה בביטוי של הגן בשם FAM83A, שכבר נקשר בעבר להתנהגות אגרסיבית במספר סוגי סרטן. כשהרמות של FAM83A עלו, תאי סרטן המעי הגס הפחיתו בחוזקה מולקולות שמסייעות להם להידבק לשכניהם והגבירו מולקולות וזרזים הקשורים לתנועה ולפירוק רקמות. כאשר החוקרים השתמשו ב-RNA מתערב קטן, כלי מולקולרי מדויק, כדי להפחית את רמות FAM83A, המעבר המונע על ידי הוזיקולות לכיוון מצב נייד נחסם במידה רבה. ממצא זה מצביע על FAM83A כמפתח מרכזי המקשר בין אות הוזיקולה מהתאים החיסוניים לתכנות הפנימי של תאי הסרטן.
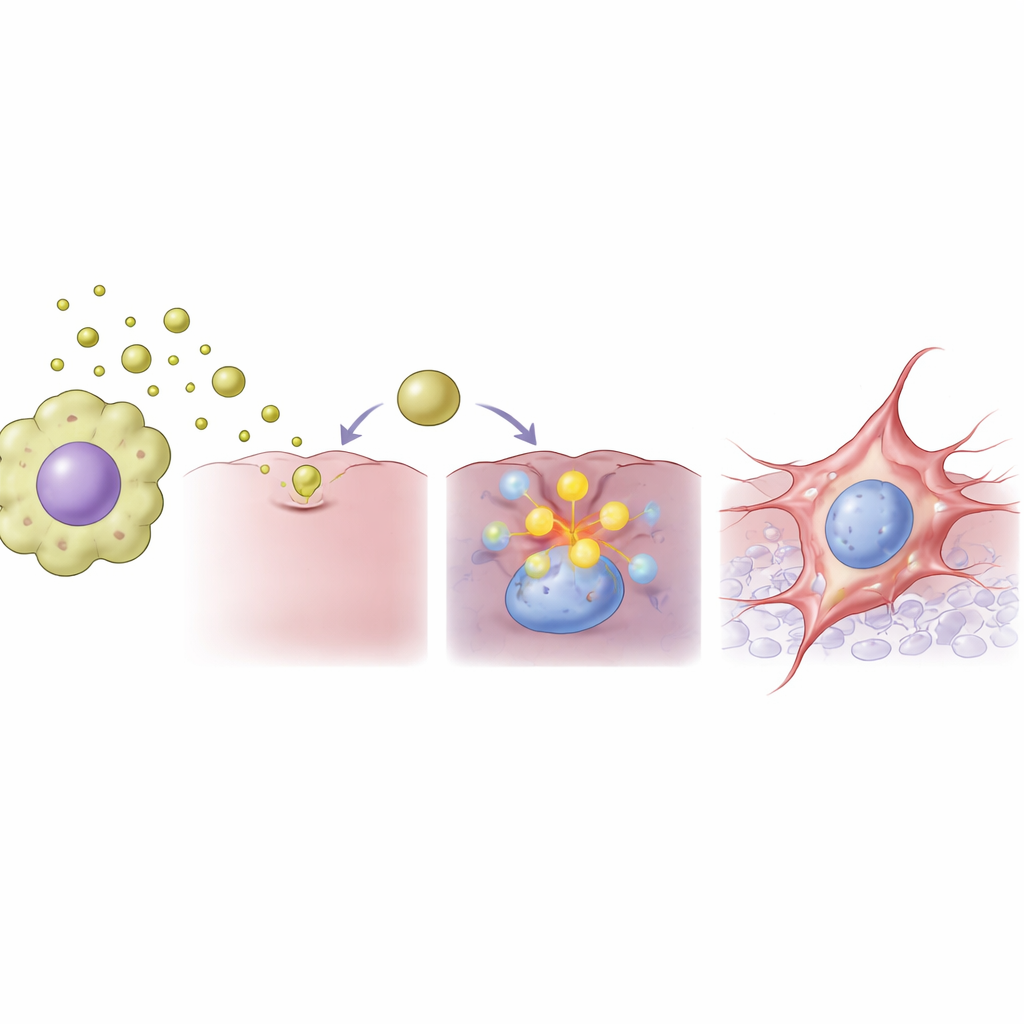
כיצד ממצאים אלה עשויים לעצב טיפולים עתידיים בסרטן
מכיוון שהוזיקולות הוכחו כחזקות יותר מהמקרופאגים עצמם בדחיפת תאי סרטן להתנהגות פולשנית, הן עולות כיעדים חדשים מבטיחים. המחקר מציע כי חסימת שחרור הוזיקולות ממקרופאגים מקושרי-גידול, או כיבוי ישיר של FAM83A בתאי הגידול, עשויה לעזור למנוע שלבים מוקדמים של מטסטזה. המחברים גם הבחינו ברמזים לכך שציר הוזיקולה–FAM83A עשוי להיות רלוונטי בסוגי סרטן אחרים, אף שתגובתו משתנה בין סוגי הגידול, מה שמדגיש את הצורך במחקר נוסף לפני שניתן יהיה לעצב טיפולים קליניים.
מה משמעות הדבר לאנשים המתמודדים עם סרטן
במילים פשוטות, עבודה זו מראה שתאים חיסוניים מסוימים יכולים לשלוח חבילות מיקרוסקופיות שמ"מאמנת" תאי סרטן המעי הגס להיות ניידים ומסוכנים יותר, ושגן יחיד בתוך תאי הסרטן משמש כנגב מרכזי להעברתו של המסר. על ידי מיפוי שרשרת זו — מהוזיקולות המקרופאגיות דרך הפעלת FAM83A ועד למצב תאי פולשני יותר — המחקר מספק תמונה ברורה יותר של האופן שבו סביבת הגידול יכולה להזין התקדמות. בטווח הארוך, טיפולים שיכולים להפריע לאותות אלה עשויים להשלים טיפולים קיימים, במטרה לא רק לקטין גידולים אלא גם למנוע את פיזורם.
ציטוט: Isik, M., Akkulak, M. & Derkus, B. M2 macrophage–derived extracellular vesicles induce EMT-like transcriptional reprogramming in colorectal cancer cells via upregulation of FAM83A. Sci Rep 16, 9829 (2026). https://doi.org/10.1038/s41598-026-39262-4
מילות מפתח: סרטן המעי הגס, מיקרו-סביבת הגידול, אקסוזומים של מקרופאגים, מעבר אפיתליאליקומזנכימלי, FAM83A