Clear Sky Science · fr
Les vésicules extracellulaires dérivées des macrophages M2 induisent une reprogrammation transcriptionnelle de type EMT dans les cellules du cancer colorectal via la surexpression de FAM83A
Pourquoi nos propres défenses peuvent parfois aider le cancer
Le cancer ne se développe pas en vase clos ; il progresse dans un « quartier » animé composé de cellules immunitaires et de soutien qui peuvent soit freiner, soit, sans le savoir, aider la tumeur. Cette étude examine comment un type particulier de cellules immunitaires peut envoyer de minuscules « colis » biologiques qui poussent les cellules du cancer du côlon vers un état plus mobile et invasif, associé aux métastases, c’est‑à‑dire à la propagation du cancer dans l’organisme.
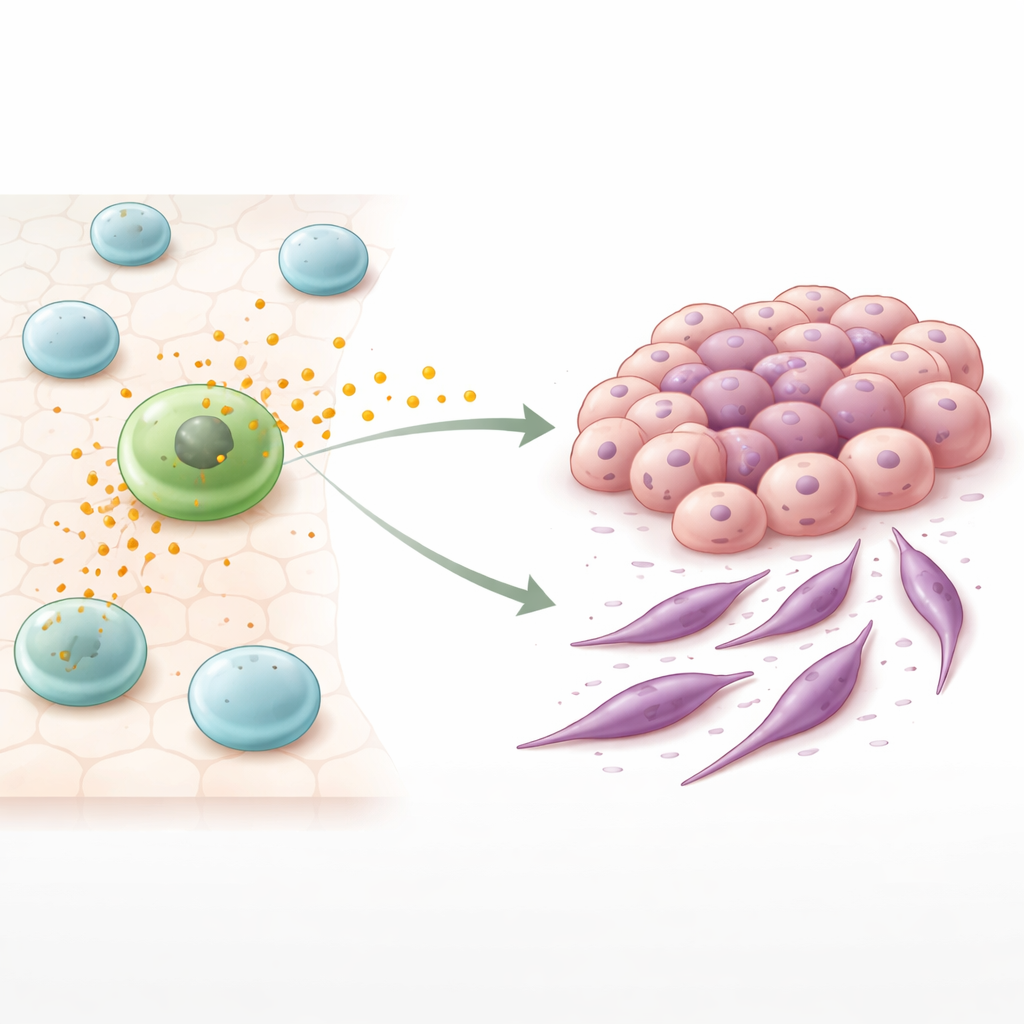
Les messages cachés envoyés par les cellules immunitaires
Parmi les cellules immunitaires qui s’accumulent autour des tumeurs, les macrophages jouent un rôle central. Certains macrophages adoptent un mode « guerrier » capable d’attaquer les tumeurs, tandis que d’autres, dits de type M2, prennent un rôle plus nourricier et de cicatrisation. Dans de nombreux cancers, ces cellules de type M2 s’accumulent et sont associées à la croissance tumorale et à un mauvais pronostic. Les auteurs se sont intéressés à de minuscules bulles membranaires libérées par ces cellules, connues sous le nom de vésicules extracellulaires ou exosomes. Chargées de protéines et de matériel génétique, ces vésicules voyagent entre les cellules et peuvent reprogrammer le comportement de leurs cibles.
Transformer des cellules tumorales sédentaires en vagabondes
Pour tester l’effet de ces vésicules sur le cancer du côlon, les chercheurs ont cultivé des cellules humaines de cancer colorectal en présence de macrophages de type M2 ou ont exposé les cellules cancéreuses uniquement à des vésicules macrophagiques purifiées. Dans les deux situations, les cellules cancéreuses ont commencé à perdre les caractéristiques d’un tissu bien collé et ordonné et ont acquis des traits de cellules plus flexibles et fusiformes, capables de se déplacer plus facilement. Ce changement ressemble au processus de transition épithélio‑mésenchymateuse (EMT), dans lequel des cellules auparavant stables relâchent leurs attaches et deviennent plus migratoires. Fait marquant, les changements étaient encore plus prononcés lorsque les cellules cancéreuses étaient traitées par des vésicules isolées que lorsqu’elles étaient simplement en co‑culture avec des macrophages, ce qui suggère que ces vésicules sont un moteur majeur de l’effet.
Découvrir un interrupteur clé à l’intérieur des cellules cancéreuses
Pour comprendre ce qui se passait à l’intérieur des cellules cancéreuses, l’équipe a comparé l’activité de milliers de gènes après exposition aux vésicules. Ils ont observé une réorganisation étendue de l’activité génétique, incluant une forte augmentation d’un gène appelé FAM83A, déjà associé à un comportement agressif dans plusieurs cancers. Lorsque les niveaux de FAM83A augmentaient, les cellules du cancer colorectal réduisaient fortement les molécules favorisant leur adhésion aux cellules voisines et augmentaient les molécules et enzymes associées au mouvement et à la dégradation des tissus. Lorsque les chercheurs ont utilisé de petits ARN interférents, un outil moléculaire précis, pour diminuer les niveaux de FAM83A, la bascule induite par les vésicules vers un état plus mobile a été en grande partie bloquée. Cela identifie FAM83A comme un interrupteur crucial reliant le signal des vésicules des cellules immunitaires à la reprogrammation interne des cellules cancéreuses.
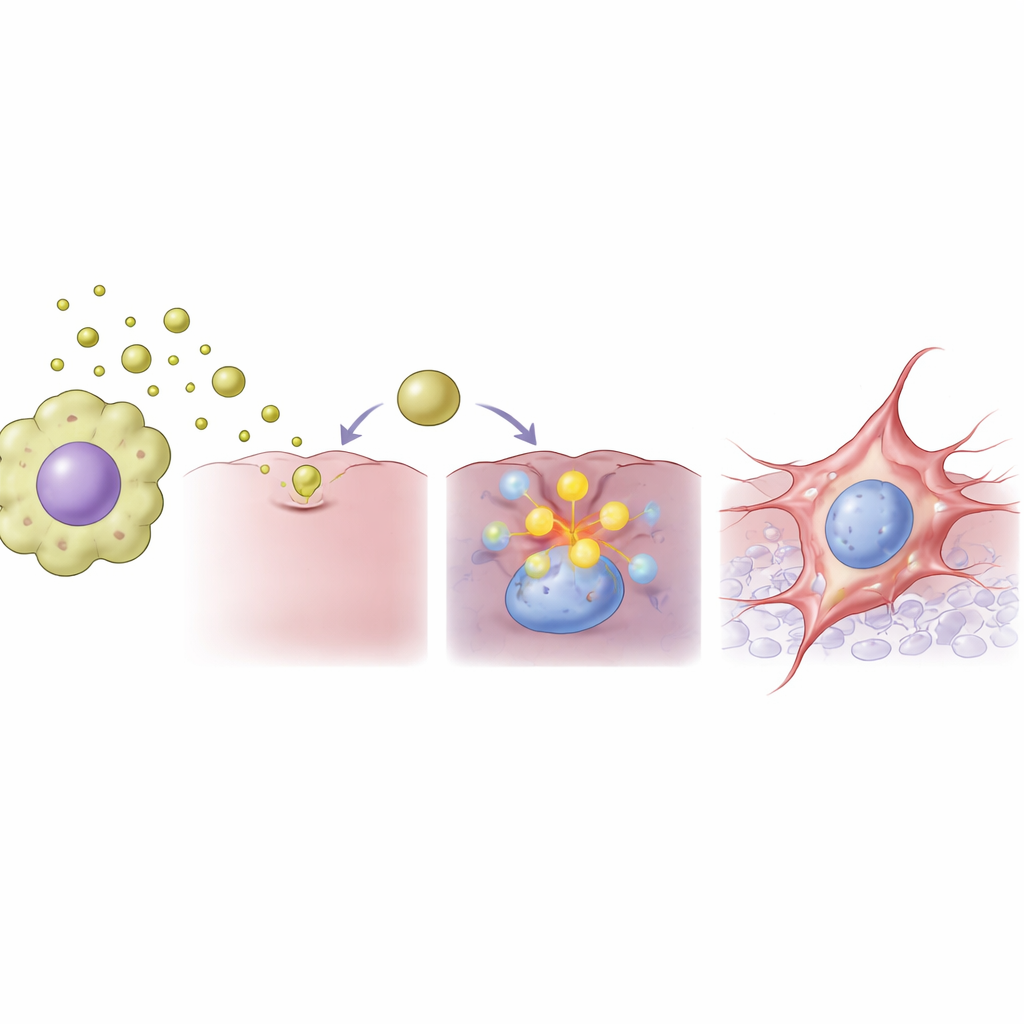
Comment ces découvertes pourraient orienter de futurs traitements contre le cancer
Comme ces vésicules se sont révélées plus puissantes que les macrophages eux‑mêmes pour pousser les cellules cancéreuses vers un comportement invasif, elles apparaissent comme de nouvelles cibles prometteuses. L’étude suggère que bloquer la libération de vésicules par les macrophages associés aux tumeurs, ou réduire directement FAM83A dans les cellules tumorales, pourrait aider à prévenir les premières étapes de la métastase. Les auteurs ont aussi relevé des indices que cette voie vésicule–FAM83A pourrait être pertinente dans d’autres cancers, bien que son rôle semble varier selon les types tumoraux, ce qui souligne la nécessité d’approfondir les recherches avant de concevoir des thérapies.
Ce que cela signifie pour les personnes confrontées au cancer
En termes simples, ce travail montre que certaines cellules immunitaires peuvent envoyer des colis microscopiques qui « coachinguent » les cellules du cancer colorectal pour devenir plus mobiles et potentiellement plus dangereuses, et qu’un seul gène à l’intérieur des cellules cancéreuses agit comme un relais clé de ce message. En cartographiant cette chaîne — des vésicules macrophagiques à l’activation de FAM83A puis à un état cellulaire plus invasif — l’étude offre une image plus claire de la manière dont le microenvironnement tumoral peut alimenter la progression. À long terme, des thérapies visant à perturber ces signaux pourraient compléter les traitements existants, visant non seulement à réduire la taille des tumeurs mais aussi à empêcher leur dissémination.
Citation: Isik, M., Akkulak, M. & Derkus, B. M2 macrophage–derived extracellular vesicles induce EMT-like transcriptional reprogramming in colorectal cancer cells via upregulation of FAM83A. Sci Rep 16, 9829 (2026). https://doi.org/10.1038/s41598-026-39262-4
Mots-clés: cancer colorectal, microenvironnement tumoral, exosomes de macrophages, transition épithélio-mésenchymateuse, FAM83A