Clear Sky Science · zh
通过在体外帕金森病神经元模型中过表达URG7以靶向氧化应激和线粒体功能障碍
为何保护脑细胞重要
帕金森病会逐渐剥夺人的运动能力和独立性,而现有治疗主要是缓解症状,无法阻止病损。许多科学家认为,一个主要的罪魁祸首是脑细胞内部的“生锈”——由有害的含氧分子所驱动,这些分子不断侵袭细胞的能量工厂线粒体。该研究考察了一种鲜为人知的蛋白质URG7,并提出一个简单但重要的问题:如果在类神经细胞内增强这种蛋白的表达,能否帮助它们抵御这种来自内部的磨损?
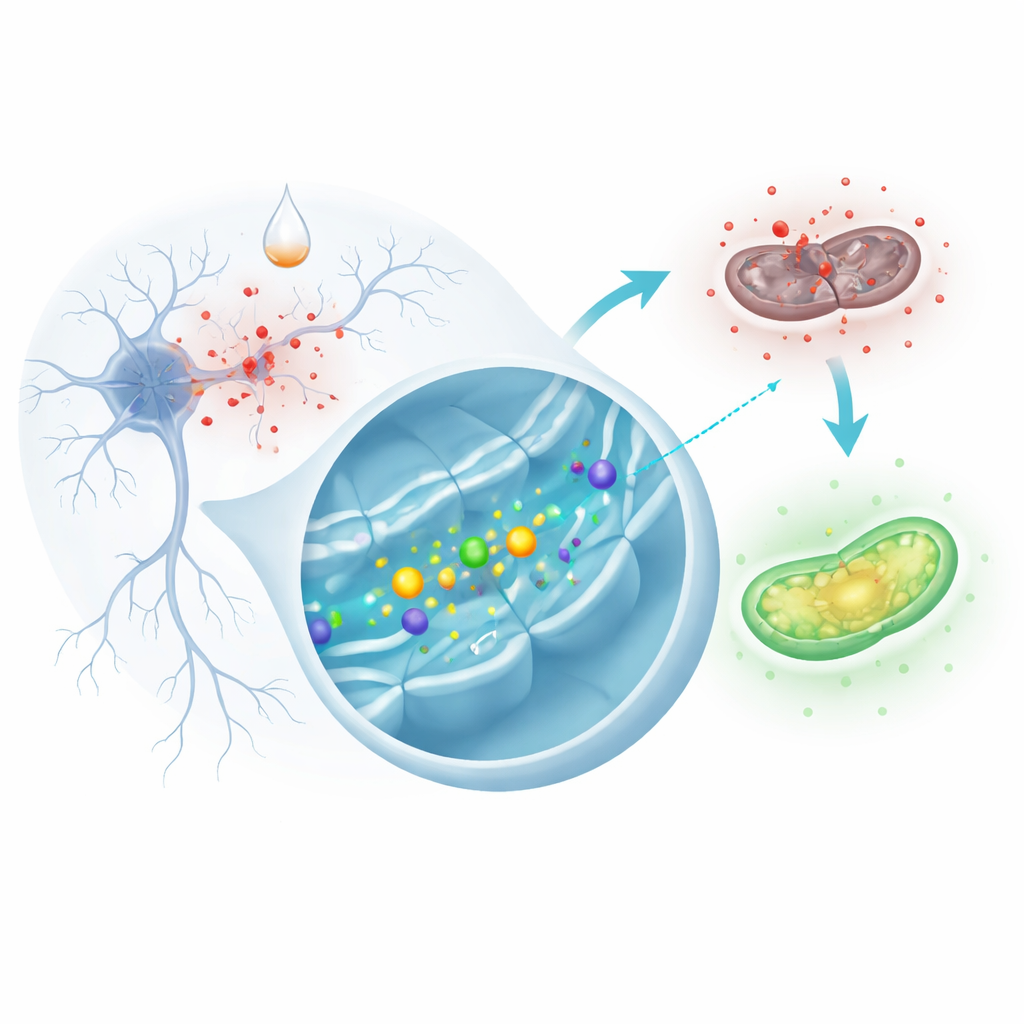
实验室中的帕金森损伤替代模型
由于难以直接观察活体人脑细胞的退化,研究人员常用培养细胞作为替代模型。本研究组使用了SH‑SY5Y细胞,这是一种能模拟许多神经元特性的人的细胞系。他们用一种叫6‑羟多巴胺的化学物质处理这些细胞,这种试剂广泛用于在实验室中再现帕金森病的关键方面。进入细胞后,该化合物会快速产生活性氧(reactive oxygen species)——一类寿命短、反应性强的分子,会损伤蛋白质、脂类和DNA,导致线粒体衰竭并最终细胞死亡。科学家们将普通细胞与被工程化以过表达URG7的细胞进行了比较,URG7是一种位于内质网——细胞蛋白处理与信号中枢的小型蛋白。
更少的细胞死亡与更温和的氧化应激
当两种细胞类型暴露于递增剂量的毒性化合物时,富含URG7的细胞存活明显更好。在显微镜下,对照组细胞开始变圆,失去树枝状突起并从培养皿脱落——这是受压、将死神经元的典型表现——而过表达URG7的细胞大体保持形态和数量。对活性氧的测量证实了这一视觉印象:在对照组中,随毒素剂量增加氧化信号显著上升,但在URG7细胞中,这些信号接近基线,尤其是在选定用于深入研究的剂量下。这表明URG7并非被动存在于细胞中;它积极参与抑制有害氧化物激增。
增强细胞自身的防御
为了解URG7如何发挥这种保护作用,研究人员检测了细胞内部防御系统的关键组成部分。他们考察了如过氧化氢酶(catalase)和线粒体超氧化物歧化酶2(superoxide dismutase 2)等酶,这些酶可安全分解有害的含氧物种,以及作为众多解毒基因开关的主控蛋白Nrf2。在过表达URG7的细胞中,这三者在RNA和蛋白水平上均有所升高,且过氧化氢酶活性在毒素暴露后不仅没有下降,反而增加。损伤标志物也从相反角度讲述了相同的故事:丙二醛(一种脂类被氧化损伤后的副产物)在对照细胞中显著上升,但在存在URG7时明显较低。综上,这些发现表明URG7更像是上游的协调者,提升细胞自身抗氧化工具箱的响应能力,而不是直接中和氧化物。
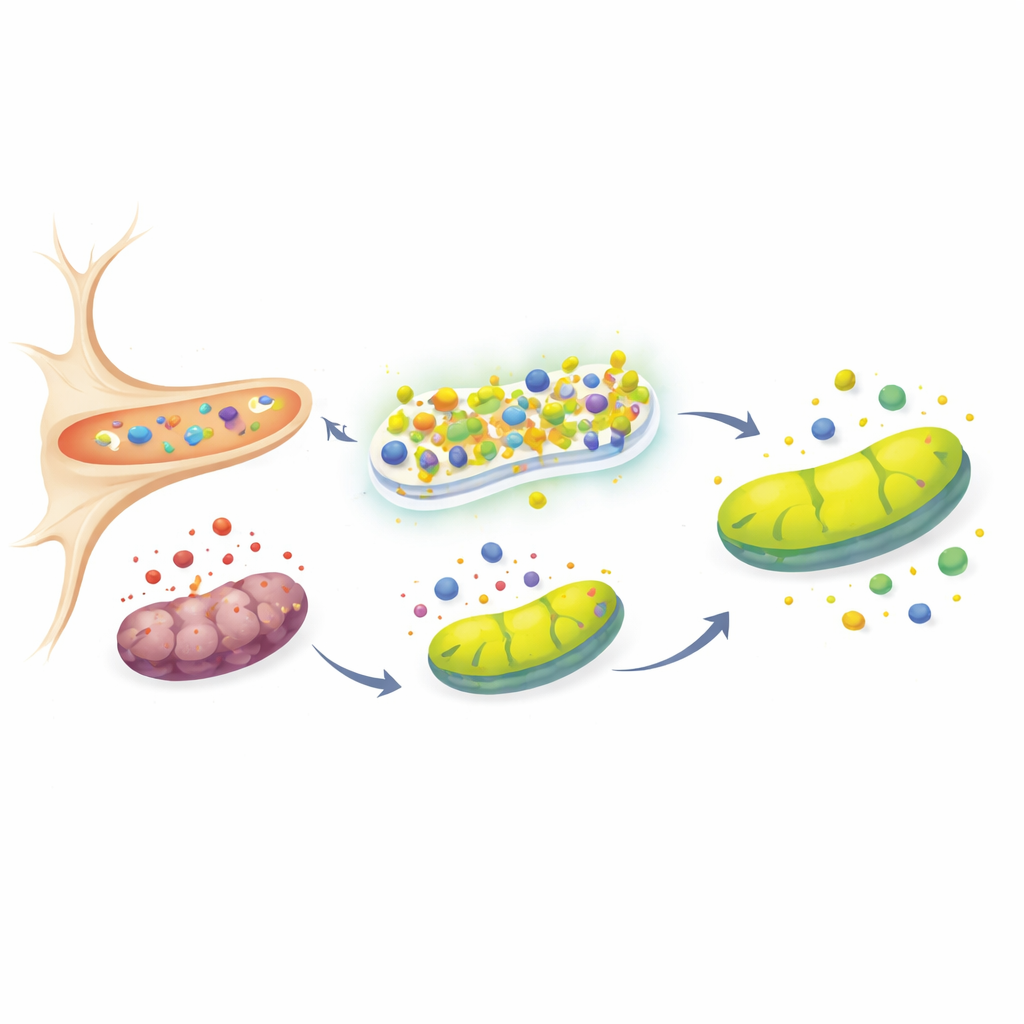
维持细胞“发电厂”的运行
线粒体常被称为细胞的发电厂,既是氧化应激的主要来源,也是首要受害者。其健康状况的一个关键指标是跨膜电位,线粒体受损时该电位会下降。毒素处理后,对照组细胞明显丧失了这种电位,反映出线粒体受到损伤,而富含URG7的细胞则保持近似正常值。研究小组随后检查了与线粒体质量控制和帕金森病密切相关的蛋白:PINK1、Parkin和DJ‑1。在健康细胞中,PINK1会持续从线粒体被清除;只有在线粒体受损时它才会积累。在过表达URG7的细胞中,尽管有毒素存在,PINK1仍保持低水平,这与线粒体完整性被保留相一致。同时,Parkin和DJ‑1——这两者都与支持线粒体功能和抗氧化防御相关——表达上调,提示URG7有助于维持一个更广泛的保护网络,从而稳定线粒体并限制细胞死亡。
这对未来疗法的可能意义
简而言之,这项工作表明URG7在类神经细胞内像一个早期预警的哨兵。当氧化应激上升时,富含URG7的细胞能更好地启动保护性基因、提升解毒酶活性并保持能量工厂的完整,从而在类帕金森环境中显著提高生存几率。尽管这些实验是在培养皿中而非活体脑中进行,但它们将URG7突出了作为潜在治疗靶点的前景,旨在保护神经元免受氧化损伤和线粒体衰竭——帕金森病及其他神经退行性疾病的两大核心驱动因素。
引用: Nigro, I., Miglionico, R., Lela, L. et al. Targeting oxidative stress and mitochondrial dysfunction via URG7 overexpression in an in vitro Parkinson’s disease neuronal model. Sci Rep 16, 9955 (2026). https://doi.org/10.1038/s41598-026-38925-6
关键词: 帕金森病, 氧化应激, 线粒体保护, 神经保护, URG7蛋白