Clear Sky Science · ru
Ориентирование на окислительный стресс и митохондриальную дисфункцию путем сверхэкспрессии URG7 в in vitro нейронной модели болезни Паркинсона
Почему важно защищать клетки мозга
Болезнь Паркинсона постепенно лишает людей подвижности и независимости, а современные методы лечения лишь смягчают симптомы, но не останавливают разрушение. Многие учёные считают, что главным виновником является внутреннее «ржавление» клеток мозга, вызванное вредными кислородсодержащими молекулами, которые повреждают энергетические фабрики клетки — митохондрии. В этом исследовании изучается малоизвестный белок URG7 и ставится простой, но важный вопрос: если повысить уровень этого белка внутри клеток, похожих на нервные, поможет ли это им выдержать подобный внутренний износ?
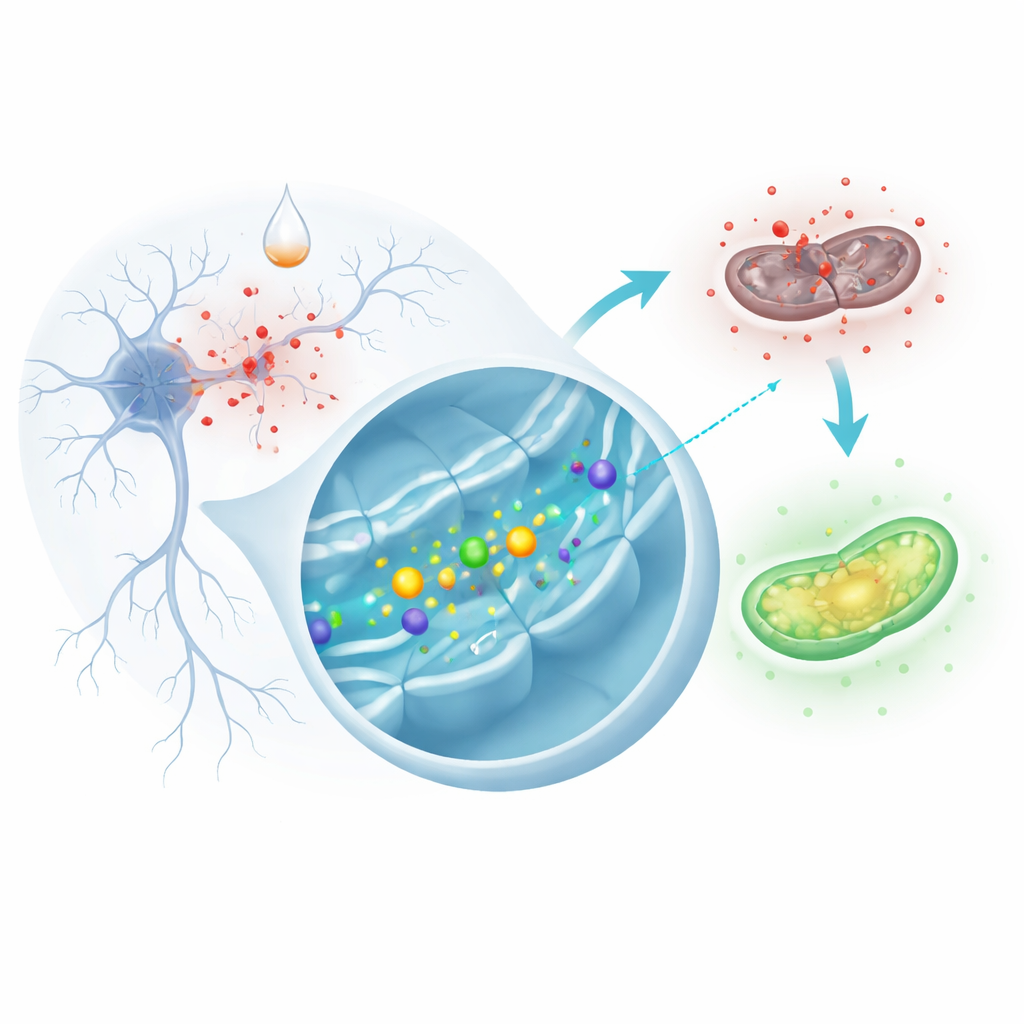
Лабораторный аналог повреждений при болезни Паркинсона
Поскольку нам трудно наблюдать живые человеческие клетки мозга в процессе вырождения, исследователи часто используют культивируемые клетки в качестве замены. В этой работе команда использовала клетки SH‑SY5Y, человеческую клеточную линию, способную имитировать многие свойства нейронов. Эти клетки подвергали воздействию вещества 6‑гидроксидопамина, широко применяемого для воспроизведения ключевых аспектов болезни Паркинсона в лаборатории. Попадая в клетки, это соединение быстро генерирует реактивные формы кислорода — короткоживущие, высокореактивные молекулы, способные повреждать белки, липиды и ДНК — что ведёт к отказу митохондрий и, в конечном счёте, к гибели клетки. Учёные сравнивали обычные клетки с клетками, модифицированными для синтеза дополнительного URG7, небольшого белка, локализующегося в эндоплазматическом ретикулуме — центре обработки белков и сигнальной активности клетки.
Меньше погибших клеток и сниженный окислительный стресс
При воздействии растущих доз токсического вещества клетки с избытком URG7 выживали значительно лучше. Под микроскопом контрольные клетки начинали округляться, теряли ветвистые отростки и отставали от поверхности — классическая картина стрессовых, гибнущих нейронов — тогда как клетки с сверхэкспрессией URG7 в основном сохраняли форму и количество. Измерения реактивных форм кислорода подтвердили эти наблюдения: в контрольных клетках сигналы окисления резко возрастали с увеличением дозы токсина, а в клетках с URG7 они оставались близкими к исходному уровню, особенно при дозе, выбранной для более глубокого изучения. Это указывает на то, что URG7 не просто пассивно присутствует в клетке: он активно помогает сдерживать всплеск вредных окислителей.
Усиление собственных защит клеток
Чтобы понять, как URG7 оказывает защитное действие, исследователи изучали ключевые компоненты внутренней защитной системы клетки. Они оценивали ферменты, такие как каталазa и супероксиддисмутаза 2, которые безопасно разлагают вредные формы кислорода, а также главный регулятор Nrf2, включающий множество детоксикационных генов. В клетках со сверхэкспрессией URG7 все три показателя были повышены на уровне РНК и белка, а сама активность каталазы увеличивалась вместо ожидаемого снижения после воздействия токсина. Маркёры повреждения подтверждали ту же картину с противоположной стороны: уровень малондиальдегида, побочного продукта окисленного липида, резко повышался в контрольных клетках, но оставался гораздо ниже при присутствии URG7. В совокупности эти данные указывают, что URG7 действует как вышеуровневый координатор, усиливая работу собственной антиоксидантной «аппаратуры» клетки, а не непосредственно нейтрализуя окислители.
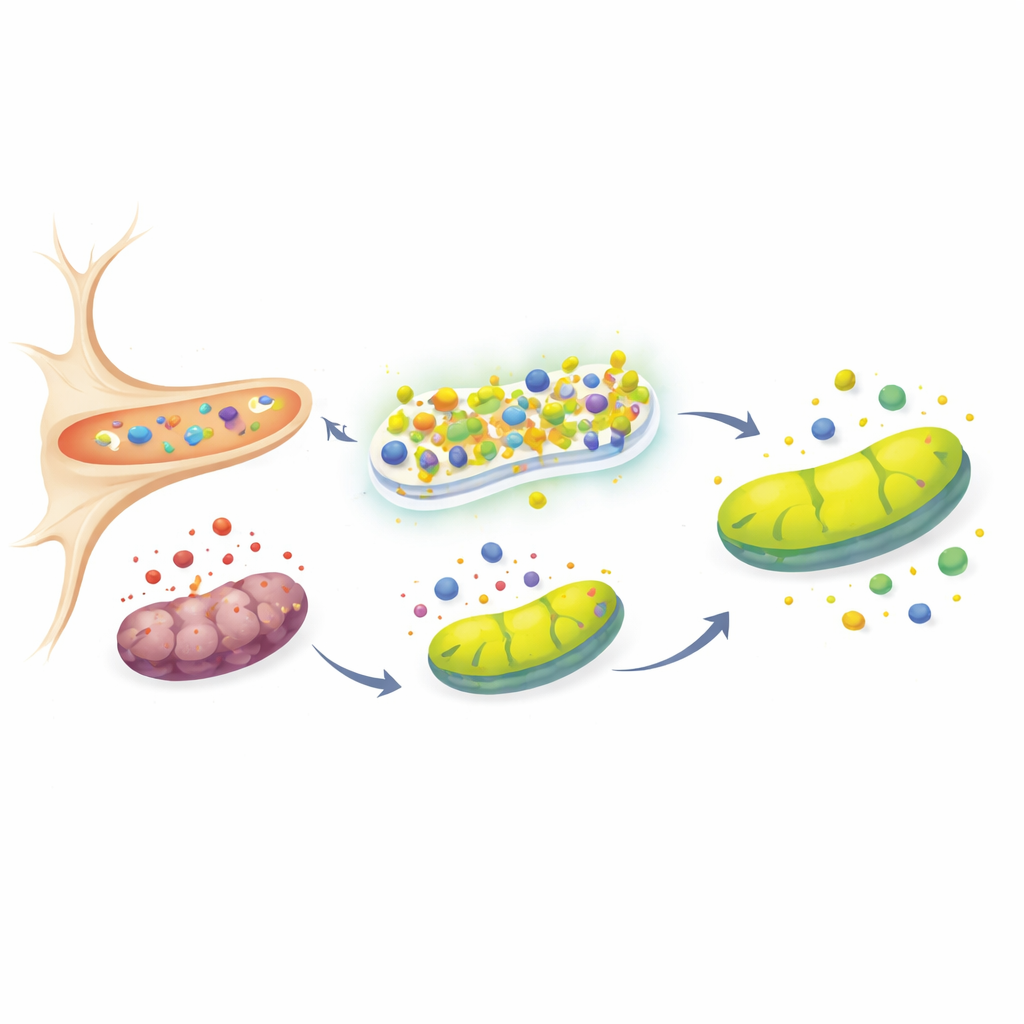
Сохранение работы клеточных электростанций
Митохондрии, часто называемые энергетическими станциями клетки, одновременно являются и важным источником, и основным объектом повреждений при окислительном стрессе. Ключевой показатель их здоровья — мембранный электрический потенциал, который падает при повреждении. После обработки токсином в контрольных клетках наблюдалась явная потеря этого потенциала, сигнализировавшая о митохондриальном стрессе, тогда как в клетках с избытком URG7 значения оставались близкими к норме. Затем команда изучила белки, тесно связанные с контролем качества митохондрий и болезнью Паркинсона: PINK1, Parkin и DJ‑1. В здоровых клетках PINK1 постоянно удаляется из митохондрий; он накапливается лишь при повреждении этих органелл. В клетках со сверхэкспрессией URG7 PINK1 оставался низким несмотря на воздействие токсина, что согласуется с сохранённой целостностью митохондрий. Одновременно Parkin и DJ‑1 — оба связанные с поддержкой митохондриальной функции и антиоксидантной защиты — были повышены, что наводит на мысль, что URG7 поддерживает более широкую защитную сеть, стабилизирующую митохондрии и ограничивающую гибель клеток.
Что это может значить для будущих терапий
Проще говоря, эта работа показывает, что URG7 ведёт себя как ранний сторожевой сигнал внутри нервоподобных клеток. При росте окислительного стресса клетки с избытком URG7 лучше включают защитные гены, наращивают детоксикационные ферменты и сохраняют свои энергетические фабрики, существенно повышая шансы на выживание в среде, похожей на болезнь Паркинсона. Хотя эти эксперименты выполнены в культуре клеток, а не в живом мозге, они выделяют URG7 как перспективную мишень для разработок, направленных на защиту нейронов от окислительных повреждений и митохондриальной недостаточности — двух ключевых факторов болезни Паркинсона и других нейродегенеративных расстройств.
Цитирование: Nigro, I., Miglionico, R., Lela, L. et al. Targeting oxidative stress and mitochondrial dysfunction via URG7 overexpression in an in vitro Parkinson’s disease neuronal model. Sci Rep 16, 9955 (2026). https://doi.org/10.1038/s41598-026-38925-6
Ключевые слова: Болезнь Паркинсона, окислительный стресс, защита митохондрий, нейропротекция, белок URG7