Clear Sky Science · sv
Målinriktning av oxidativ stress och mitokondriell dysfunktion genom ökad uttryckning av URG7 i en in vitro‑neuronal modell för Parkinsons sjukdom
Varför det är viktigt att skydda hjärnceller
Parkinsons sjukdom berövar människor rörelseförmåga och självständighet i långsam takt, och dagens behandlingar lindrar i bästa fall symtom utan att stoppa den underliggande skadan. Många forskare misstänker att en huvudorsak är en intern ”rostning” av hjärnceller, driven av skadliga syrebaserade molekyler som angriper cellernas energifabriker, mitokondrierna. Den här studien undersöker ett relativt okänt protein kallat URG7 och ställer en enkel men viktig fråga: om vi ökar mängden av detta protein i nervliknande celler, kan det hjälpa dem att stå emot denna typ av intern nedbrytning?
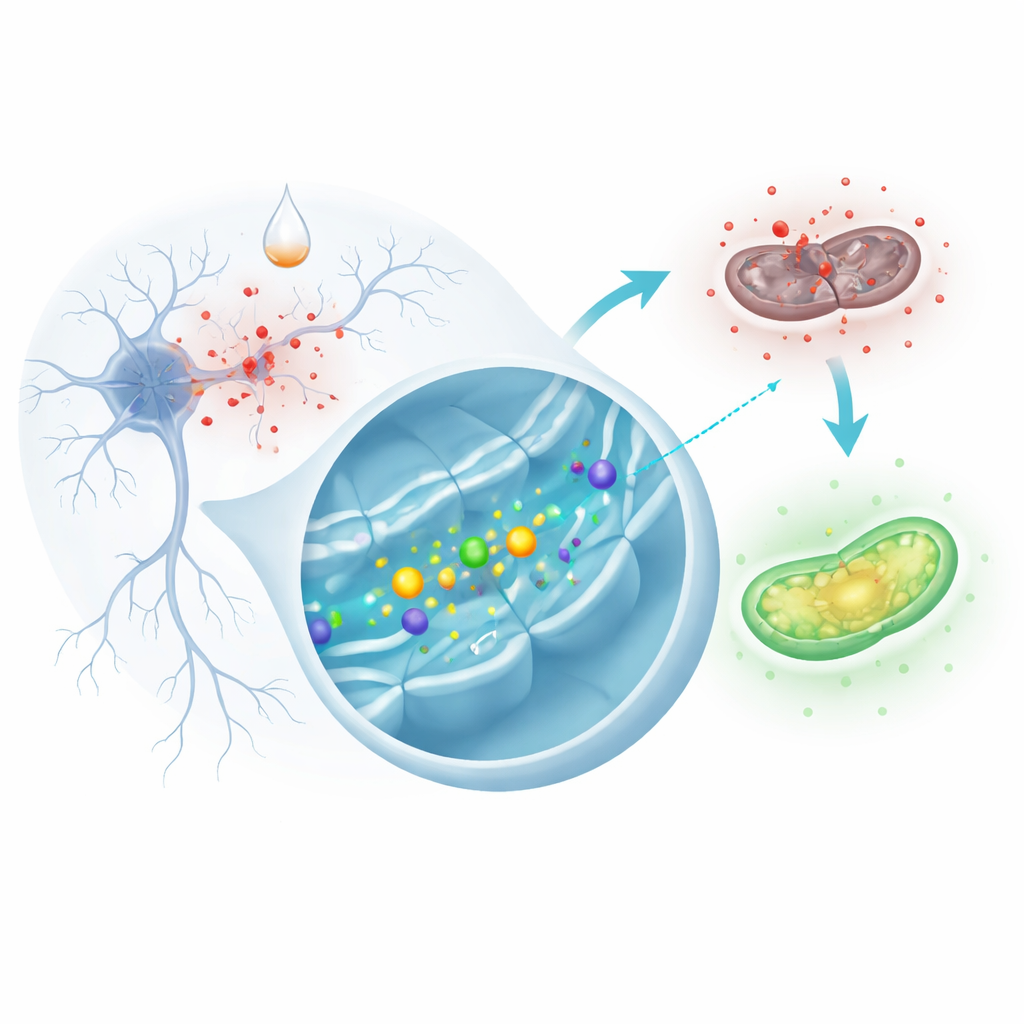
En laboratoriestånd‑in för Parkinson‑skada
Eftersom det är svårt att iaktta levande mänskliga hjärnceller när de degenererar använder forskare ofta odlade celler som ersättning. Här använde teamet SH‑SY5Y‑celler, en mänsklig cellinje som kan efterlikna många egenskaper hos neuroner. De exponerade dessa celler för en kemikalie kallad 6‑hydroxydopamin, som ofta används för att reproducera centrala aspekter av Parkinsons sjukdom i laboratoriet. När det kommer in i cellerna genererar denna förening snabbt reaktiva syreradikaler—kortlivade, mycket reaktiva molekyler som kan skada proteiner, fetter och DNA—vilket leder till mitokondriell kollaps och i slutändan celldöd. Forskarna jämförde vanliga celler med celler genetiskt modifierade för att producera extra URG7, ett litet protein som är lokaliserat till det endoplasmatiska retikulumet, cellens centrum för proteinbearbetning och signalering.
Färre dödande celler och lugnare oxidativ stress
När båda celltyperna utmanades med ökande doser av det toxiska ämnet överlevde URG7‑rika celler avsevärt bättre. Under mikroskopet började kontrollceller runda ihop sig, förlora sina grenliknande utskott och släppa från odlingsytan—en klassisk bild av stressade, döende neuroner—medan URG7‑överuttryckande celler i stort behöll form och antal. Mätningar av reaktiva syreradikaler bekräftade detta visuella intryck: i kontrollceller steg de oxidativa signalerna brant med ökande dos, men i URG7‑celler höll de sig nära baslinjen, särskilt vid den dos som valdes för fördjupad analys. Detta antyder att URG7 inte bara sitter passivt i cellen; det hjälper aktivt till att dämpa uppsvinget av skadliga oxidantmolekyler.
Att stärka cellens egna försvar
För att förstå hur URG7 utövar denna skyddande effekt granskade forskarna centrala komponenter i cellens interna försvarssystem. De undersökte enzymer som katalas och superoxiddismutas 2, vilka tryggt bryter ner skadliga syremolekyler, samt huvudregulatorn Nrf2, som slår på många avgiftande gener. I URG7‑överuttryckande celler var alla tre uppreglerade på både RNA‑ och proteinnivå, och katalasaktiviteten ökade i stället för att sjunka efter toxinput. Markörer för skada berättade samma historia från motsatt håll: nivåerna av malondialdehyd, en biprodukt från fetter som skadats genom oxidation, steg kraftigt i kontrollceller men var mycket lägre när URG7 fanns närvarande. Tillsammans visar dessa fynd att URG7 fungerar som en tidig koordinator som höjer cellens eget antioxidativa verktygslåda snarare än att direkt neutralisera oxidanten.
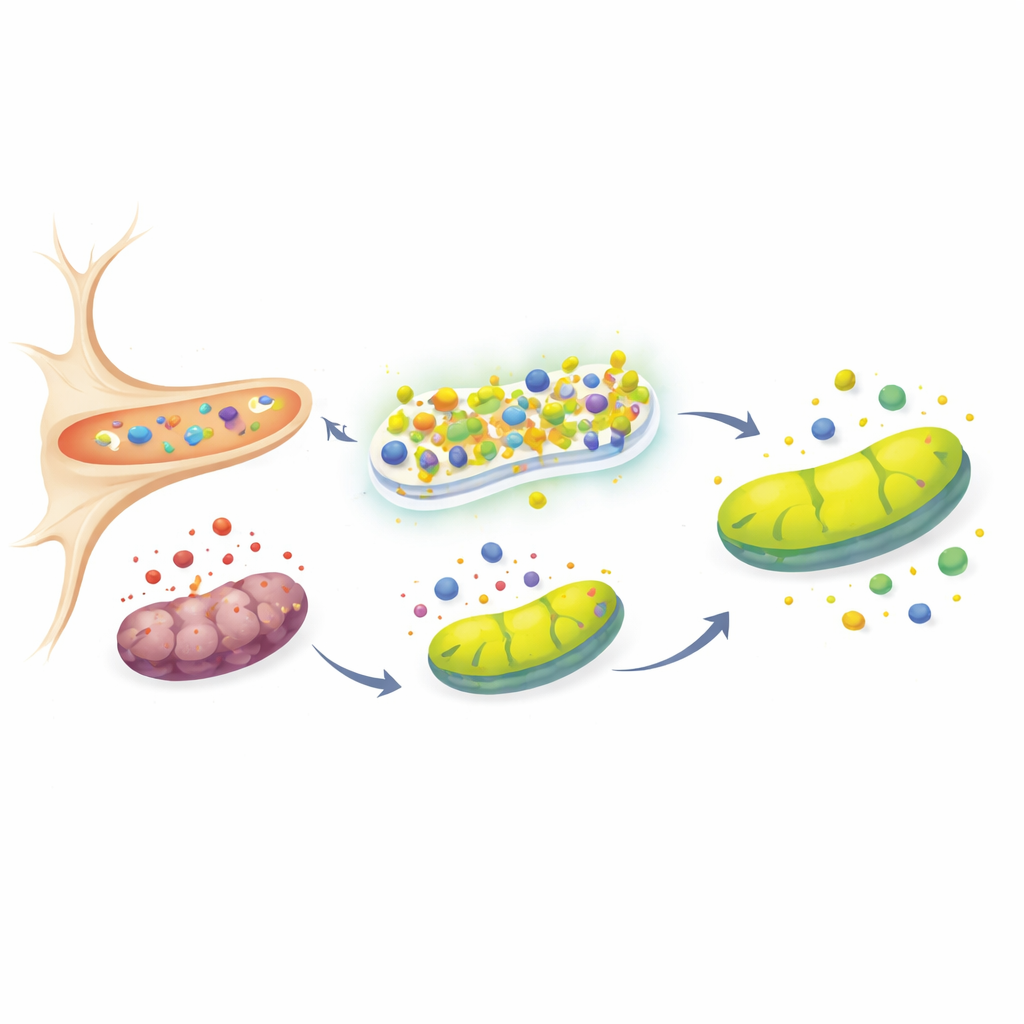
Att hålla cellens kraftverk igång
Mitokondrierna, ofta kallade cellens kraftverk, är både en huvudkälla och ett primärt offer för oxidativ stress. En viktig indikator på deras hälsa är den elektriska potentialen över deras membran, vilken sjunker när de är skadade. Efter toxinput visade kontrollceller en tydlig förlust av denna potential, ett tecken på mitokondriell svikt, medan URG7‑rika celler behöll nära‑normala värden. Teamet undersökte sedan proteiner tätt knutna till mitokondriell kvalitetskontroll och Parkinsons sjukdom: PINK1, Parkin och DJ‑1. I friska celler rensas PINK1 kontinuerligt från mitokondrier; det ackumuleras bara när dessa organeller skadas. I URG7‑överuttryckande celler förblev PINK1 låg trots toxinet, i linje med bevarad mitokondriell integritet. Samtidigt var Parkin och DJ‑1—båda kopplade till stöd för mitokondriell funktion och antioxidativt försvar—uppreglerade, vilket antyder att URG7 hjälper till att upprätthålla ett bredare skyddsnät som stabiliserar mitokondrier och begränsar celldöd.
Vad detta kan betyda för framtida terapier
Enkelt uttryckt tyder detta arbete på att URG7 beter sig som en tidig varningssentinel inne i nervliknande celler. När oxidativ stress ökar är URG7‑rika celler bättre rustade att slå på skyddsgener, öka avgiftande enzymer och hålla sina energifabriker intakta, vilket väsentligt förbättrar deras överlevnad i en Parkinson‑lik miljö. Även om dessa experiment utfördes i en odlingsskål och inte i levande hjärnor, lyfter de fram URG7 som ett lovande nytt mål för behandlingar avsedda att skydda neuroner från oxidativ skada och mitokondriell kollaps—två centrala drivkrafter i Parkinsons sjukdom och andra neurodegenerativa tillstånd.
Citering: Nigro, I., Miglionico, R., Lela, L. et al. Targeting oxidative stress and mitochondrial dysfunction via URG7 overexpression in an in vitro Parkinson’s disease neuronal model. Sci Rep 16, 9955 (2026). https://doi.org/10.1038/s41598-026-38925-6
Nyckelord: Parkinsons sjukdom, oxidativ stress, mitokondriellt skydd, neuroprotektion, URG7‑protein