Clear Sky Science · fr
Cibler le stress oxydatif et la dysfonction mitochondriale via la surexpression de l’URG7 dans un modèle neuronal in vitro de la maladie de Parkinson
Pourquoi protéger les cellules cérébrales est important
La maladie de Parkinson prive progressivement les personnes de leurs mouvements et de leur autonomie ; les traitements actuels ne font qu’atténuer les symptômes sans arrêter la progression. De nombreux chercheurs soupçonnent qu’un des principaux responsables est une « rouille » interne des cellules cérébrales, provoquée par des molécules oxygénées nocives qui attaquent les usines à énergie de la cellule, les mitochondries. Cette étude explore une protéine peu connue nommée URG7 et pose une question simple mais importante : si l’on augmente la quantité de cette protéine à l’intérieur de cellules de type nerveux, peut‑elle les aider à résister à ce type d’usure interne ?
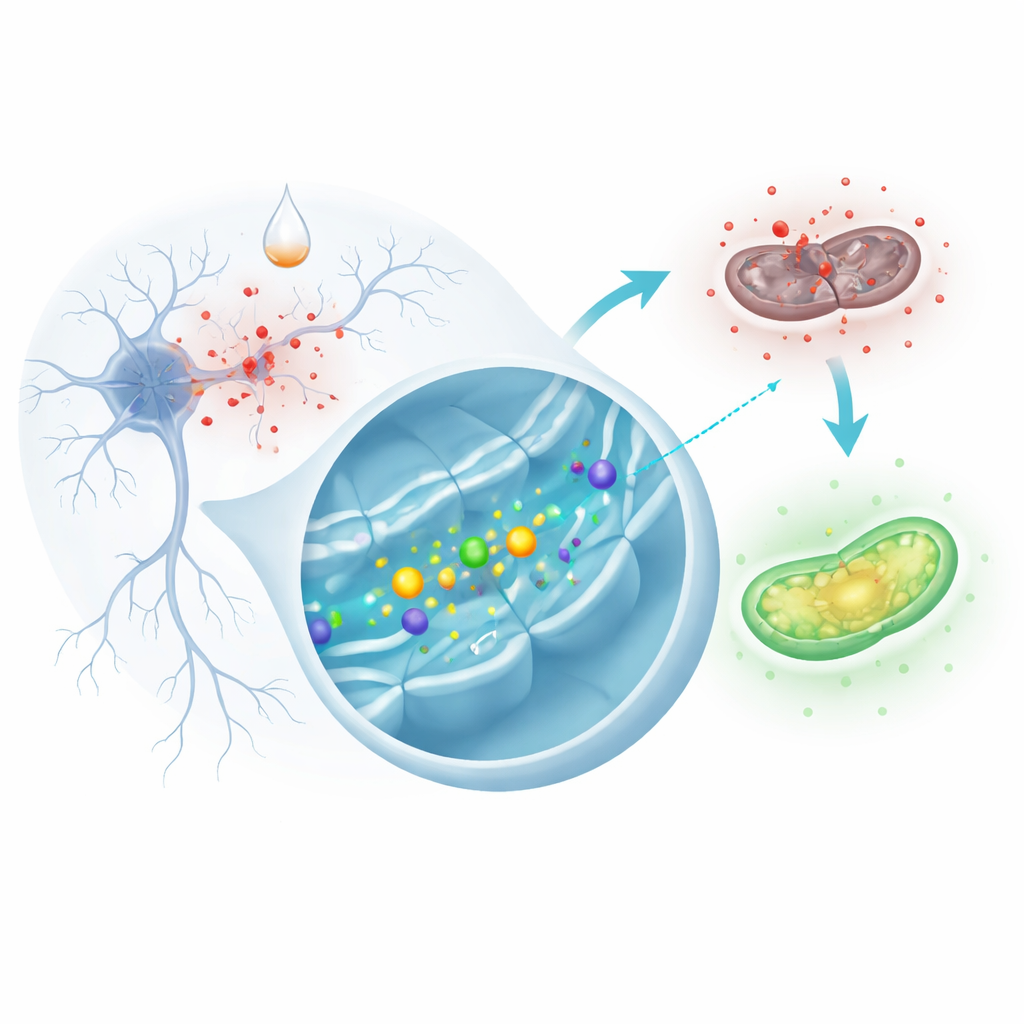
Un substitut en laboratoire aux lésions de Parkinson
Parce qu’il est difficile d’observer la dégénérescence des cellules cérébrales humaines vivantes, les chercheurs utilisent souvent des cellules en culture comme modèle. Ici, l’équipe a utilisé des cellules SH‑SY5Y, une lignée humaine capable d’imiter de nombreuses caractéristiques des neurones. Ils ont exposé ces cellules à un composé appelé 6‑hydroxydopamine, largement utilisé pour reproduire en laboratoire des aspects clés de la maladie de Parkinson. Une fois à l’intérieur des cellules, ce composé génère rapidement des espèces réactives de l’oxygène — des molécules courtes et très réactives qui peuvent endommager protéines, lipides et ADN — entraînant une défaillance mitochondriale et finalement la mort cellulaire. Les scientifiques ont comparé des cellules ordinaires avec des cellules génétiquement modifiées pour produire davantage d’URG7, une petite protéine localisée dans le réticulum endoplasmique, le centre de traitement et de signalisation des protéines de la cellule.
Moins de cellules mourantes et un stress oxydatif apaisé
Lorsque les deux types cellulaires ont été exposés à des doses croissantes du composé toxique, les cellules riches en URG7 ont survécu de manière significative davantage. Au microscope, les cellules témoins se sont mises à se rétracter, à perdre leurs prolongements en forme de branches et à se détacher du milieu — une image classique de neurones stressés et en mort — tandis que les cellules surexprimant l’URG7 ont globalement conservé leur forme et leur nombre. Les mesures des espèces réactives de l’oxygène ont confirmé cette impression visuelle : dans les cellules témoins, les signaux oxydatifs augmentaient fortement avec la dose de toxique, alors que dans les cellules URG7 ils restaient proches de la ligne de base, en particulier à la dose retenue pour les études approfondies. Cela suggère que l’URG7 ne se contente pas d’être passive dans la cellule ; elle contribue activement à limiter l’augmentation des oxydants dommageables.
Renforcer les défenses intrinsèques de la cellule
Pour comprendre comment l’URG7 exerce cet effet protecteur, les chercheurs ont étudié des éléments clés du système de défense cellulaire. Ils ont examiné des enzymes telles que la catalase et la superoxyde dismutase 2, qui décomposent en toute sécurité les espèces d’oxygène nocives, ainsi que la protéine contrôleur maîtresse Nrf2, qui active de nombreux gènes de détoxification. Dans les cellules surexprimant l’URG7, ces trois éléments étaient augmentés au niveau de l’ARN et des protéines, et l’activité de la catalase elle‑même augmentait au lieu de diminuer après l’exposition au toxique. Les marqueurs de dommages confirment le même constat sous un autre angle : les niveaux de malondialdéhyde, un sous‑produit de l’oxydation des lipides, montaient fortement dans les cellules témoins mais restaient bien plus bas en présence d’URG7. Ensemble, ces résultats indiquent que l’URG7 agit comme un coordinateur en amont, augmentant l’activité de l’arsenal antioxydant de la cellule plutôt que de neutraliser directement les oxydants.
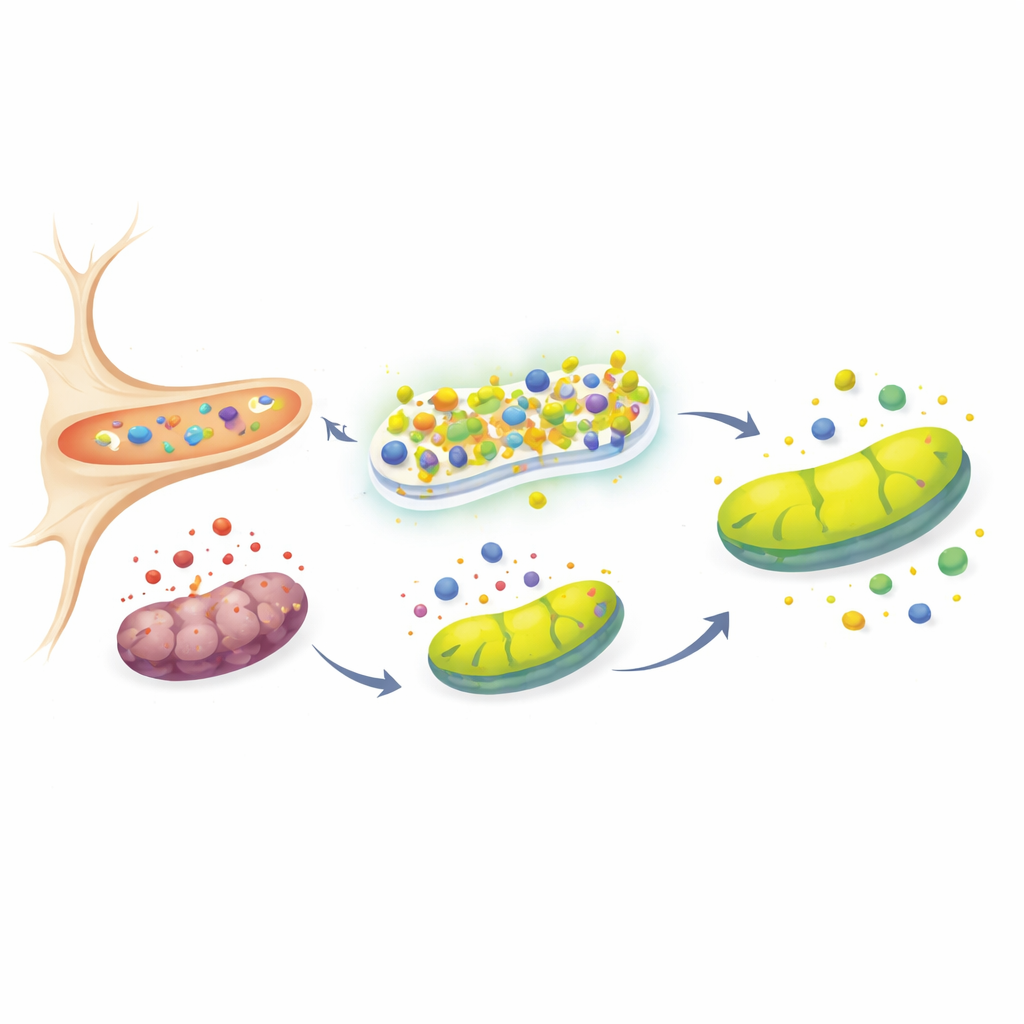
Maintenir les centrales énergétiques cellulaires opérationnelles
Les mitochondries, souvent qualifiées de centrales électriques de la cellule, sont à la fois une source majeure et une victime de choix du stress oxydatif. Un indicateur clé de leur santé est le potentiel électrique à travers leur membrane, qui chute lorsqu’elles sont endommagées. Après traitement au toxique, les cellules témoins ont montré une perte nette de ce potentiel, signe de détresse mitochondriale, alors que les cellules riches en URG7 ont maintenu des valeurs proches de la normale. L’équipe a ensuite examiné des protéines étroitement liées au contrôle de la qualité mitochondriale et à la maladie de Parkinson : PINK1, Parkin et DJ‑1. Dans des cellules saines, PINK1 est constamment éliminé des mitochondries ; il ne s’accumule que lorsque ces organites sont endommagés. Dans les cellules surexprimant l’URG7, PINK1 restait bas malgré le toxique, cohérent avec une intégrité mitochondriale préservée. Parallèlement, Parkin et DJ‑1 — tous deux associés au soutien de la fonction mitochondriale et à la défense antioxydante — étaient régulés à la hausse, suggérant que l’URG7 aide à maintenir un réseau protecteur plus large qui stabilise les mitochondries et limite la mort cellulaire.
Ce que cela pourrait signifier pour des thérapies futures
En termes simples, ce travail suggère que l’URG7 se comporte comme un sentinelle d’alerte précoce à l’intérieur des cellules de type nerveux. Lorsque le stress oxydatif augmente, les cellules riches en URG7 sont mieux à même d’activer des gènes protecteurs, d’augmenter les enzymes détoxifiantes et de préserver leurs usines énergétiques, améliorant fortement leurs chances de survie dans un environnement semblable à la maladie de Parkinson. Bien que ces expériences aient été réalisées en culture et non dans des cerveaux vivants, elles mettent en évidence l’URG7 comme une nouvelle cible prometteuse pour des traitements visant à protéger les neurones contre les dommages oxydatifs et la défaillance mitochondriale — deux moteurs centraux de la maladie de Parkinson et d’autres troubles neurodégénératifs.
Citation: Nigro, I., Miglionico, R., Lela, L. et al. Targeting oxidative stress and mitochondrial dysfunction via URG7 overexpression in an in vitro Parkinson’s disease neuronal model. Sci Rep 16, 9955 (2026). https://doi.org/10.1038/s41598-026-38925-6
Mots-clés: Maladie de Parkinson, stress oxydatif, protection mitochondriale, neuroprotection, protéine URG7