Clear Sky Science · zh
蒽醌苷(Physcion-8-O-β-D-单葡萄糖苷)通过抑制PI3K/AKT/NF-κB信号通路保护肝细胞免受TNF-α介导的凋亡
这为何关系到肝脏健康
肝病正在成为全球日益严重的问题,许多病例起始于一种称为急性肝损伤的突发且剧烈的肝细胞损害。这类损伤若不控制,可迅速导致肝功能衰竭,而现有治疗手段有限。本文所基于的研究探索了一种来自传统中药的天然化合物,可能有助于保护肝细胞免受机体自身最具破坏性的炎性信号之一的伤害。
具有现代潜力的植物化合物
本研究聚焦的化合物为蒽醌苷(physcion-8-O-β-D-monoglucoside,简称PMG),存在于大黄类根茎(Radix et Rhizoma Rhei)中,这种类大黄根在中医中用于治疗肝病。既往研究表明粗提物及相关分子可能具有护肝作用,但它们吸收差且作用机制不明。PMG为一种更易被吸收的形式,经口给药后在血液中可达到更高水平。作者先前观察到PMG能减轻小鼠的毒素诱导性肝损伤,本研究旨在揭示其在细胞和分子层面的具体作用机制。
压低一种危险的警报信号
肿瘤坏死因子-α(TNF-α)是急性肝损伤中的关键角色,它是免疫细胞释放的一种强烈警报信号。TNF-α与肝细胞表面的受体TNFR1结合,可促使这些细胞走向程序性死亡和炎症反应。研究者在小鼠肝细胞培养与受四氯化碳损伤的小鼠模型中均显示,PMG帮助细胞抵御TNF-α驱动的压力。在细胞培养中,PMG本身对健康细胞无害,但当添加TNF-α及致敏药物时,PMG能恢复细胞存活、改善细胞形态,并减少进入培养液的肝酶泄漏——即细胞损伤的标志。
受损小鼠肝脏的证据
在活体小鼠中,四氯化碳导致了急性肝损伤的典型表现:组织结构破坏、大量细胞死亡,以及血中肝酶(AST和ALT)显著升高。预处理PMG的动物肝组织明显更健康,酶水平更低,显微染色也显示细胞死亡更少。PMG还降低了肝脏自身产生的TNF-α及另一种炎性因子白细胞介素-6的水平。当研究组用基因载体强制使肝脏过度表达TNF-α时,PMG的这些保护作用大多消失。这一逆转强烈表明PMG的保护效应依赖于抑制TNF-α及其下游结果。
阻断细胞内有害的连锁反应
为探明PMG如何抑制TNF-α信号,研究者考察了细胞内著名的分子级连锁事件——PI3K/AKT/NF-κB通路。该通路一旦过度激活,会增强促炎基因表达并促进细胞死亡。研究团队采用计算分子对接显示,PMG可直接与TNFR1受体结合,支持其在信号起始的第一步就发挥干预作用的观点。在四氯化碳损伤的小鼠肝脏中,活化的PI3K和AKT、核内的NF-κB水平均升高,细胞执行程序性死亡的标志性蛋白裂解型caspase-3亦增加。PMG处理降低了这些信号并减弱了caspase-3的激活。然而,当TNF-α被人为过度产生时,这些保护性改变消失,信号通路再次被激活。
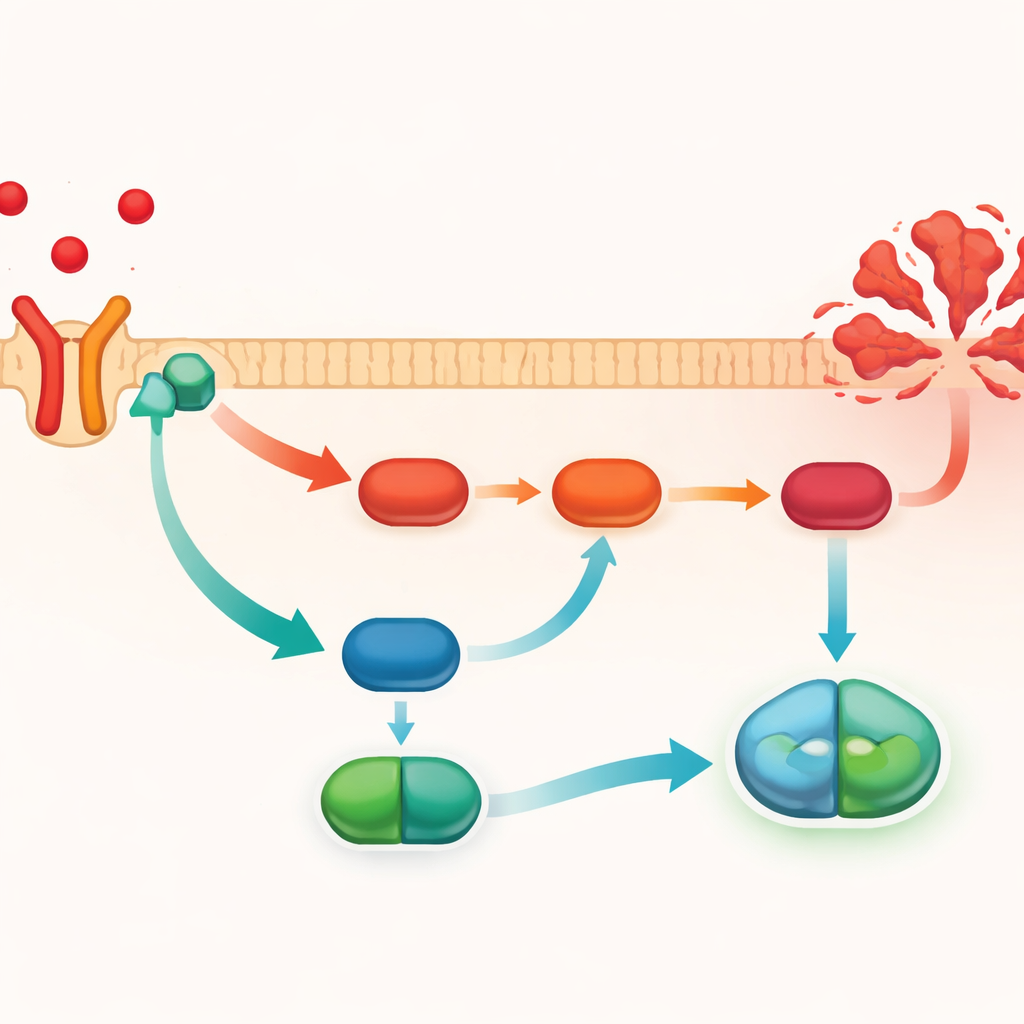
这对未来治疗的可能意义
综上所述,研究结果勾勒出一个清晰图景:PMG似乎通过在受体层面阻断TNF-α信号并平抑PI3K/AKT/NF-κB通路,从而保护肝细胞免受急性炎性损伤。尽管该工作在小鼠和细胞模型中完成,但它为一种植物来源分子作为急性肝损伤潜在药物候选者提供了机制依据。后续仍需进一步研究以评估安全性、剂量以及在人体中是否能获得类似益处,但该研究强调了传统疗法如何启发现代靶向护肝治疗的可能性。
引用: Hu, R., Chen, Z., Chen, T. et al. Physcion-8-O-β-D-monoglucoside protects hepatocytes from TNF-α-mediated apoptosis by suppressing the PI3K/AKT/NF-κB signaling pathway. Sci Rep 16, 12716 (2026). https://doi.org/10.1038/s41598-026-38701-6
关键词: 急性肝损伤, 炎症, 肿瘤坏死因子, 中医药, 护肝