Clear Sky Science · fr
La physcion-8-O-β-D-monoglucoside protège les hépatocytes de l’apoptose médiée par le TNF-α en supprimant la voie de signalisation PI3K/AKT/NF-κB
Pourquoi cela compte pour la santé du foie
Les maladies du foie sont un problème mondial croissant, et de nombreux cas débutent par des lésions soudaines et intenses des cellules hépatiques, appelées lésions hépatiques aiguës. Ce type de lésion peut rapidement évoluer vers une insuffisance hépatique si elle n’est pas maîtrisée, alors que les traitements actuels restent limités. L’étude à l’origine de cet article explore un composé naturel, dérivé d’une plante de la médecine traditionnelle chinoise, qui pourrait aider à protéger les cellules du foie contre l’un des signaux inflammatoires internes les plus délétères.
Un composé végétal revisité
Le composé étudié ici s’appelle physcion-8-O-β-D-monoglucoside (PMG), présent dans Radix et Rhizoma Rhei, une racine ressemblant à la rhubarbe utilisée en médecine traditionnelle chinoise pour les affections hépatiques. Des travaux antérieurs suggéraient que des extraits bruts et des molécules apparentées pouvaient protéger le foie, mais ils étaient mal absorbés et leurs mécanismes précis restaient flous. Le PMG est une forme mieux absorbable, atteignant des niveaux plus élevés dans le sang après administration orale. Les auteurs avaient auparavant montré que le PMG pouvait atténuer les lésions hépatiques induites par des toxines chez la souris ; ici, ils cherchent à élucider précisément son mode d’action aux niveaux cellulaire et moléculaire.
Atténuer un signal d’alarme dangereux
Un acteur clé des lésions hépatiques aiguës est le facteur de nécrose tumorale-alpha (TNF-α), un puissant signal d’alarme libéré par les cellules immunitaires. Le TNF-α se lie à un récepteur des hépatocytes nommé TNFR1 et peut pousser ces cellules vers la mort programmée et l’inflammation. En utilisant à la fois des cellules hépatiques murines en culture et des souris exposées à un produit chimique hépatotoxique (le tétrachlorure de carbone), les chercheurs ont montré que le PMG aide ces cellules à résister au stress induit par le TNF-α. En culture cellulaire, le PMG n’endommageait pas les cellules saines à lui seul, mais lorsque le TNF-α et un médicament sensibilisant étaient ajoutés, le PMG a restauré la survie cellulaire, amélioré la morphologie des cellules et réduit la fuite d’enzymes hépatiques — marqueurs de lésions cellulaires — dans le milieu de culture.
Preuves tirées du foie de souris blessées
Chez l’animal, le tétrachlorure de carbone a provoqué des signes classiques de lésion hépatique aiguë : altération de la structure tissulaire, nécrose cellulaire étendue et forte élévation des enzymes hépatiques (AST et ALT) dans le sang. Les animaux prétraités par le PMG présentaient un tissu hépatique sensiblement plus sain, des taux enzymatiques plus faibles et moins de cellules en train de mourir selon plusieurs méthodes de coloration microscopique. Le PMG a également réduit la production hépatique de TNF-α lui-même et d’une autre cytokine inflammatoire, l’interleukine-6. Lorsque l’équipe a forcé le foie à produire davantage de TNF-α via un virus délivrant un gène, les bénéfices du PMG ont en grande partie disparu. Cette inversion suggère fortement que les effets protecteurs du PMG dépendent du maintien du TNF-α et de ses conséquences en aval sous contrôle.
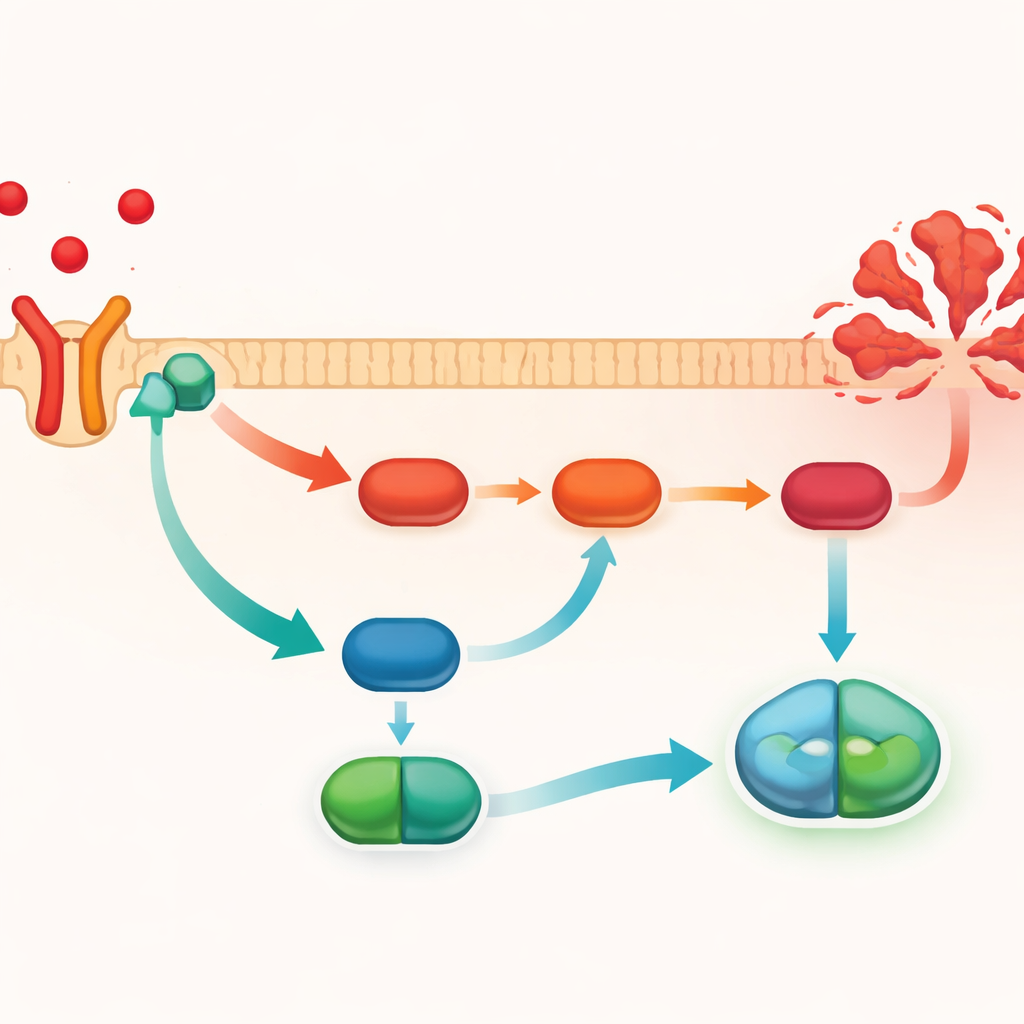
Bloquer une réaction en chaîne délétère à l’intérieur des cellules
Pour comprendre comment le PMG tempère le signal du TNF-α, les chercheurs ont examiné une cascade moléculaire bien connue à l’intérieur des cellules : la voie PI3K/AKT/NF-κB. Lorsqu’elle est hyperactivée, cette voie augmente l’expression de gènes inflammatoires et favorise la mort cellulaire. L’équipe a utilisé le dock moléculaire assisté par ordinateur pour montrer que le PMG peut se lier directement au récepteur TNFR1, soutenant l’idée qu’il interfère dès la première étape du signalement. Dans les foies de souris endommagés par le tétrachlorure de carbone, les niveaux de PI3K et AKT activés ainsi que de NF-κB nucléaire étaient tous augmentés, de même que la protéine exécutrice clivée caspase-3, un marqueur de suicide cellulaire. Le traitement par le PMG a atténué tous ces signaux et réduit l’activation de la caspase-3. Cependant, lorsque le TNF-α était surproduit artificiellement, ces changements protecteurs disparaissaient et la voie de signalisation repartait à la hausse.
Ce que cela pourrait signifier pour les traitements futurs
Pris ensemble, les résultats brossent un tableau clair : le PMG semble protéger les cellules hépatiques contre les lésions inflammatoires aiguës en bloquant le signal du TNF-α à son récepteur et en calmant la voie PI3K/AKT/NF-κB qui, autrement, stimulerait l’inflammation et la mort cellulaire. Bien que ce travail ait été réalisé chez la souris et sur des cellules en culture, il fournit une base mécanistique pour un composé d’origine végétale en tant que candidat-médicament potentiel pour la lésion hépatique aiguë. Des études supplémentaires seront nécessaires pour évaluer la sécurité, les posologies et la transposabilité de ces bénéfices chez l’homme, mais l’étude illustre comment des remèdes traditionnels peuvent inspirer des thérapies modernes ciblées pour protéger l’un des organes les plus vitaux du corps.
Citation: Hu, R., Chen, Z., Chen, T. et al. Physcion-8-O-β-D-monoglucoside protects hepatocytes from TNF-α-mediated apoptosis by suppressing the PI3K/AKT/NF-κB signaling pathway. Sci Rep 16, 12716 (2026). https://doi.org/10.1038/s41598-026-38701-6
Mots-clés: lésion hépatique aiguë, inflammation, facteur de nécrose tumorale, médecine traditionnelle chinoise, protection du foie