Clear Sky Science · de
Physcion-8-O-β-D-monoglucosid schützt Hepatozyten vor TNF-α-vermittelter Apoptose durch Unterdrückung des PI3K/AKT/NF-κB-Signalwegs
Warum das für die Lebergesundheit wichtig ist
Lebererkrankungen nehmen weltweit zu, und viele Fälle beginnen mit einer plötzlichen, intensiven Schädigung der Leberzellen, die als akute Leberschädigung bezeichnet wird. Diese Art von Schädigung kann ohne Gegenmaßnahmen schnell zur Leberinsuffizienz führen, doch die verfügbaren Behandlungen sind begrenzt. Die Studie hinter diesem Artikel untersucht eine natürliche Verbindung, die aus einem pflanzlichen Mittel der traditionellen chinesischen Medizin gewonnen wird und die Leberzellen vor einem der schädlichsten entzündlichen Signale des Körpers schützen könnte.
Eine Pflanzenverbindung mit modernem Anspruch
Die in dieser Arbeit zentrale Verbindung heißt Physcion-8-O-β-D-monoglucosid (PMG) und kommt in Radix et Rhizoma Rhei vor, einer rhabarberähnlichen Wurzel, die in der traditionellen chinesischen Medizin bei Leberleiden verwendet wird. Frühere Untersuchungen deuteten darauf hin, dass rohe Extrakte und verwandte Moleküle die Leber schützen können, aber sie wurden schlecht resorbiert und ihre genauen Wirkmechanismen waren unklar. PMG ist eine besser aufnehmbare Form und erreicht nach oraler Gabe höhere Blutspiegel. Die Autorinnen und Autoren beobachteten zuvor, dass PMG die durch Toxine ausgelöste Leberschädigung bei Mäusen mindern kann, und in dieser Studie wollten sie genau aufklären, wie es auf zellulärer und molekularer Ebene wirkt.
Ein gefährliches Alarmsignal dämpfen
Ein entscheidender Akteur bei akuter Leberschädigung ist Tumornekrosefaktor-alpha (TNF-α), ein starkes Alarmsignal, das von Immunzellen freigesetzt wird. TNF-α bindet an einen Rezeptor auf Leberzellen, genannt TNFR1, und kann diese Zellen in Richtung programmierter Zellsterblichkeit und Entzündung treiben. Anhand von kultivierten Maus-Leberzellen und Mäusen, die einem leberschädigenden Chemikalium (Tetrachlorkohlenstoff) ausgesetzt wurden, zeigten die Forschenden, dass PMG diesen Zellen hilft, den durch TNF-α ausgelösten Stress zu überstehen. In Zellkulturen schädigte PMG gesunde Zellen nicht, aber wenn TNF-α und ein sensibilisierendes Medikament hinzugefügt wurden, stellte PMG das Überleben der Zellen wieder her, verbesserte ihre Morphologie und verringerte das Auslaufen von Leberenzymen – Marker für Zellschädigung – in das Kulturmedium.
Belege aus verletzten Mauslebern
In lebenden Mäusen führte Tetrachlorkohlenstoff zu klassischen Zeichen akuter Leberschädigung: Störung der Gewebearchitektur, weitverbreiteter Zelltod und stark erhöhte Spiegel von Leberenzymen (AST und ALT) im Blut. Tiere, die mit PMG vorbehandelt wurden, zeigten deutlich gesündere Lebergewebe, niedrigere Enzymwerte und weniger absterbende Zellen bei verschiedenen mikroskopischen Färbemethoden. PMG verringerte außerdem die Leberproduktion von TNF-α selbst sowie eines weiteren entzündlichen Botenstoffs, Interleukin-6. Als das Team die Leber mittels eines Genübertragungs-Virus dazu brachte, vermehrt TNF-α zu produzieren, verschwanden die Vorteile von PMG weitgehend. Diese Umkehrung legt nahe, dass die schützenden Effekte von PMG davon abhängen, TNF-α und seine nachgeschalteten Folgen in Schach zu halten.
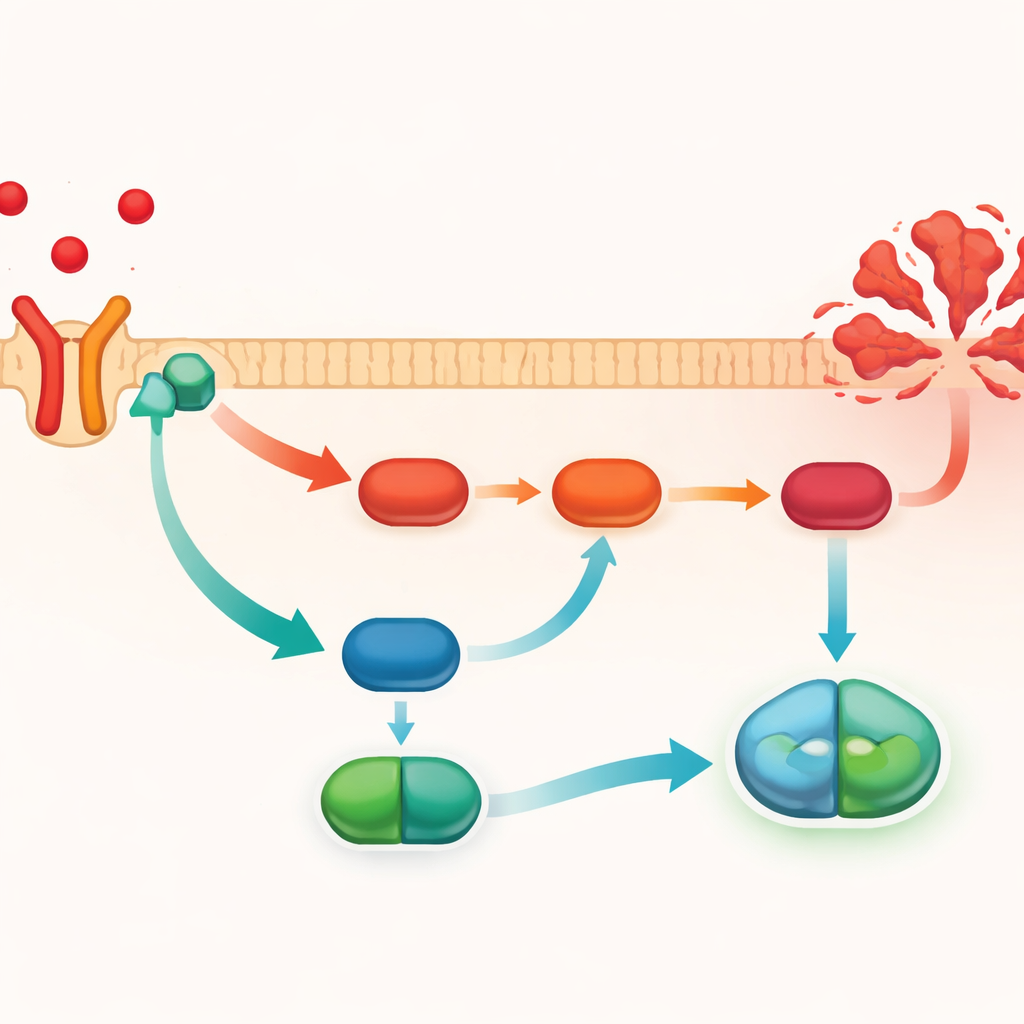
Eine schädliche Kettenreaktion in der Zelle blockieren
Um zu verstehen, wie PMG das TNF-α-Signal zügelt, untersuchten die Forschenden eine bekannte Abfolge molekularer Ereignisse in der Zelle, den PI3K/AKT/NF-κB-Signalweg. Wenn dieser Weg überaktiviert ist, fördert er die Aktivität entzündlicher Gene und begünstigt Zellsterben. Das Team nutzte computergestützte molekulare Docking-Studien, die zeigten, dass PMG direkt an den TNFR1-Rezeptor binden kann, was die Idee stützt, dass es bereits am ersten Schritt der Signalübertragung eingreift. In den durch Tetrachlorkohlenstoff geschädigten Mauserbern waren die Spiegel aktivierter PI3K und AKT sowie nukleäres NF-κB erhöht, ebenso wie das Ausführungsprotein gespaltenes Caspase-3, ein Kennzeichen der programmierten Zellselbsttötung. Die PMG-Behandlung dämpfte all diese Signale und verringerte die Caspase-3-Aktivierung. Wurde jedoch TNF-α künstlich überproduziert, gingen diese schützenden Veränderungen verloren und der Signalweg flammte wieder auf.
Was das für künftige Therapien bedeuten könnte
In der Gesamtschau zeichnen die Ergebnisse ein klares Bild: PMG scheint Leberzellen vor akuter entzündlicher Schädigung zu schützen, indem es das TNF-α-Signal am Rezeptor blockiert und den PI3K/AKT/NF-κB-Weg beruhigt, der sonst Entzündung und Zellsterben antreibt. Obwohl diese Arbeit an Mäusen und in Zellkulturen durchgeführt wurde, liefert sie eine mechanistische Grundlage dafür, dass ein pflanzlich abgeleitetes Molekül als potenzieller Wirkstoffkandidat bei akuter Leberschädigung dienen könnte. Weitere Studien sind nötig, um Sicherheit, Dosierung und Übertragbarkeit der Effekte auf den Menschen zu prüfen, doch die Untersuchung zeigt, wie traditionelle Heilmittel moderne, zielgerichtete Therapien zum Schutz eines der wichtigsten Organe des Körpers inspirieren können.
Zitation: Hu, R., Chen, Z., Chen, T. et al. Physcion-8-O-β-D-monoglucoside protects hepatocytes from TNF-α-mediated apoptosis by suppressing the PI3K/AKT/NF-κB signaling pathway. Sci Rep 16, 12716 (2026). https://doi.org/10.1038/s41598-026-38701-6
Schlüsselwörter: akute Leberschädigung, Entzündung, tumornekrosefaktor, traditionelle chinesische Medizin, Leberprotektion